Inhibition activity of 4-O-α-thevetopyranosyldiphyllin on Spirogyra communis and its effect on chloroplast ultrastructure
-
摘要:目的
探究从秃杉Taiwania flousiana中提取得到的除草活性物质秃杉素(4-O-α-thevetopyranosyldiphyllin, TSC-3)对水生植物水绵Spirogyra communis的抑制活性和对其叶绿体的影响。
方法采用乙醇萃取−分光光度法测定秃杉素对水绵叶绿素和类胡萝卜素的IC50。采用显微镜以及透射电镜技术观察不同质量浓度秃杉素对水绵显微结构和超微结构的影响。
结果经秃杉素处理7 d后,水绵的类胡萝卜素、叶绿素a、叶绿素b及总色素的IC50分别为3.41、31.50、47.34和29.30 mg·L−1。秃杉素能破坏水绵细胞的细胞壁,引起细胞膜消失、叶绿体解体、类囊体完全消失、淀粉粒分散以及蛋白核降解和碎片化。
结论秃杉素可降低水绵叶绿素a、叶绿素b和类胡萝卜素的含量,对类胡萝卜素的抑制较其他色素更强;秃杉素主要作用于叶绿体和细胞壁。本研究为解释植物源除草化合物秃杉素的除草机理提供了基础的理论依据,也为水生藻类的防控提供了理论依据。
Abstract:ObjectiveThe inhibition activity of 4-O-α-thevetopyranosyldiphyllin(TSC-3), extracted from Taiwania flousiana, on Spirogyra communis and its effect on S. communis chloroplast were investigated.
MethodThe IC50 of 4-O-α-thevetopyranosyldiphyllin on chlorophyll and carotenoids in S. communis were determined by the ethanol extraction-spectrophotometric method. The effects of 4-O-α-thevetopyranosyldiphyllin on the microstructure and ultrastructure of S. communis were observed using microscopy and transmission electron microscopy.
ResultThe IC50 of 4-O-α-thevetopyranosyldiphyllin on the contents of carotenoids, chlorophyll a, chlorophyll b and total pigments of S. communis after 7 d treatment were 3.41, 31.50, 47.34 and 29.30 mg·L−1, respectively. Further investigation showed that 4-O-α-thevetopyranosyldiphyllin could destroy the cells of S. communis, inducing broken cell wall, disappeared cell membrane, disintegrated chloroplast, completely disappeared thylakoids, dispersed starch granules, degraded and fragmented pyrenoids.
Conclusion4-O-α-thevetopyranosyldiphyllin can reduce the contents of chlorophyll a, chlorophyll b and carotenoids in S. communis. The inhibition rate of carotenoids was higher than those of the other pigments. 4-O-α-thevetopyranosyldiphyllin mainly acts on the chloroplasts and cell walls. This study provides a basis for further study of the molecular herbicidal mechanism of the plant-derived herbicidal chemical 4-O-α-thevetopyranosyldiphyllin, and also provides a theoretical basis for the control of aquatic algae.
-
Keywords:
- Botanical herbicide /
- 4-O-α-thevetopyranosyldiphyllin /
- Spirogyra communis /
- Chloroplast /
- Thylakoid
-
精密播种可实现1穴1粒和固定株距,从而减少用种量、降低劳动强度、节本增效。排种器作为播种机的核心部件直接决定播种精度[1-2]。油菜种子粒径小,其精密排种器设计难度大[3]。气力式排种器适用于高速作业,生产效率高,对种子适应性强、损伤轻,但结构复杂、加工成本高,且风机动力消耗大、性能不稳定[4];窝眼轮式精密排种器属机械式,对不同粒径种子通用性差,但结构简单、加工成本低、性能可靠,在我国精密播种机上应用广泛[5-6]。
型孔是窝眼轮式精密排种器结构组成的重要部分,其形状及参数直接影响排种器的工作性能。Garcia [7]研究发现型孔的形状、尺寸对排种精度有着重要的影响;Wang [8]根据种子尺寸对排种器型孔参数进行了优化设计;吴兆迁等[9]设计了针对不同粒径种子孔深可调的窝眼轮排种器,解决了播量调节不便的问题;宋井玲等[10]设计了1种利用凸轮活销机构实现工作过程中孔深可变的型孔轮式排种器,适用于玉米、大豆等大粒种子。而油菜种子粒径小、流动性强,对窝眼轮型孔结构要求更高,但是目前国内对于窝眼轮式油菜精密排种器型孔结构的研究甚少,使得适用于油菜等小籽粒种子的窝眼轮排种器设计理论不足。
传统的试验周期长、成本高,随着计算机技术的发展,计算机辅助分析方法在排种器研究领域的应用日渐增多。Zhang等[11]采用离散元法研究了大豆在斜槽中的流动过程;石林榕等[6]借助EDEM软件对水平圆盘式精量排种器排种进行了仿真试验。本文利用离散单元颗粒分析软件EDEM,对不同型孔结构的窝眼轮式油菜精密排种器工作机理进行仿真分析和验证试验,探寻不同型孔结构对窝眼轮排种器种子群扰动及工作性能的影响,为窝眼轮式油菜精密排种器的设计工作提供理论依据。
1. 种子群扰动机理分析
1.1 接触模型的建立
排种器工作时,种箱中的油菜种子在窝眼轮转动作用下发生扰动,引起种子间的碰撞产生接触力[12-13]。离散元分析方法中将接触模型分为软颗粒接触和硬颗粒接触,其中软颗粒接触模型可以允许碰撞持续一定的时间,并同时考虑多个颗粒的碰撞,根据颗粒碰撞重叠量和切向位移来计算接触力[14], 种子群扰动与该接触力紧密相关。考虑到油菜种子无表面粘附力,故选择Hertz-Mindlin(no slip)软颗粒接触模型[15-16]。将该模型的接触简化为有耦合器和滑动器的弹簧振子阻尼振动,如图 1所示,其运动微分方程为:

式中,m为模型粒子质量;u为偏离平衡位置位移;c为接触阻尼系数;K为弹簧弹性系数。
1.2 接触力分析
软接触颗粒碰撞模型中接触力可分解为法向力和切向力,其中法向力是模型中弹性力和阻尼力的合力。对于油菜籽的三维球形颗粒,由Hertz接触理论,法向力Fn以及切向力Ft可分别表示为:

式中kn、kt分别为法向及切向弹力系数;cn、ct分别为法向和切向阻尼系数;α为法向重叠量;νij为颗粒i与j的相对速度;νct为接触点滑移速度;δ为切向位移;n为颗粒i与颗粒j接触面的法向单位矢量。
若下式成立:

则颗粒i与颗粒j发生相对滑动,此时有:

式中μs为静摩擦因数,由油菜种子的物理特性确定,为定值;nt为切向单位向量。由公式可知,种子之间的内摩擦力即上述接触模型中的切向力是由法向力确定的,也是产生种子群扰动的主要因素[17-18]。因此以法向接触力Fn为内摩擦力的监测值分析不同型孔结构各轮种子群扰动强度,探寻型孔结构对窝眼轮式油菜精密排种器排种性能的影响。
2. 仿真分析
2.1 窝眼轮式排种器结构及工作原理
窝眼轮式油菜精密排种器由窝眼轮、外壳、清种刷、护种板、排种轴等组成,如图 2所示。排种器充种角度为90°,护种区包角为120°。窝眼轮直径、厚度分别为60、20 mm。为减少漏播,型孔底部窝眼直径D应不小于种子最大尺寸,小于2粒种子的最小尺寸和,孔深H应等于或略大于种子的最大尺寸[9, 19],根据试验所用种子的物理特性,设计D、H分别为2.5、2.3 mm。按型孔倒角不同,结合窝眼轮材料特性及油菜种子的三维尺寸、摩擦角等物理特性,根据不同倒角参数仿真结果,设计了30°倒角(A轮)、不倒角(B轮)以及半径1.25 mm倒圆角(C轮)3种窝眼轮。为确保型孔完整的同时尽可能多地布置型孔以提高充种能力和工作效率,根据窝眼轮直径和型孔尺寸,确定窝眼轮圆周面均布型孔数目为30个。A、B、C 3种窝眼轮结构如图 3所示。
工作时,排种轴带动窝眼轮匀速转动,油菜种子在重力及种间接触力的作用下由种箱进入型孔完成充种过程,经过清种刷后随着窝眼轮进入护种区,转出护种区后,靠重力作用落下,进入种沟,完成排种过程。
2.2 模型建立及仿真
借助Pro-E软件建立排种器模型,定义清种刷为尼龙材料、其余部件为有机玻璃;建立输送带模型,并定义种子与输送带为完全非弹性碰撞。模型导入EDEM软件后网格显示如图 4所示。
种子与种子、种子与排种器之间选用Hertz-Mindlin(no slip)接触模型,种子与输送带之间选择Moving Plan接触模型;导入模型并按表 1、2设置材料特性及材料间接触参数[13, 20-21]。设置颗粒产生方式为静态填充,颗粒半径1 mm并服从正态分布;设置仿真时间步长比例为20%,总时间6 s(第1秒生成颗粒,2~6 s排种),网格尺寸为最小颗粒半径的2倍。
表 1 仿真模型材料参数Table 1. Property parameter of material in the simulation model 表 2 仿真模型材料接触参数Table 2. Contact parameter of material in the simulation model
表 2 仿真模型材料接触参数Table 2. Contact parameter of material in the simulation model
综合考虑油菜种植农艺要求、国内油菜播种机的作业速度水平以及试验排种器的结构参数,在10、20、30、40、50 r·min-1下对A、B、C 3种不同型孔结构的窝眼轮排种器进行仿真分析。图 5显示了各轮30 r·min-16 s时的仿真情况,种箱里种子的堆积情况反映出种子群扰动量为:A轮>C轮>B轮。
2.3 仿真结果分析
2.3.1 不同型孔结构对种子群扰动的影响
30 r·min-1时,A、B、C 3种窝眼轮上方同一位置框选区域中,种子颗粒间接触的平均法向应力以及颗粒的平均速度随时间波动如图 6、7所示。图 6显示各轮平均法向应力随时间变化无规律波动,其中A轮波动最明显,C轮其次,B轮波动最小;A、B、C 3轮平均法向应力均值并无明显区别。由图 7可知,种子颗粒平均速度为:A轮>C轮>B轮。图 6中B轮在5.5~5.8 s法向应力波动变小,而图 7中显示该时段B轮种子颗粒的平均速度也显著降低,观察仿真录像发现B轮此时段充种情况较差(图 8),可见平均法向应力波动能有效反映种子群扰动,且种子群扰动对充种性能影响显著。种子群扰动量越大,种子运动越剧烈,种子瞬时平均速度也越大,更容易在重力和相互碰撞作用下进入型孔完成充种过程。
图 9反映了各轮上方框选区域中种间平均法向应力的均值和方差随转速提高的变化情况。图 9a显示,各轮的法向应力均值均随转速提高先增大后趋于平缓,此过程中B、C轮比A轮先达到拐点;10~30 r·min-1转速下,三轮的法向应力均值出现交叉,转速超过30 r·min-1后,各轮法向应力均值差异逐渐明显。由图 9b可知,A、B、C轮法向应力方差随转速提高而增大,B轮增幅明显小于A、C轮,此过程中,A、B、C轮方差排序为:A轮>C轮>B轮。结合前文所述法向应力、种子群扰动及充种性能的关系可知,相同转速下,各轮的种子群扰动量关系为:A轮>C轮>B轮,且A轮充种性能最好。
2.3.2 不同型孔结构对排种器各工作指标的影响
每次仿真完成后,输出输送带上表面框选区域中油菜种子x坐标值以获取粒距样本,按文献[22]所述方法,对排种器的基本性能指标:粒距合格指数、漏播指数、重播指数、变异系数进行计算,排种性能仿真结果见图 10。
图 10a表明,各轮合格指数均随转速的提高而降低,且A轮>C轮>B轮,且随着转速的提高,各轮合格指数间差值呈增大趋势,型孔结构不同使得各轮的种子群扰动量、充种性能不同。图 10b表明各轮重播指数均随转速的提高而降低,且A轮>C轮>B轮,观察仿真录像发现,型孔结构差异使得A轮型孔的囊种空间大于B轮和C轮,当2粒直径较小的种子同时出现在型孔上方时,A轮出现重播的可能性比B、C轮大。图 10c表明,各轮漏播指数均随转速提高而增加,且B轮>C轮>A轮,且各轮漏播指数差值随转速提高逐渐增大,A轮相比于B、C轮漏播指数增速较为平缓;对照图 9可知,就各轮自身而言,工作转速是影响其漏播的主要因素,平均法向应力的均值和方差对漏播影响不大,而相同转速下,各轮之间对比发现,法向应力方差对漏播影响显著,法向应力方差越大则漏播指数越小,而平均法向应力均值的影响不明显。图 10d表明,各轮的变异系数均随转速提高而增大,A轮变异系数最大,B、C轮变异系数差异不明显,在20、50 r·min-1时两者出现交叉;在EDEM中观察种子运动轨迹发现A轮的投种位置变动较大,故其投种时间间隔误差大,粒距变异系数大,这是由于型孔结构导致种子进入A轮型孔后活动范围大所致。
3. 验证试验与分析
按仿真模型参数定制了A、B、C 3种窝眼轮,安装到同一个窝眼轮排种器上,在南京农业大学工学院自制的铺砂式排种性能测试台上进行试验,其工作原理及参数见文献[23]。以仿真建模所参照的中双11号油菜种子为试验材料,测得其平均粒径1.72 ~2.21 mm、千粒质量4.68 g、密度1.06 g·cm-3、容重0.67 g·cm-3、纯净度98.5%。
试验选取与仿真相同的5种转速,每次试验添加到种箱的种子均为89 g(与仿真时约19 060粒种子质量相同),监测指标及计算方法与仿真分析相同。排种性能试验结果如图 11所示。
对比图 10、11发现,试验中各排种性能指标在数值上与仿真结果有一定偏差,但其变化趋势及其相互之间大小关系与仿真结果基本一致。由图 10a、11a可知,试验中各轮的合格指数随转速提高而下降的速度比仿真中要快,仿真中转速从10 r·min-1增加到50 r·min-1时A、B、C轮的合格指数分别从96.1%、93.1%、94.2%降低到89.8%、75.9%、81.5%,而试验结果中A、B、C轮的合格指数分别从95.8%、90.6%、93.5%降低到86.6%、67.5%、79.2%。B轮合格指数受转速影响最大、C轮次之、A轮最小。由图 10b、11b可以看出,各轮重播指数在试验与仿真中结果差异不明显。由图 10c、11c可知,试验中各轮漏播指数均高于相同转速下仿真中漏播指数,且各轮漏播指数受转速的影响在试验结果中比仿真中表现的更为明显,转速为10 r·min-1时,A、B、C轮试验和仿真漏播指数分别为:0.7%、7.2%、3.0%和0.5%、4.3%、2.4%,当转速增加到50 r·min-1时,A、B、C轮试验和仿真漏播指数分别升高到:12.4%、32.3%、20.1%和9.3%、23.9%、18.1%,可见B轮漏播指数受转速变化的影响最大,A轮最小,这与前文所述不同型孔结构对种子群扰动量及囊种空间大小的影响一致。观察图 10d、11d发现,变异系数随转速提高而上升,但试验中各轮变异系数均比相同转速下仿真中变异系数大,这与种子落到输送带时弹跳、粒距测量精度、输送带速度均匀性、排种器工作转速稳定性等因素有关。
通过仿真及试验发现,A轮在重播指数和变异系数略高于B、C轮的同时,其漏播指数和合格指数明显优于B轮和C轮,对高速作业具有更强的适应性。
4. 结论
1) 借助离散元分析软件EDEM,以接触平均法向应力均值和方差为监测值研究了型孔结构对窝眼轮排种器种子群扰动的影响,发现相同转速下A轮种子群扰动量最大、C轮次之、B轮最小,且种子群扰动量越大充种性能越好。
2) 按仿真建模参数加工了3种窝眼轮,并进行了排种性能验证试验。综合考虑仿真和试验结果,对各轮自身而言,影响其排种性能的主要因素是工作转速,随工作转速提高各轮的合格指数、重播指数均减小,漏播指数、变异系数增大;各轮之间对比发现,相同转速下,种子群扰动量越大漏播指数越小,型孔囊种空间因倒角方式而不同,且囊种空间越大,重播指数、变异系数越大;由于重播指数较小,故合格指数主要受漏播指数影响。试验结果显示,转速在10~50 r·min-1时,种子群扰动最大的A轮合格指数为86.6%~95.8%,明显优于B轮的67.5%~90.6%和C轮的79.2%~93.5%。
3) 仿真与试验的结果在数值上有偏差,但其变化趋势及相互之间大小关系基本一致,用EDEM对排种器进行仿真分析具有一定可行性。
-
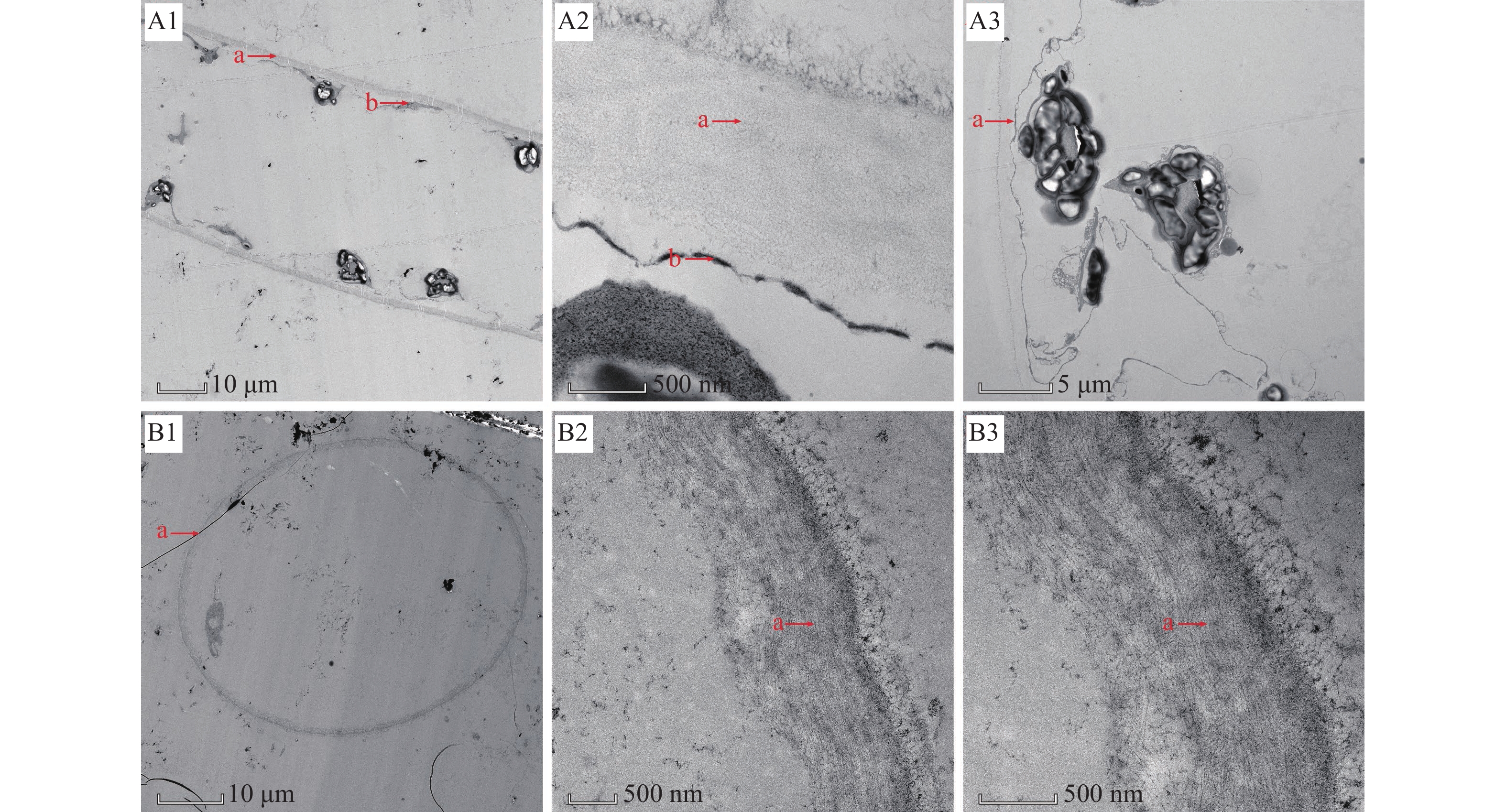
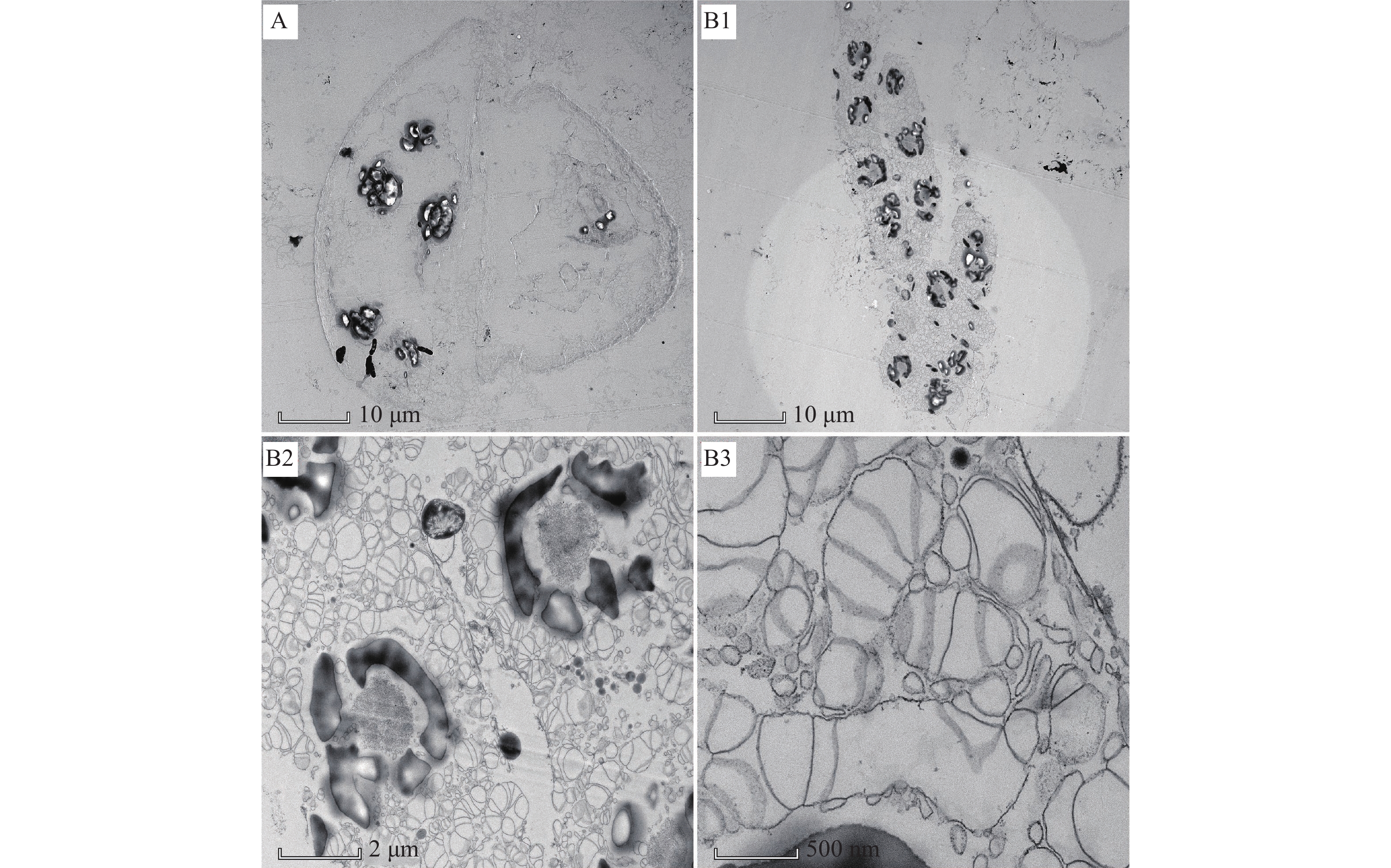
图 3 透射电镜观察2.5 mg·L−1秃杉素处理7 d后水绵细胞壁和细胞膜的变化
A1、A2、A3:对照组;B1、B2、B3:处理组; a:细胞壁;b:细胞膜
Figure 3. Observation of changes in cell walls and membranes of Spirogyra communis after 7 d of treatment with 2.5 mg·L−1 4-O-α-thevetopyranosyldiphyllin using transmission electron microscopy
A1, A2, A3: Control group; B1, B2, B3: Treatment group; a: Cell wall; b: Cell membrane
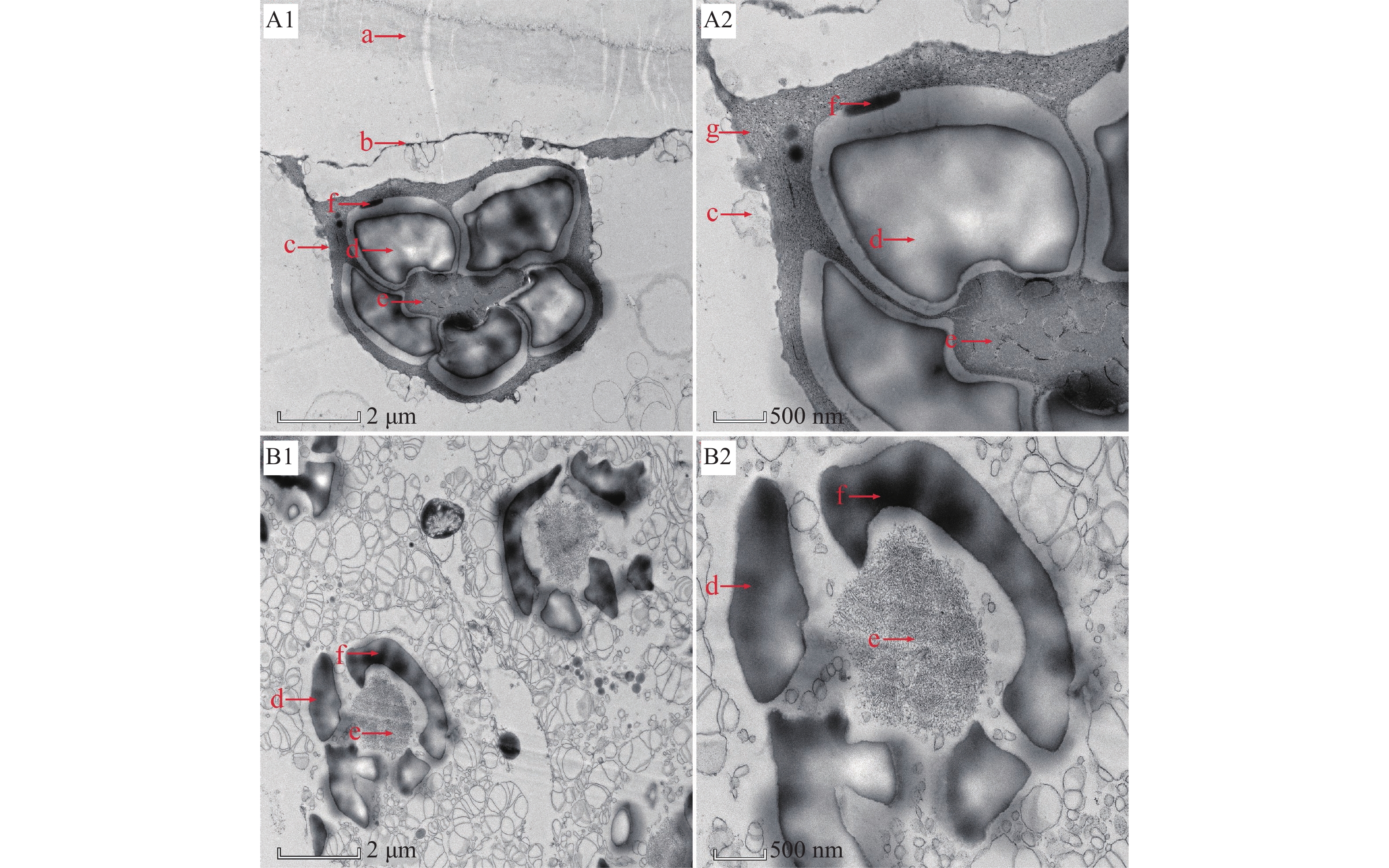
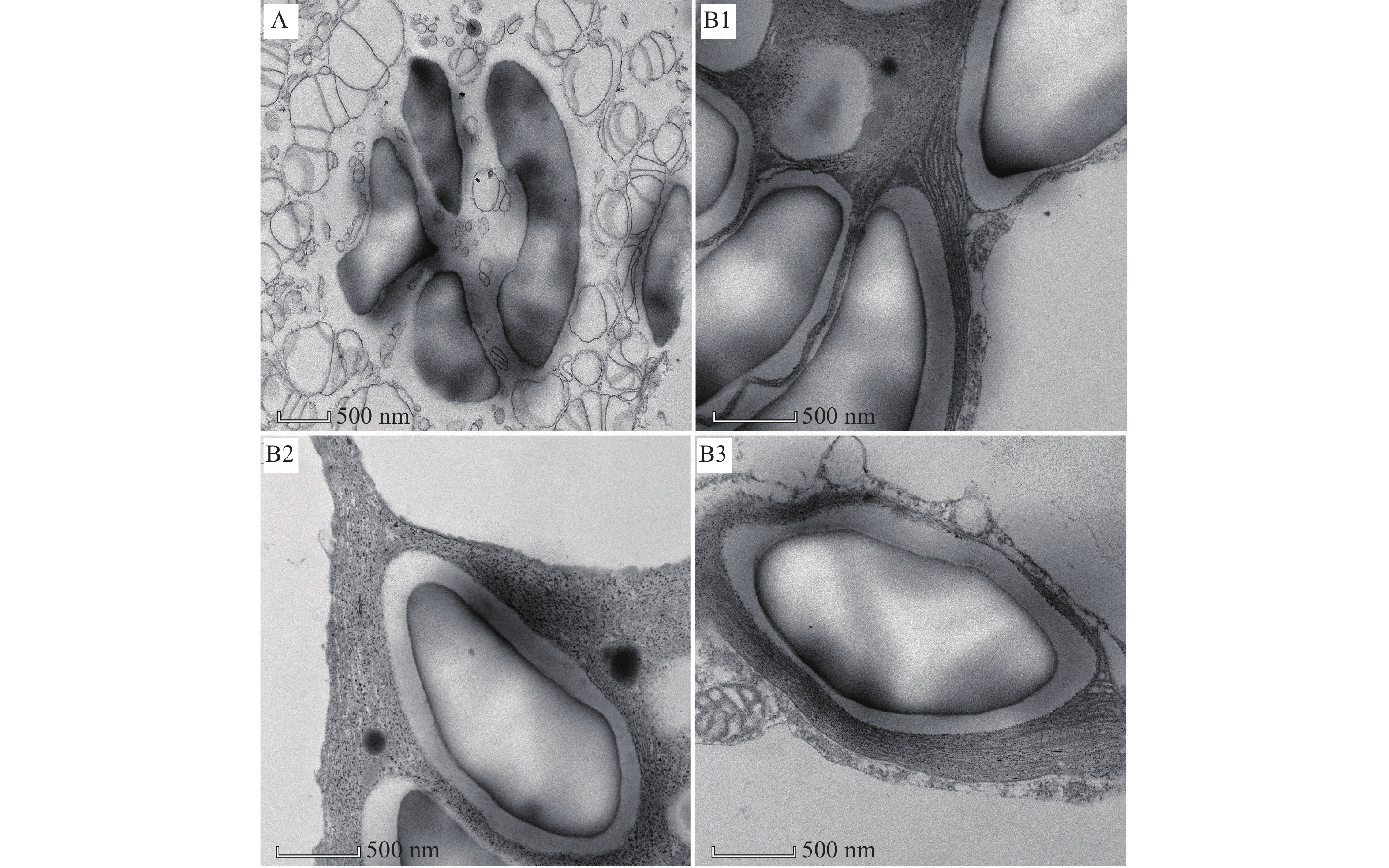
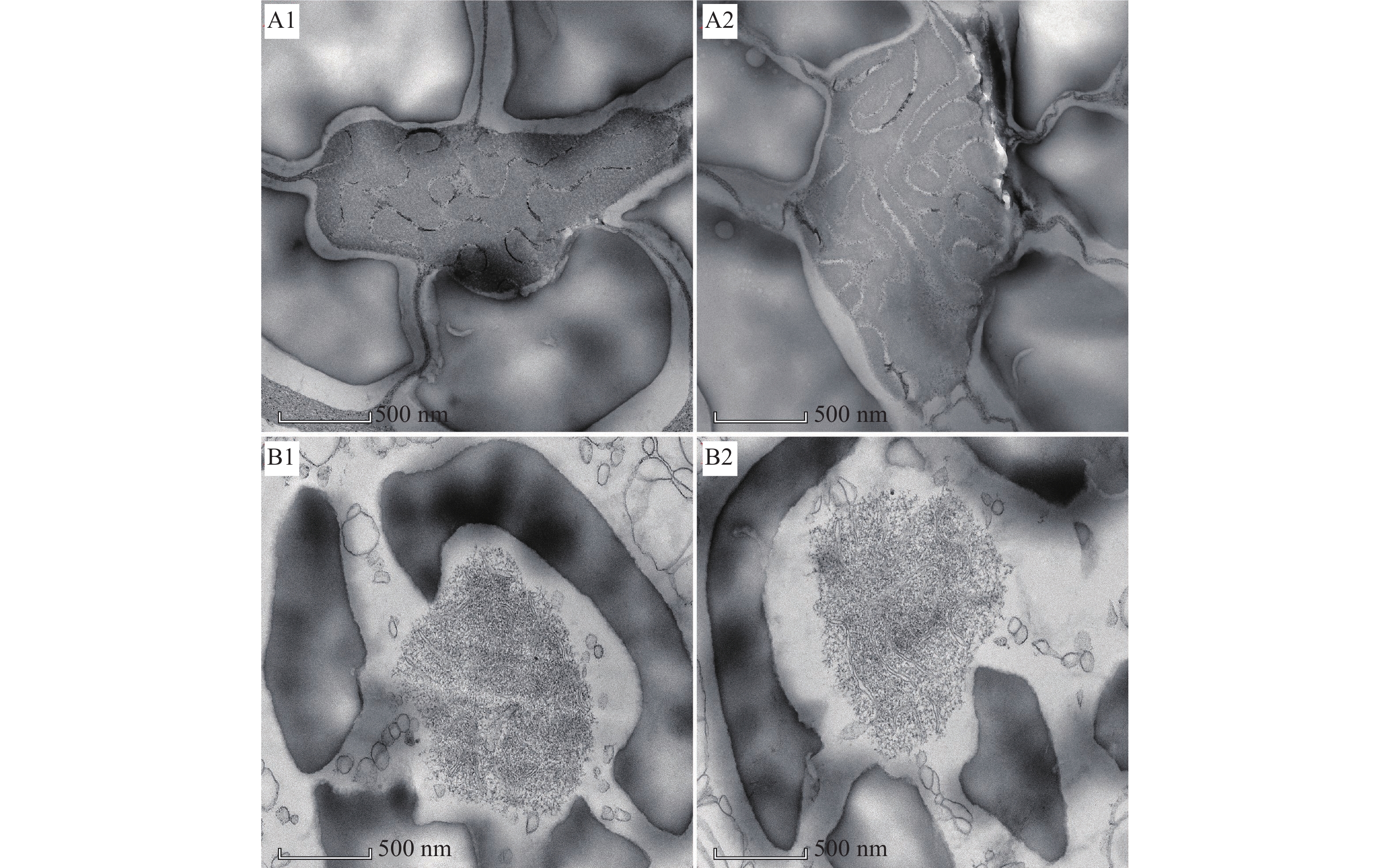
图 4 透射电镜观察2.5 mg·L−1秃杉素处理7 d后水绵细胞叶绿体的变化
A1、A2:对照组;B1、B2:处理组;a:细胞壁;b:细胞膜;c:类囊体;d:淀粉粒;e:蛋白核;f:嗜锇颗粒;g:基粒
Figure 4. Observation of changes in chloroplasts of Spirogyra communis after 7 d of treatment with 2.5 mg·L−1 4-O-α-thevetopyranosyldiphyllin using transmission electron microscopy
A1, A2: Control group; B1, B2: Treatment group; a: Cell wall; b: Cell membrane; c: Thylakoid body; d: Starch granule; e: Protein nucleus; f: Osmium loving granule; g: Basal granule
表 1 不同质量浓度秃杉素对水绵叶绿素和类胡萝卜素的抑制率1)
Table 1 Inhibitory rate of 4-O-α-thevetopyranosyldiphyllin with different mass concentrations on chlorophyll and carotenoid of Spirogyra communis
色素组分
Pigment component抑制率/% Inhibition rate 2.5 mg·L−1 5.0 mg·L−1 10.0 mg·L−1 20.0 mg·L−1 40.0 mg·L−1 类胡萝卜素 Carotenoid 46.25±1.21a 56.22±1.27a 72.50±2.14a 86.23±2.23a 94.98±3.21a 叶绿素a Chlorophyll a 19.97±0.82b 25.01±1.59b 31.25±1.55b 38.74±1.96c 58.76±1.29b 叶绿素b Chlorophyll b 6.23±0.15d 15.01±0.97c 22.52±1.46c 35.63±1.72c 43.75±1.55c 总色素 Total pigment 10.02±0.23c 20.03±1.33b 26.25±0.88bc 44.75±1.01b 60.04±2.07b 1)表中数据为平均数±标准误,n=3;同列数据后的不同小写字母表示差异显著(P<0.05,Duncan’s法)
1)Data in the table is mean ± standard error, n=3; Different lowercase letters of the same column indicate significant differences (P<0.05, Duncan’s method)表 2 秃杉素对水绵叶绿素和类胡萝卜素含量的IC50
Table 2 The IC50 of 4-O-α-thevetopyranosyldiphyllin on the contents of chlorophyll and carotenoid of Spirogyra communis
色素组分
Pigment component回归方程1)
Regression equation相关系数
Correlation index (r)IC50/ (mg·L−1) 95%置信区间/ (mg·L−1)
95% confidence interval类胡萝卜素 Carotenoid y=4.36+1.20x 0.99 3.41 2.06~5.06 叶绿素a Chlorophyll a y=2.79+1.48x 0.97 31.50 22.00~45.09 叶绿素b Chlorophyll b y=2.12+1.72x 0.97 47.34 34.65~64.68 总色素 Total pigment y=2.62+1.62x 0.98 29.30 21.31~40.29 1) x为浓度对数,y为概率单位
1) x is logarithmic concentration, y is probit -
[1] HEAP I. The international herbicide-resistant weed database[DB/OL]. [2023-06-01]. http://www.weedscience.org/Home.aspx.
[2] HULME P E. Global drivers of herbicide-resistant weed richness in major cereal crops worldwide[J]. Pest Management Science, 2022, 78(5): 1824-1832. doi: 10.1002/ps.6800
[3] DUKE S O, DAYAN F E. The search for new herbicide mechanisms of action: Is there a ‘holy grail’?[J]. Pest Management Science, 2022, 78(4): 1303-1313. doi: 10.1002/ps.6726
[4] SPARKS T C, BRYANT R J. Impact of natural products on discovery of, and innovation in, crop protection compounds[J]. Pest Management Science, 2022, 78(2): 399-408. doi: 10.1002/ps.6653
[5] LIU H M, HUANG J G, YANG S F, et al. Chemical composition, algicidal, antimicrobial, and antioxidant activities of the essential oils of Taiwania flousiana Gaussen[J]. Molecules, 2020, 25(4): 967. doi: 10.3390/molecules25040967
[6] LIU L, ZHANG S, DAI W, et al. Comparing effects of berberine on the growth and photosynthetic activities of Microcystis aeruginosa and Chlorella pyrenoidosa[J]. Water Science and Technology, 2019, 80(6): 1155-1162. doi: 10.2166/wst.2019.357
[7] 陈世国, 强胜. 生物除草剂研究与开发的现状及未来的发展趋势[J]. 中国生物防治学报, 2015, 31(5): 770-779. [8] 伏桂仙. 水生植物对城市富营养化水体的净化效果研究[D]. 扬州: 扬州大学, 2022. [9] 孙万里. 大连地区稻田水绵危害性调查与防控方法比较研究[D]. 沈阳: 沈阳农业大学, 2018. [10] WANG W L, ZHU D R, LI L N, et al. Bioactive dimeric diterpenoids from Taiwania cryptomerioides (Hayata) and their biological activities[J]. Chemistry & Biodiversity, 2023, 20(2): e202201067.
[11] NICOLAS W J, BAYER E, BROCARD L. Electron tomography to study the three-dimensional structure of plasmodesmata in plant tissues From high pressure freezing preparation to ultrathin section collection[J]. Bio-protocol, 2018, 8(1): e2681.
[12] 凡传明, 刘云国, 郭一明, 等. 水绵(Spirogyra)对蓝藻复苏及藻类群落结构的影响[J]. 环境科学学报, 2011, 31(10): 2132-2137. [13] JAFFER M, ASHRAF H, SHAHEEN S. Comparative analysis of bio-culturing of fresh water algae, Spirogyra communis (Hassall) Kützing and Hydrodictyon reticulatum L[J]. Bangladesh Journal of Botany, 2019, 48(4): 1125-1132. doi: 10.3329/bjb.v48i4.49068
[14] SHERWOOD A R, NEUMANN J M, DITTBERN-WANG M, et al. Diversity of the green algal genus Spirogyra (Conjugatophyceae) in the Hawaiian Islands[J]. Phycologia, 2018, 57(3): 331-344. doi: 10.2216/17-111.1
[15] SATI M, VERMA M, RAI J P N. Biosorption of Pb (II) by Spirogyra communis: Kinetics and isotherm model studies[J]. Pollution Research, 2015, 34(4): 707-712.
[16] HE S, CRANS V L, JONIKAS M C. The pyrenoid: The eukaryotic CO2-concentrating organelle[J]. The Plant Cell, 2023, 35(9): 3236-3259. doi: 10.1093/plcell/koad157
[17] LINES T, BEARDALL J. Carbon acquisition characteristics of six microalgal species isolated from a subtropical reservoir: Potential implications for species succession[J]. Journal of Phycology, 2018, 54(5): 599-607. doi: 10.1111/jpy.12770
[18] SEAL T, HALDER N, CHAUDHURI K, et al. Effect of solvent extraction system on the antioxidant activities of algae[J]. International Journal of Pharmacy & Pharmaceutical Sciences, 2014, 6(10): 242-245.
[19] GUO B, ZHAO M, WU Z, et al. 19-nor-pimaranes from Icacina trichantha[J]. Fitoterapia, 2020, 144: 104612. doi: 10.1016/j.fitote.2020.104612
[20] DAI W, ZHANG J, TU Q, et al. Bacterioplankton assembly and interspecies interaction indicating increasing coastal eutrophication[J]. Chemosphere, 2017, 177(6): 317-325.
[21] JOHNSON W C, LUO X L. Cool-season weed control using ammonium nonanoate and cultivation in organic Vidalia® sweet onion production[J]. Weed Technology, 2018, 32(1): 90-94. doi: 10.1017/wet.2017.91
[22] ROMDHANE S, DEVERS-LAMRANI M, MARTIN-LAURENT F, et al. Evidence for photolytic and microbial degradation processes in the dissipation of leptospermone, a natural β-triketone herbicide[J]. Environmental Science and Pollution Research International, 2018, 25(30): 29848-29859. doi: 10.1007/s11356-017-9728-4
[23] BURLACOT A, DAO O, AUROY P, et al. Alternative photosynthesis pathways drive the algal CO2 -concentrating mechanism[J]. Nature, 2022, 605: 366-371.
[24] LIU Y, LI F, HUANG Q X et al. Allelopathic effects of gallic acid from Aegiceras corniculatum on Cyclotella caspia[J]. Journal of Environmental Sciences, 2013, 25(4): 776-784. doi: 10.1016/S1001-0742(12)60112-0
[25] YALÇIN S, KARAKAŞ Ö, OKUDAN E Ş, et al. HPLC detection and antioxidant capacity determination of brown, red and green algal pigments in seaweed extracts[J]. Journal of Chromatographic Science, 2021, 59(4): 325-337. doi: 10.1093/chromsci/bmaa107




 下载:
下载: