Effects of water and nitrogen, phosphorus and potassium nutrition stress of rice seedlings on resistance of brown planthopper
-
摘要:目的
探究水源和食物对褐飞虱死亡速率的影响,探究不同浓度养分处理下的水稻幼苗对褐飞虱的抗性和趋避性,为综合应用田间水肥管理防治褐飞虱提供理论依据。
方法以感虫水稻品系‘9311’和抗性品系‘BPHR96’为供试材料,观察不同的水源和食物处理 (取食‘9311’茎段,取食‘BPHR96’茎段,有水源的饥饿胁迫以及无水源的饥饿胁迫)对褐飞虱死亡率的影响。在玻璃温室内开展水培试验,设置不同浓度营养液培养水稻幼苗,测定幼苗分蘖数、株高、根长、地上部鲜质量和根鲜质量5个表型性状;并观察侵染后褐飞虱的存活数量、增质量率、蜜露排泄量以及寄主选择数量。
结果无食物的情况下,褐飞虱死亡率上升迅速;无水源饥饿胁迫处理的褐飞虱在接虫后48 h全部死亡;接虫216 h时,有水源饥饿胁迫处理的死亡率达到96.8%,取食‘BPHR96’的死亡率达到85.0%,而取食‘9311’的死亡率也始终维持较低水平(44.3%)。营养液水培试验发现,与对照和高浓度氮磷钾营养液处理相比,低浓度氮磷钾营养液虽然对水稻幼苗的生长有所抑制,但能显著降低褐飞虱的存活数量、增质量率、蜜露排泄量以及寄主选择数量,且抗性水稻品系的效应更为明显。相比于低浓度钾营养液处理,对照和高浓度钾营养液处理能显著促进水稻幼苗的生长,但未发现钾浓度对褐飞虱的取食响应有显著影响。
结论充足的水分是保证褐飞虱维持生命活动的首要因素,其次才是食物的适口性。低浓度氮磷钾处理能够降低褐飞虱对水稻的危害,高浓度氮磷钾处理则利于褐飞虱的侵害,水稻大田生产过程中可通过水肥管理对褐飞虱进行综合防治。
Abstract:ObjectiveTo provide theoretical basis for the comprehensive application of field water and fertilizer to control brown planthopper (BPH), we investigated the effect of water and food on the mortality rate of BPH, and rice seedlings treated with different nitrogen, phosphorus and potassium mass concentrations on the antixenosis and antibiosis of BPH.
MethodThe BPH mortality under water or food treatments (‘9311’ stem segments, ‘BPHR96’ stem segments, starvation stress with water or without water) was detected with susceptible rice line ‘9311’ and resistant line ‘BPHR96’. Rice seedlings were cultured with low/control/high nitrogen, phosphorus and potassium or low/control/high potassium concentrations nutrient solution in a greenhouse. Five seedling traits including tiller number, plant height, root length, aboveground fresh weight and root fresh weight and BPH survival number, BPH growth rate, honeydew excretion score and host selection number were detected.
ResultThe BPH mortality increased rapidly in the absence of food. All the BPH treated without food and water died at 48 h after infestation. The mortality was 96.8%, 85.0%, and 44.3% treated with water, ‘BPHR96’ or ‘9311’ stem segments, respectively at 216 h after infestation. Comparing with control or high concentration of nitrogen, phosphorus and potassium, low concentration restricted the growth of rice seedlings, but significantly reduced the survival number, weight gain, honeydew excretion and host selection number of BPH. The effect was more obvious for the resistant rice line. Furthermore, control and high concentration of potassium had no significant effect on the growth of BPH except for rice seedlings compared to low potassium.
ConclusionWater is the primary factor for BPH survival, followed by the palatability of food. Low concentration of nitrogen, phosphorus and potassium treatment can reduce BPH damage to rice seedlings, while high concentration of nitrogen, phosphorus and potassium is beneficial to the invasion of BPH. Therefore, water and fertilizer managements can be applied to the comprehensive control of BPH in the process of rice production.
-
球孢白僵菌Beauveria bassiana是目前研究较深入、应用广泛的一种昆虫病原真菌, 其致病性强、杀虫范围广, 在多种害虫的防治中取得了显著的经济、社会和生态效益[1]。我国曾大规模地应用球孢白僵菌防治马尾松毛虫Dendrolimus punctatus Walker, 并取得了巨大的成功[2-3]。球孢白僵菌也广泛应用于防治亚洲玉米螟Ostrinia furnacalis, 特别是我国东北地区利用白僵菌防治越冬代玉米螟成为玉米螟生物防治的重要方法[4-5]。
球孢白僵菌侵染寄主昆虫一般要经历分生孢子的附着、萌发与穿透表皮, 菌丝在血腔内生长、产生毒素、致死寄主、入侵所有器官继而穿出表皮, 产生新一代分生孢子、继续扩散流行等阶段。球孢白僵菌的致病机理不像化学农药那样依靠自身毒力杀死害虫, 而是通过吸收寄主体内水分和养分满足自身菌丝生长, 导致寄主体内生理代谢紊乱或代谢发生障碍而死亡。关于寄主昆虫对球孢白僵菌的免疫作用已有一些研究, 大腊螟Galleria mellonalla幼虫感染球孢白僵菌后在最佳条件和热激条件下产生不同的体液免疫能力[6]; 接种球孢白僵菌分生孢子对桑天牛Apriona germari幼虫血细胞数量有显著的影响[7]。对亚洲玉米螟幼虫注射不同剂量球孢白僵菌芽生孢子后, 其血细胞总数发生变化, 活体与离体血细胞均对芽生孢子产生包囊作用, 但是在活体条件下血细胞粘附在芽生孢子表面形成包囊, 而在离体条件下包囊形成的速度较慢, 其致密程度不如活体状态, 表明亚洲玉米螟对球孢白僵菌芽生孢子具有细胞防御能力[8]。膜翅目寄生蜂腰带长体茧蜂Macrocentrus cingulum是亚洲玉米螟的重要天敌, 腰带长体茧蜂的卵不会被亚洲玉米螟血细胞囊胞化, 因而可以在其体内完成发育, 这一现象说明寄主昆虫与寄生物具有复杂的免疫与抗免疫关系[9-10]。
亚洲玉米螟血细胞系SYSU-OfHe-C由中山大学胡建博士创建, 可连续继代培养[11]。本研究将考察球孢白僵菌对亚洲玉米螟血细胞SYSU-OfHe-C的毒性及其形态的影响, 进一步研究亚洲玉米螟幼虫与球孢白僵菌的免疫互作关系, 促进利用球孢白僵菌防治亚洲玉米螟生物防治技术的发展。
1. 材料与方法
1.1 材料
亚洲玉米螟幼虫血细胞系SYSU-OfHe-C由中山大学生命科学学院胡建博士馈赠。球孢白僵菌BbTS01菌株是华南农业大学天然农药与化学生物学教育部重点实验室从西藏日喀则市白朗县土壤中分离获得。
EX-CELL420培养基(美国Sigma公司); 胎牛血清(Gibco公司); MTT(南京凯基生物科技发展有限公司); CCK-8(日本同仁公司); 二甲基亚砜DMSO(美国Sigma公司); 吐温80(天津市富宇精细化工有限公司)。
酶标仪(iMark, 伯乐生命医学产品有限公司); 倒置显微镜(MF52型, 广州市明美光电技术有限公司); 96孔板(美国Corning Incorporated公司), 血球计数板(上海求精生化试剂仪器有限公司)。
1.2 方法
亚洲玉米螟幼虫血细胞系SYSU-OfHe-C采用EX-CELL420培养基添加φ为10%的胎牛血清, 27 ℃恒温培养, 每隔3~4 d传代1次, 取对数期细胞用于试验。球孢白僵菌BbTS01菌株取斜面菌种接种于PDA平板上培养约2周, 收集分生孢子。取分生孢子100 mg, 用2 g·L-1的吐温水1 mL配成悬浮液, 采用血球计数板计数, 调整浓度为107 mL-1备用。
1.2.1 球孢白僵菌对血细胞系SYSU-OfHe-C细胞的毒力测定
1) MTT法:96孔板每孔加入90 μL受试细胞悬浮液, 静置培养24 h, 待细胞浓度为1×105 mL-1时, 分别滴加10 μL球孢白僵菌分生孢子悬浮液, 使球孢白僵菌分生孢子终浓度分别达到3.5×106、3.5×105、3.5×104、3.5×103 mL-1, 以2 g·L-1吐温水为对照, 以不加细胞的完全培养基为本底, 每个处理重复4次。在27 ℃恒温培养箱中培养24 h后, 每孔加入50 μL的1×MTT, 27 ℃培养4 h, 吸出上清液(悬浮细胞用此法时经1 000 r·min-1离心后去除上清液), 每孔加入150 mL DMSO使甲臜溶解, 摇匀; 酶标仪测定波长处检测每孔的D490 nm。2) CCK-8法:细胞培养与处理方法同上述MTT法, 接种球孢白僵菌分生孢子并培养24 h后, 向每孔加入10 μL CCK-8溶液, 注意不形成气泡, 将培养板在培养箱内孵育1~4 h, 酶标仪测定D450 nm。
1.2.2 球孢白僵菌对血细胞系SYSU-OfHe-C细胞形态的影响
96孔板每孔加入90 μL受试细胞悬浮液, 静置24 h, 接种球孢白僵菌分生孢子悬浮液使其终浓度为3.5×104 mL-1, 倒置显微镜下监测球孢白僵菌与血细胞的生长情况, 每隔30 min拍照记录。取上述接种球孢白僵菌后培养24 h的亚洲玉米螟血细胞, 在光学显微镜与扫描电子显微镜下观察其形态变化, 并拍照记录。
1.3 数据处理
试验结果采用SPSS软件分析细胞死亡率, 改良寇氏法[12]计算IC50值。

式中, Xm为处理最大浓度的对数值; i为各浓度倍比浓度的对数值; ΣP为各组死亡率之和; 0.5为经验常数。
2. 结果与分析
2.1 球孢白僵菌对血细胞系SYSU-OfHe-C细胞的毒力测定
球孢白僵菌对SYSU-OfHe-C细胞的毒力测定结果见图 1, 不同浓度的球孢白僵菌分生孢子悬浮液处理24 h后, SYSU-OfHe-C细胞的死亡率不同, 随着球孢白僵菌分生孢子悬浮液浓度的增大, SYSU-OfHe-C细胞的死亡率增加, 总体上看, CCK-8法与MTT法的结果相差不大, 但前者测得的SYSU-OfHe-C细胞死亡率更高一点, 当球孢白僵菌分生孢子悬浮液浓度为3.5×106 mL-1, CCK-8法测得的SYSU-OfHe-C细胞死亡率达77.3%, MTT法为66.4%;球孢白僵菌分生孢子悬浮液浓度为3.5×103 mL-1, CCK-8法与MTT法的死亡率分别为15.2%和15.6%。CCK-8法与MTT法测得球孢白僵菌对SYSU-OfHe-C细胞的毒力回归方程见表 1, 从表 1可知MTT法测得球孢白僵菌分生孢子对SYSU-OfHe-C细胞的IC50(2.8×105 mL-1)稍高于CCK-8法的IC50(1.4×105 mL-1)。
表 1 球孢白僵菌对SYSU-OfHe-C细胞的毒力回归方程和IC50值Table 1. The toxicity regression equation and IC50 value of Beauveria bassiana against SYSU-OfHe-C cells
2.2 球孢白僵菌对血细胞系SYSU-OfHe-C细胞形态的影响
在光学显微镜下观察发现, 在接种球孢白僵菌分生孢子后, 大约10 h分生孢子萌发长出菌丝, 此后菌丝不断伸长, 亚洲玉米螟血细胞开始移动、数量变少且形态改变, 至24 h左右, 球孢白僵菌菌丝长满整个视野, 未见囊胞化与吞噬作用(图 2)。
接种球孢白僵菌分生孢子24 h后, SYSU-OfHe-C细胞部分从近似圆形变长或者变为不规则形状, 似乎还原成浆血细胞和类绛色细胞的原始形状, 但未见吞噬与囊胞化等细胞免疫现象发生。另外, 也发现少数SYSU-OfHe-C细胞聚集、破碎、细胞减少, 以及出现空泡和瘤状突起等现象(图 3)。在扫描电镜下还观察到球孢白僵菌菌丝穿透SYSU-OfHe-C细胞的现象(图 4)。
3. 讨论与结论
本研究运用MTT和CCK-8法测定了球孢白僵菌对SYSU-OfHe-C细胞的毒力, 结果有一定差异, 可能原因是:使用MTT法检测时, 需要使用裂解液溶解甲臜晶体沉淀, 可能遇到颗粒不完全溶解、吸取上清的操作中带走部分细胞等问题, 导致MTT法的结果容易出现细胞死亡率比实际情况偏低的情况; 而CCK-8是一种综合指标较好的细胞毒性检测试剂, 对细胞的毒性相当低, 其检测原理和检测条件与MTT法略有差异。CCK-8法产生的甲臜是水溶性的, 可以省去后续的溶解步骤, 减少一定的误差, 使试验结果更加稳定, 尽管当有还原物质存在时会影响CCK-8的测定, 但CCK-8法一般比MTT法更加灵敏、稳定, 而且重复性较好。
昆虫细胞免疫反应是由血细胞介导的, 主要依赖血细胞对外来异物的吞噬、集结和包囊[13]。包囊反应在昆虫细胞免疫反应中占有很重要的位置, 对昆虫细胞免疫反应的研究必定要进行囊胞化分析。本试验未发现亚洲玉米螟细胞系SYSU-OfHe-C对球孢白僵菌的囊胞化与吞噬作用等细胞免疫现象, 可能原因之一是SYSU-OfHe-C本身特性决定的, 其缺乏血浆的某些成份, 影响了其囊胞化效率[11]; 也与球孢白僵菌本身的特性有关, 球孢白僵菌是一种通过营养竞争策略使寄主昆虫生病的虫生真菌, 通过增加入侵量和快速分裂或生长来逃避寄主昆虫的免疫防御[14]; 也可能与血细胞的密度有关[15], 自然情况下, 亚洲玉米螟体内血细胞密度约为1.0×107~4.0×107 mL-1[9], 本研究采用细胞密度为1.0×105 mL-1, 低于亚洲玉米螟体内血细胞密度, 有可能造成SYSU-OfHe-C细胞囊胞化作用降低。
球孢白僵菌等微生物制剂的广泛应用是农业发展的重要方向, 亚洲玉米螟是我国重要的农业害虫, 生物因子在控制亚洲玉米螟种群数量方面起着十分重要的作用[16]。通过研究球孢白僵菌对亚洲玉米螟血细胞系SYSU-OfHe-C的毒力作用和对其细胞形态及生长的影响, 为进一步深入研究亚洲玉米螟幼虫与球孢白僵菌的免疫互作奠定基础, 有利于促进球孢白僵菌对亚洲玉米螟的生物防治。
-
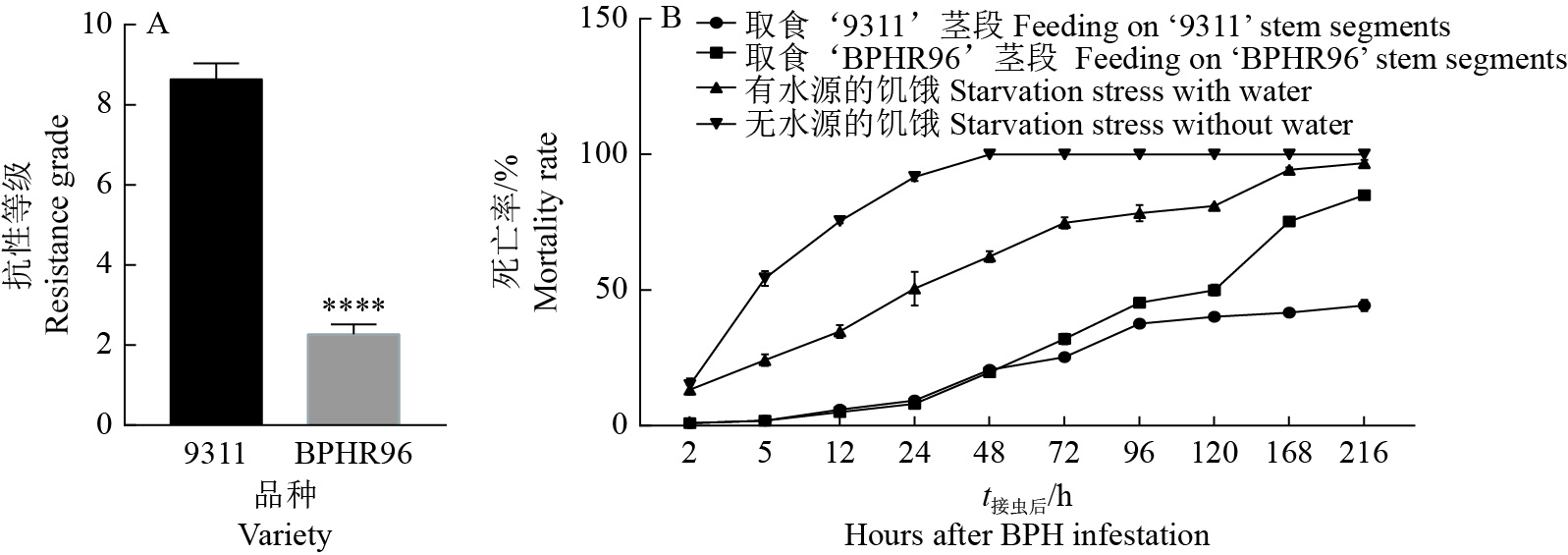
图 1 水稻品系抗褐飞虱评级(A)和不同水源和食物处理下褐飞虱的死亡率(B)
“****”表示‘BPHR96’与‘9311’的褐飞虱抗性等级差异显著(P < 0.0001,t检验)
Figure 1. Resistance grade of rice lines to brown planthopper (A) and mortality rate of brown planthopper under different water and food treatments (B)
“****” indicates significant difference in resistance grade between ‘BPHR96’ and ‘9311’ (P < 0.0001, t test)
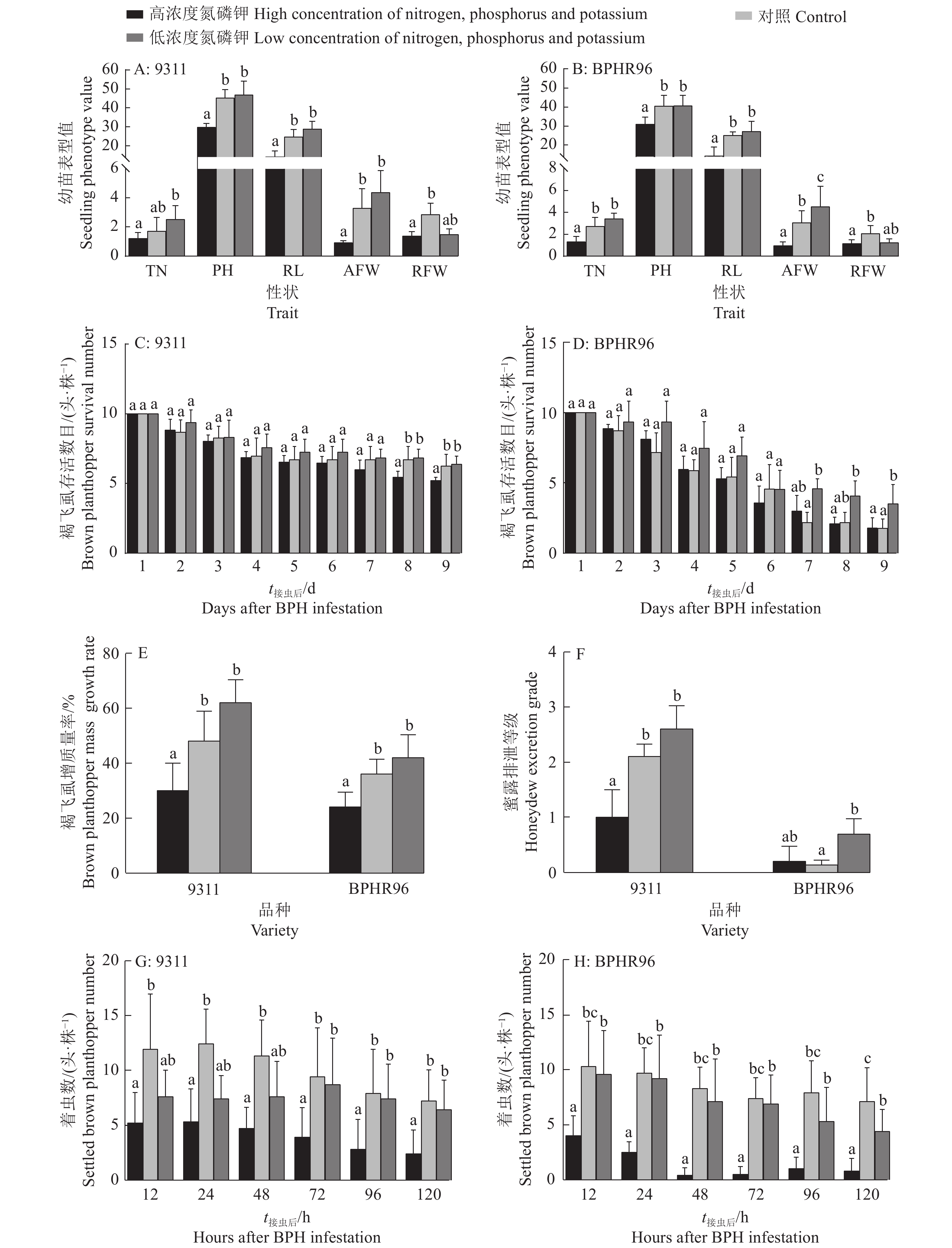
图 2 不同氮磷钾质量浓度对水稻品系‘9311’和‘BPHR96’苗期生长与褐飞虱取食的影响
各小图中同一指标图柱上不同小写字母表示处理间差异显著(P < 0.05,DMRT法);TN:分蘖数;PH:株高(cm);RL:根长(cm);AFW:地上部鲜质量(g);RFW:根鲜质量(g)
Figure 2. Effects of different nitrogen, phosphorus and potassium mass concentration on seedling growth and brown planthopper feeding of rice lines ‘9311’ and ‘BPHR96’
Different lowercase letters on the same indicator bar indicate significant difference among treatments (P < 0.05, DMRT method); TN: Tiller number; PH: Plant height (cm); RL: Root length (cm); AFW: Aboveground fresh weight (g); RFW: Root fresh weight (g)
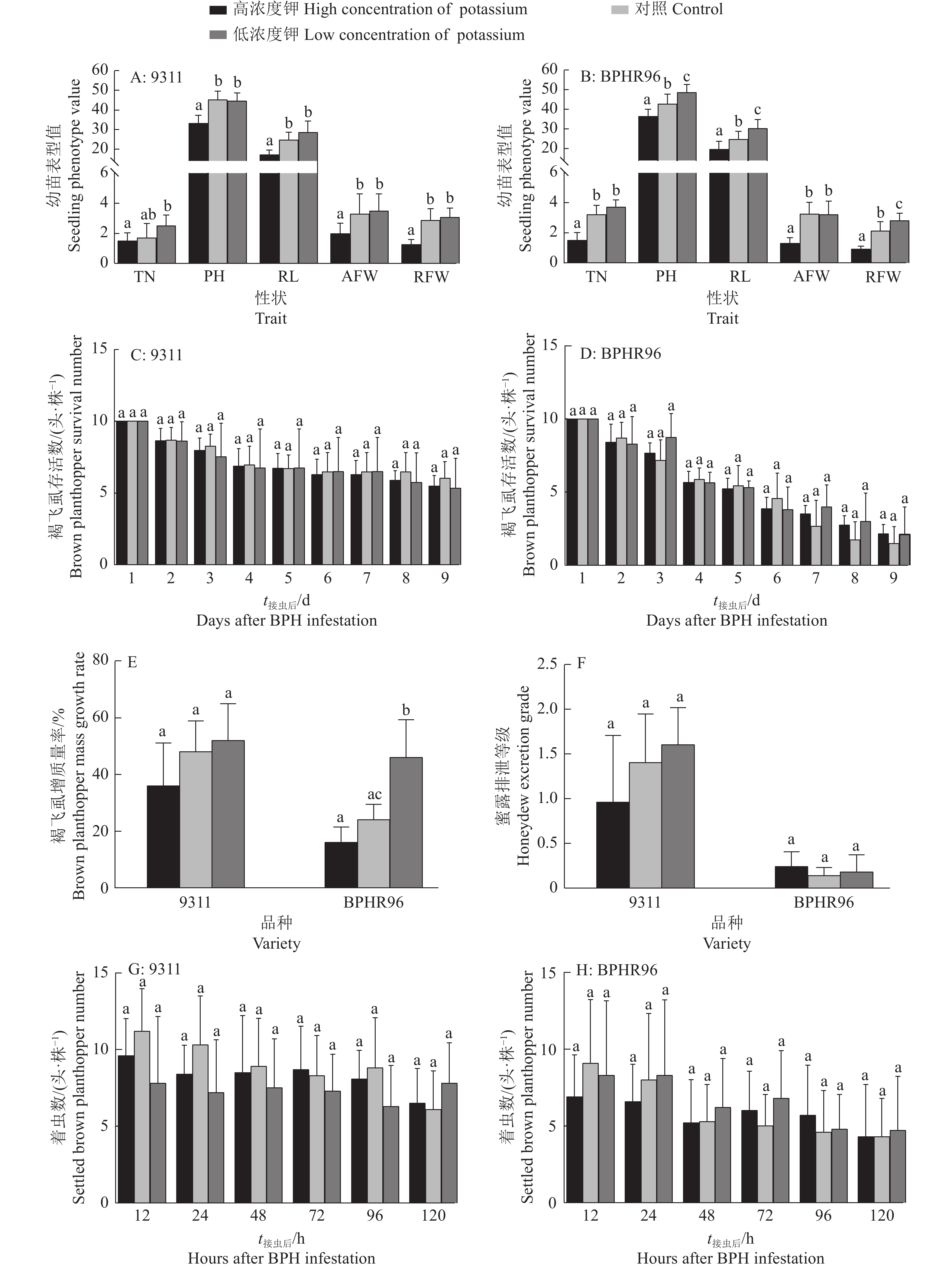
图 3 不同钾质量浓度对水稻品系‘9311’和‘BPHR96’苗期生长与褐飞虱取食的影响
各小图中同一指标图柱上不同小写字母表示处理间差异显著(P < 0.05,DMRT法);TN:分蘖数;PH:株高(cm);RL:根长(cm);AFW:地上部鲜质量(g);RFW:根鲜质量(g)
Figure 3. Effects of different mass concentration potassium on seedling growth and brown planthopper feeding of rice lines ‘9311’ and ‘BPHR96’
Different lowercase letters on the same indicator bar indicate significant difference among treatments (P < 0.05, DMRT method); TN: Tiller number; PH: Plant height (cm); RL: Root length (cm); AFW: Aboveground fresh weight (g); RFW: Root fresh weight (g)
-
[1] HUANG S, WANG P T, YAMAJI N, et al. Plant nutrition for human nutrition: Hints from rice research and future perspectives[J]. Molecular Plant, 2020, 13(6): 825-835. doi: 10.1016/j.molp.2020.05.007
[2] TRIPATHI R, TEWARI R, SINGH K P, et al. Plant mineral nutrition and disease resistance: A significant linkage for sustainable crop protection[J]. Frontiers in Plant Science, 2022, 13: 883970. doi: 10.3389/fpls.2022.883970.
[3] JEEVANANDHAM N, RAMAN R, RAMAIAH D, et al. Rice: Nilaparvata lugens Stal interaction: Current status and future prospects of brown planthopper management[J]. Journal of Plant Diseases and Protection, 2023, 130(1): 125-141. doi: 10.1007/s41348-022-00672-x
[4] HORGAN F G, DE FREITAS T F S, CRISOL- MARTÍNEZ E, et al. Nitrogenous fertilizer reduces resistance but enhances tolerance to the brown planthopper in fast-growing, moderately resistant rice[J]. Insects, 2021, 12(11): 989. doi: 10.3390/insects12110989.
[5] 刘井兰, 吴进才. 褐飞虱侵害对不同抗性水平水稻根部吸收氮、磷、钾的影响[J]. 昆虫学报, 2010, 53(4): 411-419. [6] 刘井兰, 于建飞, 吴进才, 等. 褐飞虱侵害后不同水稻品种根及地上部氮、磷、钾含量的变化[J]. 昆虫学报, 2007, 50(10): 1034-1041. [7] RASHID M M, JAHAN M, ISLAM K S. Impact of nitrogen, phosphorus and potassium on brown planthopper and tolerance of its host rice plants[J]. Rice Science, 2016, 23(3): 119-131. doi: 10.1016/j.rsci.2016.04.001
[8] GUPTA R, LEIBMAN-MARKUS M, ANAND G, et al. Nutrient elements promote disease resistance in tomato by differentially activating immune pathways[J]. Phytopathology, 2022, 112(11): 2360-2371. doi: 10.1094/PHYTO-02-22-0052-R
[9] BALLINI E, NGUYEN T T, MOREL J B. Diversity and genetics of nitrogen-induced susceptibility to the blast fungus in rice and wheat[J]. Rice, 2013, 6(1): 32. doi: 10.1186/1939-8433-6-32.
[10] 张晓燕. 施钾对苜蓿营养、次生代谢物质及抗蓟马的影响[D]. 兰州: 甘肃农业大学, 2017. [11] WU X Y, YU Y G, BAERSON S R, et al. Interactions between nitrogen and silicon in rice and their effects on resistance toward the brown planthopper Nilaparvata lugens[J]. Frontiers in Plant Science, 2017, 8: 28. doi: 10.3389/fpls.2017.00028.
[12] HE W Q, YANG M, LI Z H, et al. High levels of silicon provided as a nutrient in hydroponic culture enhances rice plant resistance to brown planthopper[J]. Crop Protection, 2015, 67: 20-25. doi: 10.1016/j.cropro.2014.09.013
[13] YANG M, HE W Q, LI Y, et al. Effects of low levels of nitrogen or phosphorus provided in hydroponic culture on brown planthopper feeding and survival[J]. International Journal of Pest Management, 2021, 67(2): 89-98. doi: 10.1080/09670874.2019.1682210
[14] LIN Y B, LIN X H, DING C H, et al. Priming of rice defense against a sap-sucking insect pest brown planthopper by silicon[J]. Journal of Pest Science, 2022, 95(3): 1371-1385. doi: 10.1007/s10340-021-01462-4
[15] 陈英之, 韦燕萍, 李孝琼, 等. 稻褐飞虱新抗源的鉴定和利用[J]. 西南农业学报, 2009, 22(6): 1581-1588. [16] QIU Y F, GUO J P, JING S L, et al. High-resolution mapping of the brown planthopper resistance gene Bph6 in rice and characterizing its resistance in the 9311 and Nipponbare near isogenic backgrounds[J]. Theoretical and Applied Genetics, 2010, 121(8): 1601-1611. doi: 10.1007/s00122-010-1413-7
[17] 邓钊, 石少阶, 王卉颖, 等. 籼稻资源WD15515中抗褐飞虱QTL的定位研究[J]. 作物学报, 2016, 42(3): 353-360. [18] BAQUI M A, KERSHAW W J S. Effect of plant water stress on honeydew production, weight gain and oviposition of brown planthopper Nilaparvata lugens on rice cultivars[J]. Entomologia Experimentalis et Applicata, 1993, 67(1): 25-30. doi: 10.1111/j.1570-7458.1993.tb01647.x
[19] 于莹, 徐红星, 郑许松, 等. 在高温下干旱胁迫对褐飞虱生态适应性的影响[J]. 植物保护学报, 2013, 40(3): 193-199. [20] 谭椰, 徐文彦, 周文武, 等. 水分胁迫下水稻对褐飞虱转录组的影响[J]. 植物保护学报, 2017, 44(6): 973-981. [21] 李超, 刘洋, 陈恺林, 等. 灌溉方式对优质晚稻褐飞虱及其主要天敌种群动态的影响[J]. 中国生态农业学报, 2016, 24(10): 1391-1400. [22] 郑世燕, 丁伟, 杜根平, 等. 增施矿质营养对烟草青枯病的控病效果及其作用机理[J]. 中国农业科学, 2014, 47(6): 1099-1110. [23] NAJIHAH N I, HANAFI M M, IDRIS A S, et al. Silicon treatment in oil palms confers resistance to basal stem rot disease caused by Ganoderma boninense[J]. Crop Protection, 2015, 67: 151-159. doi: 10.1016/j.cropro.2014.10.004
[24] 郑许松, 陈桂华, 徐红星, 等. 温度和氮肥对褐飞虱存活、生长发育和繁殖的交互作用[J]. 应用生态学报, 2009, 20(5): 1171-1175. [25] REUVENI R, DOR G, RAVIV M, et al. Systemic resistance against Sphaerotheca fuliginea in cucumber plants exposed to phosphate in hydroponics system, and its control by foliar spray of mono-potassium phosphate[J]. Crop Protection, 2000, 19(5): 355-361. doi: 10.1016/S0261-2194(00)00029-6
[26] CAMPOS-SORIANO L, BUNDÓ M, BACH-PAGES M, et al. Phosphate excess increases susceptibility to pathogen infection in rice[J]. Molecular Plant Pathology, 2020, 21(4): 555-570. doi: 10.1111/mpp.12916
[27] 左丽娟, 赵正雄, 杨焕文, 等. 增加施钾量对红花大金元烤烟部分生理生化参数及“两黑病”发生的影响[J]. 作物学报, 2010, 36(5): 856-862. [28] 李刘杰, 汪强, 韩燕来, 等. 钾水平对小麦酚类物质、木质素代谢和接种蚜虫群体动态的影响[J]. 中国农学通报, 2009, 25(17): 143-148. [29] MIYASAKA S C, HANSEN J D, MCDONALD T G, et al. Effects of nitrogen and potassium in kikuyu grass on feeding by yellow sugarcane aphid[J]. Crop Protection, 2007, 26(4): 511-517. doi: 10.1016/j.cropro.2006.04.023




 下载:
下载: