Establishment of IMSA-LAMP detection method for Ralstonia solanacearu
-
摘要:目的
桑树青枯病是由茄科雷尔氏菌Ralstonia solanacearum引起的一种危害严重的细菌性病害,建立一种快速、灵敏的茄科雷尔氏菌检测方法,对桑树青枯病的有效控制有重要意义。
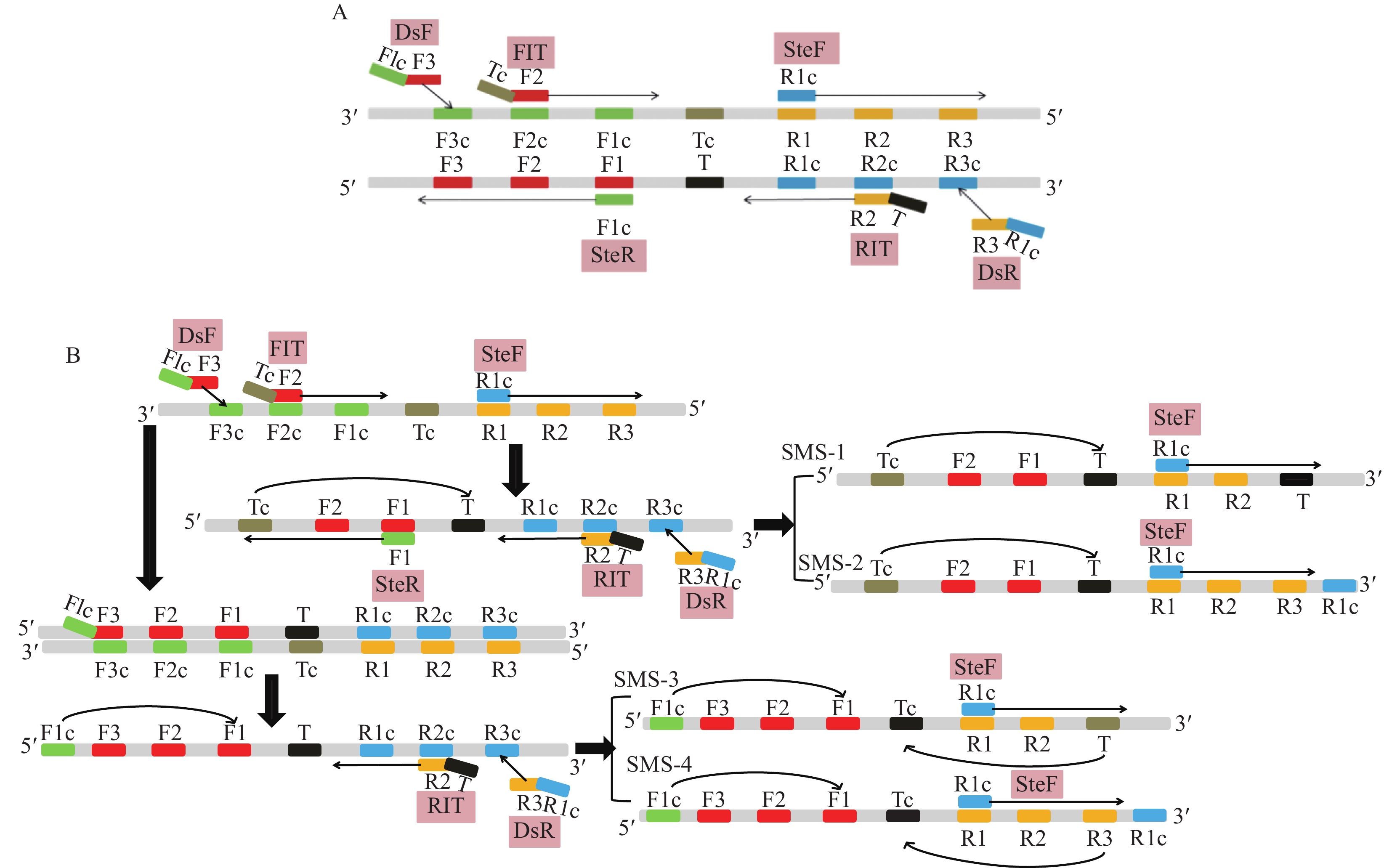
方法本研究以茄科雷尔氏菌果胶裂解酶基因(Pectate lyase gene)为靶标,基于等温多自配引发扩增技术(Isothermal multiple self-matching-initiated amplification,IMSA)的引物设计原理,结合环介导等温扩增技术(Loop-mediated isothermal amplification,LAMP)的反应体系,建立一种快速有效检测茄科雷尔氏菌的IMSA-LAMP法,并对该方法的最佳反应参数进行了筛选。
结果基于果胶裂解酶基因建立的IMSA-LAMP检测方法在64.5 ℃条件下,45 min内可完成对阳性样品的特异检测,对茄科雷尔氏菌的模板DNA检测灵敏度达200 fg/µL (对应菌为1×102 CFU/mL);对生产上收集的疑似桑树青枯病病样的检出率为87.5%。
结论IMSA-LAMP检测方法具有良好的实用性,可为桑树青枯病的快速检测、诊断与防疫提供新的技术支持。
Abstract:ObjectiveMulberry bacterial wilt is a seriously harmful bacterial disease caused by Ralstonia solanacearum. Therefore, it is of great significance to establish a rapid and sensitive detection method for R. solanacearum to effectively control mulberry bacterial wilt.
MethodPectate lyase gene of R. solanacearum was used as the target. Based on the primer design principle of isothermal multiple self-matching-initiated amplification (IMSA), combining the loop-mediated isothermal amplification (LAMP) reaction system, a rapid and effective IMSA-LAMP method for detection ofR. solanacearum was established. The optimal reaction parameters of this method were screened.
ResultThe IMSA-LAMP method based on pectate lyase gene could complete the specific detection of positive samples within 45 min at 64.5 ℃, and the detection sensitivity of R. solanacearum template DNA was 200 fg/μL (the corresponding bacteria detection sensitivity was 1 × 102 CFU/mL); The detection rate of suspected mulberry bacterial wilt samples collected in production was 87.5%.
ConclusionThis method has good practicability and can provide new technical support for the rapid detection, diagnosis and epidemic prevention of mulberry bacterial wilt.
-
Keywords:
- Mulberry bacterial wilt /
- IMSA-LAMP /
- Ralstonia solanacearum /
- Pectate lyase gene
-
单倍体诱导技术是培育玉米新品种最快速、经济的手段.Stock6[1]是玉米中发现的第1个孤雌生殖诱导系,利用其所选育的诱导系有WS14[2]、MHI[3]等.但Stock6在诱导率、繁殖性能等方面存在严重缺陷,吉林农业大学玉米育种课题组对Stock6进行了遗传改良,成功地获得了诱导率10%以上、遗传标记明显、花粉量大、持粉时间长、抗病性好的新型诱导系JS6.本研究以诱导系JS6的姊妹系JS6-11 ~ JS6-15作父本,以高抗丝黑穗病自交系K88和高感丝黑穗病自交系G115的杂交F1代作为母本材料,杂交诱导产生单倍体,探讨不同诱导因素下单倍体诱导率的变化特点,对有效利用单倍体诱导系及单倍体诱导技术,提高育种效率并选育自有的单倍体诱导系,快速培育玉米自交系并用其选育玉米新品种具有重要意义.
可供加倍的单倍体材料有限,玉米单倍体加倍技术尚不成熟.研究报道,许多玉米材料单倍体自然加倍率低于5%,有些材料根本不发生自然加倍[4-5].因此,要获得大量玉米Double haploid(DH)系并从中选育出优良自交系供生产上利用,必须借助单倍体人工染色体加倍.玉米单倍体的化学加倍方法有很多[5-9],其中秋水仙素应用最为广泛.本研究通过设计4种秋水仙素加倍方式,进一步探讨秋水仙素加倍技术,以期为生产上玉米单倍体的加倍提供理论参考.
1. 材料与方法
1.1 杂交诱导试验
以高抗丝黑穗病自交系K88和高感丝黑穗病自交系G115的杂交F1代作为母本,以吉林农业大学玉米育种课题组选育的5个诱导系JS6-11 ~ JS6-15作为父本,于2011年在吉林农业大学育种基地杂交诱导单倍体.试验设置花丝长短和授粉时期2个因素.花丝长短设2个处理:在长花丝(≥7 cm)和短花丝(≤4 cm)条件下用诱导系花粉授粉;授粉时期设2个处理:伏期(07-15—08-01)和伏后(08-15—09-01)授粉.用于研究的母本材料分别于2011年5月中旬和6月上旬播种.
于母本吐丝后进行授粉,收获后选择结实较好的果穗,在果穗上挑选无色胚芽、紫色粒顶、胚近三角形的准单倍体,所有准单倍体于2012年春种植于吉林农业大学长春玉米育种基地进行鉴定.其中单倍体植株田间表现为矮小、叶片和茎秆均呈绿色、多为不育.根据杂交当代子粒和单倍体子粒数,计算单倍体诱导率:

1.2 单倍体加倍试验
单倍体加倍药剂为西格玛-奥德里奇公司生产的秋水仙素原药、2%(φ)DMSO(二甲基亚砜)和5%(φ)甘油辅助剂.采取4种处理方法,每种方法分3个浓度梯度(0.2、0.4和0.6 mg·mL-1).1)浸根法:单倍体种子浸泡在清水中6 h后置于28 ℃培养箱中催根,待幼苗长到2 ~ 3片叶时,将其置入4 ℃冰箱中炼苗2 ~ 3 h,而后用自编的带有小孔且上面附有1层保湿滤纸的铁丝网将幼芽固定,并将幼根浸泡于不同浓度(0.2、0.4、0.6 mg·mL-1)的秋水仙素+ 2%(φ)DMSO + 5%(φ)甘油溶液中,溶液漫过幼根生长点,浸泡6 h后,再用流水清洗2 h,移栽至大田.2)浸芽法:采用毛巾卷法催芽,当幼芽长约2 cm时用刀片将幼芽顶端胚芽鞘切掉1 ~ 2 mm,使之露出1个小口(但不要伤害到嫩芽),将其在室温下密闭浸泡在不同浓度(0.2、0.4、0.6 mg·mL-1)的秋水仙素+ 2%(φ)DMSO + 5%(φ)甘油溶液中6 h,流水清洗2 h后将其种在育苗盘中,幼苗长到4 ~ 5片叶时移栽至大田.3)滴心叶法:选择长势一致的单倍体幼苗,待其生长到3 ~ 5叶时,分别抽取约1 mL的(0.2、0.4、0.6 mg·mL-1)秋水仙素+ 2%(φ)DMSO + 5%(φ)甘油溶液至单倍体植株的心叶处. 4)针刺生长点法:长势一致的单倍体幼苗田间长到6 ~ 7叶时,用微量移液器抽取5 μL的(0.2、0.4、0.6 mg·mL-1)秋水仙素+ 2%(φ)DMSO + 5%(φ)甘油溶液注射于幼苗茎秆的盾片节处的生长点.
加倍材料源于试验1.1中杂交诱导产生的单倍体,将准单倍体均分4等份(100粒)后根据不同的秋水仙素加倍处理后种植田间,去除非单倍体植株.田间观察成活率、散粉率、结实率和药害情况.以单倍体植株是否散粉和结实来判断玉米单倍体植株是否加倍成功.为防外来花粉授粉结实,试验选取单倍体自交后代结实较好的果穗于2012年冬和2013年春分别在三亚和长春种植观察,以进一步鉴别其加倍情况.



1.3 数据处理
数据采用Excel和DPS[10]软件进行处理及分析.
2. 结果与分析
2.1 不同因素对诱导率的影响
2.1.1 不同花丝长度的单倍体诱导率
从表 1中可以看出,花丝长度对单倍体诱导率有很大影响,花丝≥7 cm时的平均诱导率(17.0%)明显大于花丝长度≤4 cm时的平均诱导率(5.2%).其中在花丝长度≤4 cm时的诱导系中,诱导率最高的是JS6-14,诱导率为7.9%.花丝长度≥7 cm时诱导率最高的诱导系为JS6-13,诱导率为21.2%.诱导系长花丝处理单倍体诱导率高于短花丝处理,说明长花丝诱导效果比短花丝效果好.
表 1 不同花丝长度授粉单倍体诱导率Table 1. Haploid induced rates at different silk length pollination
2.1.2 花丝长度与诱导系对诱导率的影响
花丝长度和诱导系对诱导率的影响的方差分析见表 2.结果表明:不同诱导系诱导率存在显著差异,不同花丝长度诱导率存在极显著差异,说明诱导系和花丝长度对诱导率均有很大影响,且长花丝条件下授粉可以提高诱导率.
表 2 花丝长度与诱导系间的方差分析Table 2. Variance analysis between the silk length and inducer
2.1.3 不同授粉时期的单倍体诱导率
由表 3可知,授粉时期对单倍体诱导率亦有很大影响,伏后授粉时的平均诱导率(18.4%)明显大于伏期授粉时的平均诱导率(5.4%).其中在伏期授粉时,诱导率最高的是诱导系JS6-14(8.1%).伏后授粉时诱导率最高的诱导系为JS6-13(22.8%).诱导系伏后授粉时单倍体平均诱导率(18.4%)高于伏期授粉(5.4%),说明伏后授粉效果更好.
表 3 不同授粉时期单倍体诱导率Table 3. Haploid induced rates at different pollinating dates
2.1.4 授粉时期与诱导系对诱导率的影响
授粉时期和诱导系对诱导率的影响的方差分析见表 4.结果表明:诱导系、授粉时期诱导率均达到了极显著水平,说明不同授粉时期对诱导率有很大影响,且伏后授粉时可以提高单倍体诱导率.此外,相对于花丝长度,授粉时期对诱导率影响更大.
表 4 授粉时期与诱导系间的方差分析Table 4. Variance analysis between the pollinating dates and inducer
2.2 不同方法对单倍体加倍效果的影响
2.2.1 加倍方法对单倍体植株成活率的影响
从表 5可知,滴心叶法的适宜浓度为0.4 mg·mL-1,浸芽法的适宜浓度为0.2 mg·mL-1.针刺生长点法的适宜浓度为0.6 mg·mL-1.在秋水仙素各浓度梯度下浸根法处理时单倍体植株受害程度比其他3种方法严重,0.2、0.4、0.6 mg·mL-1存活率分别为39.3%、42.2%和25.6%.
表 5 不同方法、不同浓度秋水仙素处理单倍体的成活、散粉和结实情况Table 5. The survival, fertility and seed setting of haploid plants under different colchicines concentrations and methods
2.2.2 加倍方法对单倍体植株散粉和结实的影响
由表 5可知,4种加倍方法中,针刺生长点法的效果最好,散粉率均超过10%,在秋水仙素为0.6 mg·mL-1时散粉率达到45.9%;结实率也最高,为15.2%.滴心叶法在0.4 mg·mL-1下散粉率为28.9%,结实率为11.1%;浸根法的散粉率都低于10%,在秋水仙素为0.4和0.6 mg·mL-1下结实率都极低(1.1%);浸芽法虽在0.4 mg·mL-1下散粉率超过10%,但其结实率却很低(1.1%).综上可以看出,在散粉性和结实率方面,针刺生长点法和滴心叶法相对较好.
3. 讨论与结论
3.1 诱导条件对玉米单倍体诱导率的影响
在花丝长度≥7 cm和花丝长度≤4 cm授粉时进行杂交诱导,前者单倍体诱导率较高(21.2%);在伏期授粉(07-15—08-01)时的单倍体诱导率(8.1%)远低于伏后授粉(08-15—09-01)的单倍体诱导率(22.8%).其中花丝长度对玉米单倍体诱导率的影响可能原因是花粉中2个精细胞形成雄性生殖单位是保证2个精核同步转运的重要条件,较长的花丝增加了2个精核在花粉管中运输的不同步性[11].刘志增等[12]研究表明,精核间距在诱导单倍体过程中起重要作用,花丝长使得花粉粒萌发后花粉管到达胚囊距离延长,进而造成2个精核的间距加大,更容易诱导形成单倍体.授粉时期对单倍体诱导率的影响可能同气温有密切关系.授粉期早时温度相对较高,玉米花粉管生长速度快,新陈代谢非常旺盛,能量和物质的消耗都加快了,而供给的能量和物质不会相应地增加,相对于本身内含物就很少的玉米孤雌生殖诱导系花粉粒来说,这种状况会加速花粉管的衰老,不正常花粉的竞争力减弱,从而导致单倍体的产生减少.而授粉晚时,温度相对较低,新陈代谢相对较慢,玉米孤雌生殖诱导系的不正常花粉粒的2个精核在花粉管中有充足的时间分开运输,从而单受精产生玉米单倍体.
姜龙等[13]以玉米单倍体诱导系JS6-1为父本和8个不同母本基础组合在长春、长岭和三亚的研究结果表明,不同基因型诱导基础材料的单倍体诱导率为海南三亚冬繁明显高于长春和长岭,表明昼夜温差大有利于玉米单倍体的诱导.
花丝长短和授粉时期也可能影响了精卵结合的过程,随着花丝的增长,但极核和卵核接受精核的能力均减弱,极核与精核结合的能力相对较强,由此导致胚乳正常发育,而雌配子由于没有受精而发育为单倍体.低温对受精过程也可能有类似影响.从花丝不同时期接受花粉的能力来看,雌穗在吐丝后3 ~ 4 d内抽出的花丝活力较强[14],6 ~ 9 d后活力开始下降[15].考虑到本研究母本基因型较少,有关温度、花丝活力和母本基因型等因素对诱导性能的影响仍需进一步研究.
3.2 人工染色体加倍处理对玉米单倍体加倍的影响
Chase[16]曾提出用秋水仙素溶液注射玉米幼苗的盾片节进行加倍,Gayen等[17]曾采用浸种法,使单倍体加倍率达到了18%.魏俊杰等[18]在6叶期和拔节期用不同浓度的秋水仙素配以DMSO注射处理茎尖生长点,发现在6叶期,以0.5%(φ)秋水仙素配以2.0%(φ)的DMSO处理效果最好,加倍率高达32.3%.敬成俊等[19]研究表明秋水仙素加倍作用是通过与幼嫩组织正在分裂的细胞接触,引起纺锤丝缩减并且结构发生变化,细胞整齐地被阻止在分裂中期,因而使重组核具有加倍的染色体数.秋水仙素在植物组织中迅速扩散,通过维管系统在植物体内运转,实现使植株组织加倍达到长效的目的[9].
本研究秋水仙素处理结果表明:浸根法对植株伤害较严重,存活率低于50%;针刺生长点法(0.6 mg·mL-1)和滴心叶法(0.4 mg·mL-1)的散粉率较高(45.9%,28.9%),相应的结实率也较高(15.2%,11.1%),说明针刺生长点法处理效果最好,滴心叶法次之.其生理生化机制可能是:
1) 玉米根系的最重要功能是从土壤中吸收水分和营养物质,当用一定浓度的秋水仙素处理后,玉米根系的发育受到一定的阻碍,而且秋水仙素也破坏了玉米根系中的根毛和根尖幼嫩组织.移栽到大田后,幼苗吸收水分和营养物质困难,容易过早死亡.二倍体植株具有发达的根系,相对于单倍体根系具有较强的抵抗秋水仙素药害的作用,因此在田间发育良好[20].
2) 针刺生长点法是处理茎尖分生组织,相对于浸根法、浸芽法来说造成的损伤较大,其原因可能是针刺生长点法中秋水仙素注射于茎尖分生组织后并长期作用于茎尖分生组织,而且田间的高温加重了药害,植株的死亡率也很高,即使植株存活下来也表现为叶片发黄、萎缩,但由于秋水仙素长期有效地作用于茎尖分生组织,对植株的加倍效果也很明显,只要植株成活都有可能加倍成功[21].
3) 针刺生长点法和滴心叶法结实率不高的原因可能是多方面的,除了上述秋水仙素造成的药害外,还有加倍成功的植株雌雄花期不协调和生殖器官变态等原因,这样的植株也不会散粉和结实[9].
综上所述,在浸根法和浸芽法中,应该降低秋水仙素的浓度以减小药害,同时浸根法中应该尝试着处理侧根以使植株移栽到大田后能吸收水分和营养物质.针刺生长点法中处理后,应当多浇水,做好田间管理以增加植株存活率.
-
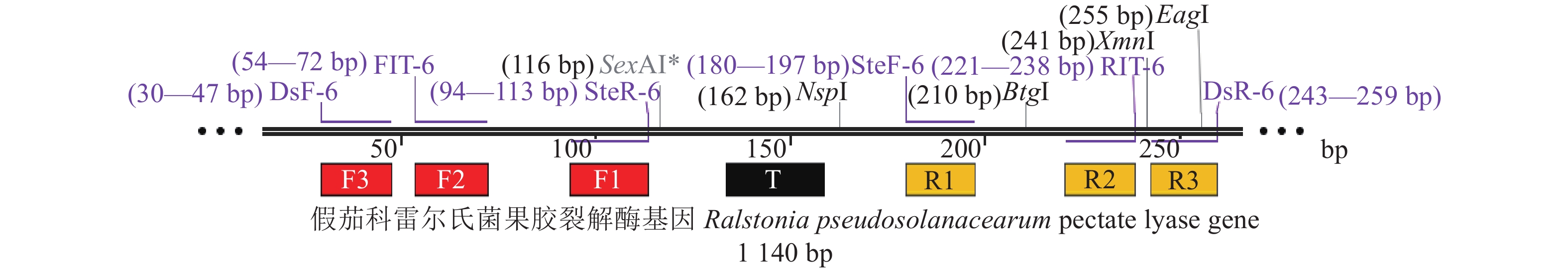
图 3 IMSA-LAMP引物组6的6条检测引物的位置及7个特异识别位点
F1:CAGCGCGCAGTACAACTGCT,F2:GAATCACGATGCGGGTTCC, F3:CCATTTCCAGACGCCCTC,T:TCAAAGCGAGCAAGCTGTTCGGGAA,R1:CGACAACGCCGGCCAGAA,R2:GTCATCATGGCGGCTCGA,R3:GTTCGGTGCAAACGGCC
Figure 3. Locations of six primers of primer group 6 and their seven specific recognition sites in IMSA-LAMP
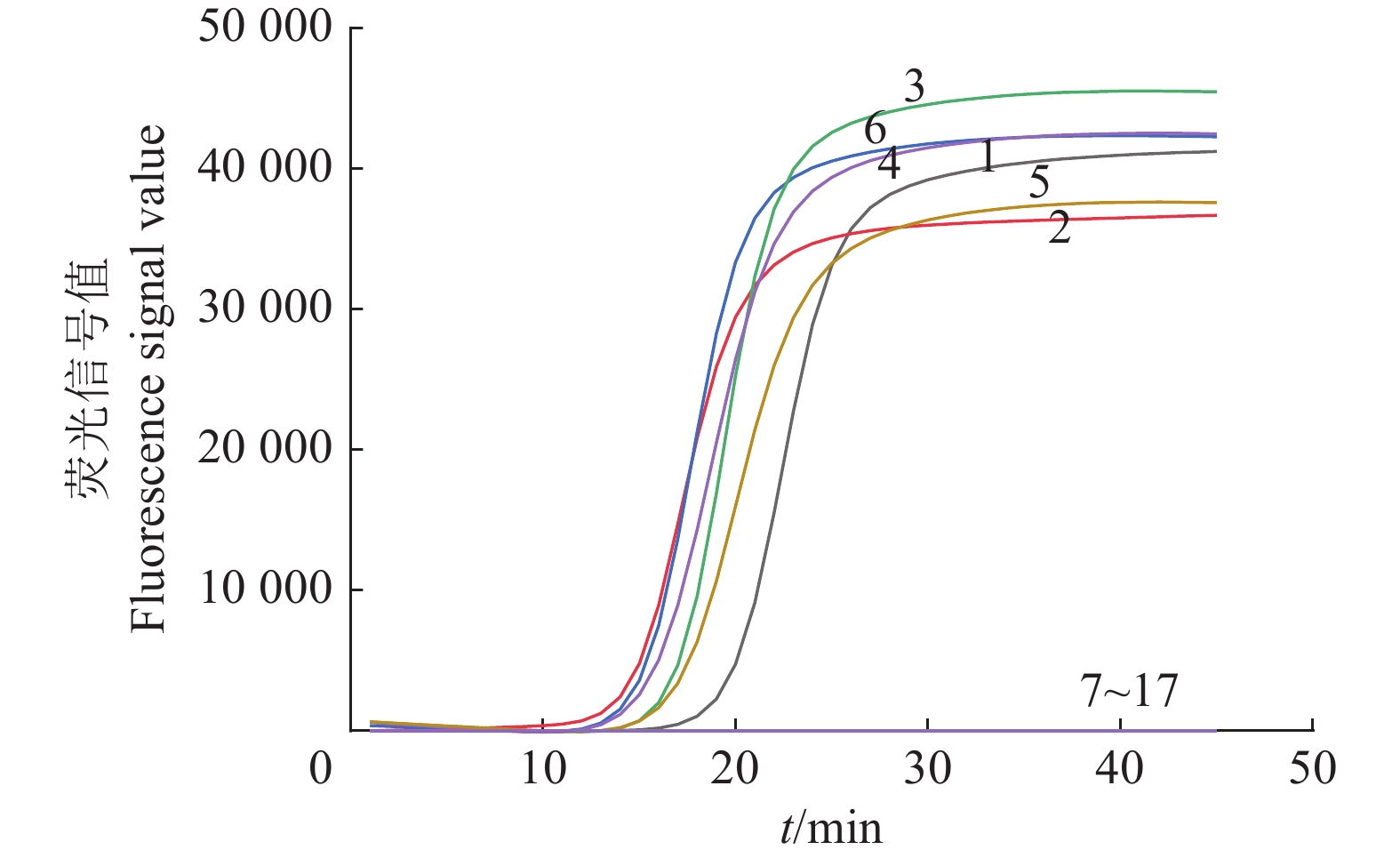
图 4 茄科雷尔氏菌IMSA-LAMP特异性检测结果
1~6:茄科雷尔氏菌(YZqk1、YLqk1、XZqk2、XCqk4、LZqk5、YDqk6);7:阴沟肠杆菌(XCYG-001);8:克雷伯氏菌(LCKL-001);9:菠萝泛菌(LCFJ-001);10:铜绿假单胞菌(YD-001);11:丁香假单胞菌(ZJDX-003);12:多黏类芽孢杆菌(YD-002);13:短小杆菌(YDDX-001);14:芽孢杆菌(YD-003);15:无菌水;16、17:健康桑树DNA
Figure 4. Specific detection results of IMSA-LAMP for Ralstonia solanacearum
1−6: Ralstonia solanacearum (YZqk1, YLqk1, XZqk2, XCqk4, LZqk5, YDqk6); 7: Enterobacter cloacae (XCYG-001); 8: Klebsiella sp. (LCKL-001); 9: Pantoea ananas (LCFJ-001); 10: Pseudomonas aeruginosa (YD-001); 11: Pseudomonas syringae (ZJDX-003); 12: Paenibacillus polymyxa (YD-002); 13: Bacillus pumilus (YDDX-001); 14: Bacillus sp. (YD-003); 15: Sterile water; 16−17: DNA of healthy mulberry
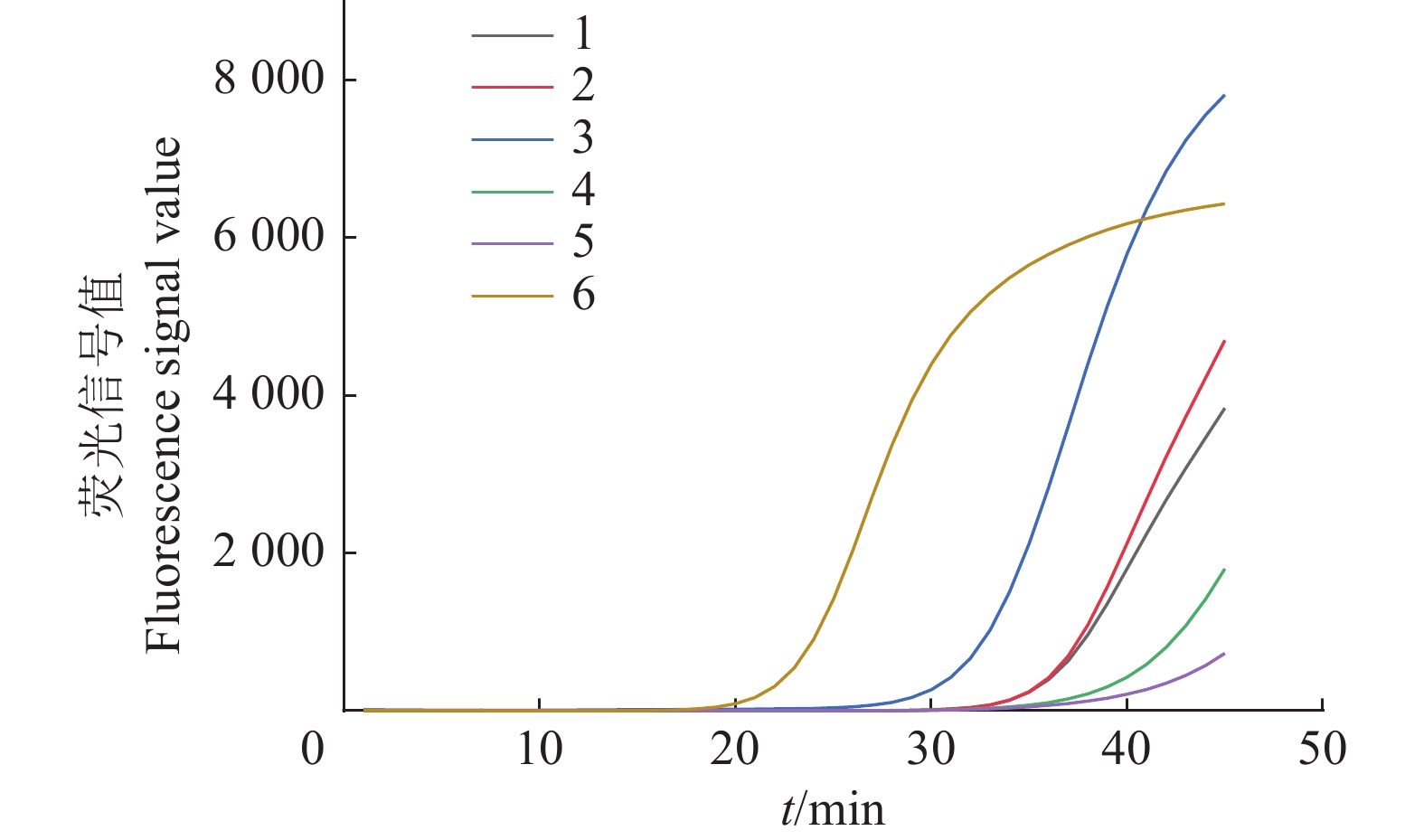
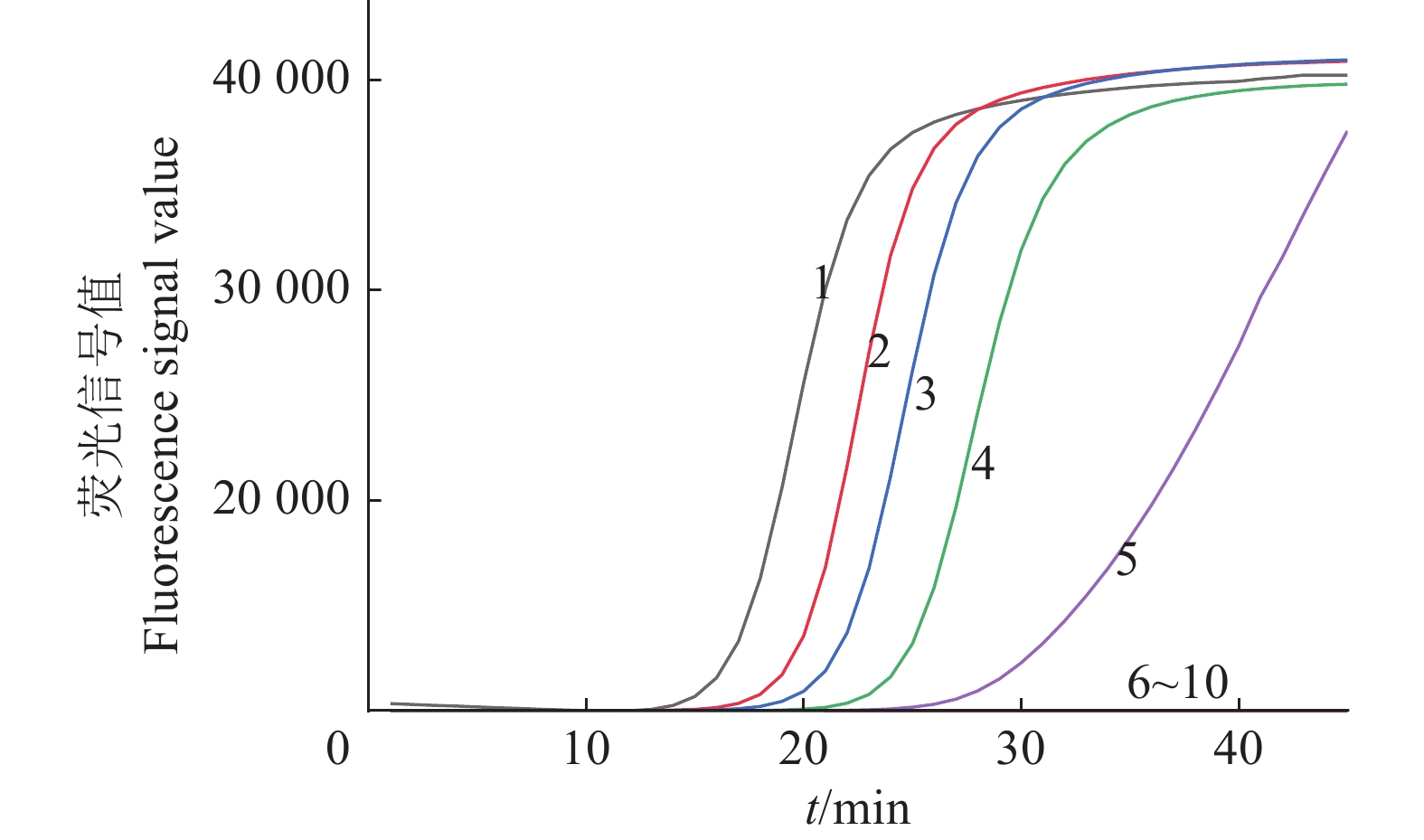
图 7 IMSA-LAMP对茄科雷尔氏菌灵敏度的检测结果
1:2 ng/μL (1×106 CFU/mL);2:200 pg/μL (1×105 CFU/mL);3:20 pg/μL (1×104 CFU/mL);4:2 pg/μL (1×103 CFU/mL);5:200 fg/μL (1×102 CFU/mL);6:20 fg/μL (1×10 CFU/mL);7:2 fg/μL (1×10−1 CFU/mL);8:200 ag/μL (1×10−2 CFU/mL);9:无菌水;10:健康桑树DNA
Figure 7. Sensitivity test results of IMSA-LAMP for Ralstonia solanacearum
1: 2 ng/μL (1×106 CFU/mL); 2: 200 pg/μL (1×105 CFU/mL); 3: 20 pg/μL (1×104 CFU/mL); 4: 2 pg/μL (1×103 CFU/mL); 5: 200 fg/μL (1×102 CFU/mL); 6: 20 fg/μL (1×10 CFU/mL); 7: 2 fg/μL (1×10−1 CFU/mL); 8: 200 ag/μL (1×10−2 CFU/mL); 9: Sterilized water; 10: DNA of healthy mulberry
图 8 PCR对茄科雷尔氏菌灵敏度检测结果
1:2 ng/μL (1×106 CFU/mL);2:200 pg/μL (1×105 CFU/mL);3:20 pg/μL (1×104 CFU/mL);4:2 pg/μL (1×103 CFU/mL);5:200 fg/μL (1×102 CFU/mL);6:20 fg/μL (1×10 CFU/mL);7:2 fg/μL (1×10−1 CFU/mL);8:200 ag/μL (1×10−2 CFU/mL);9:无菌水;10:健康桑树DNA
Figure 8. Sensitivity test results of PCR for Ralstonia solanacearum
1: 2 ng/μL (1×106 CFU/mL); 2: 200 pg/μL (1×105 CFU/mL); 3: 20 pg/μL (1×104 CFU/mL); 4: 2 pg/μL (1×103 CFU/mL); 5: 200 fg/μL (1×102 CFU/mL); 6: 20 fg/μL (1×10 CFU/mL); 7: 2 fg/μL (1×10−1 CFU/mL); 8: 200 ag/μL (1×10−2 CFU/mL); 9: Sterilized water; 10: DNA of healthy mulberry
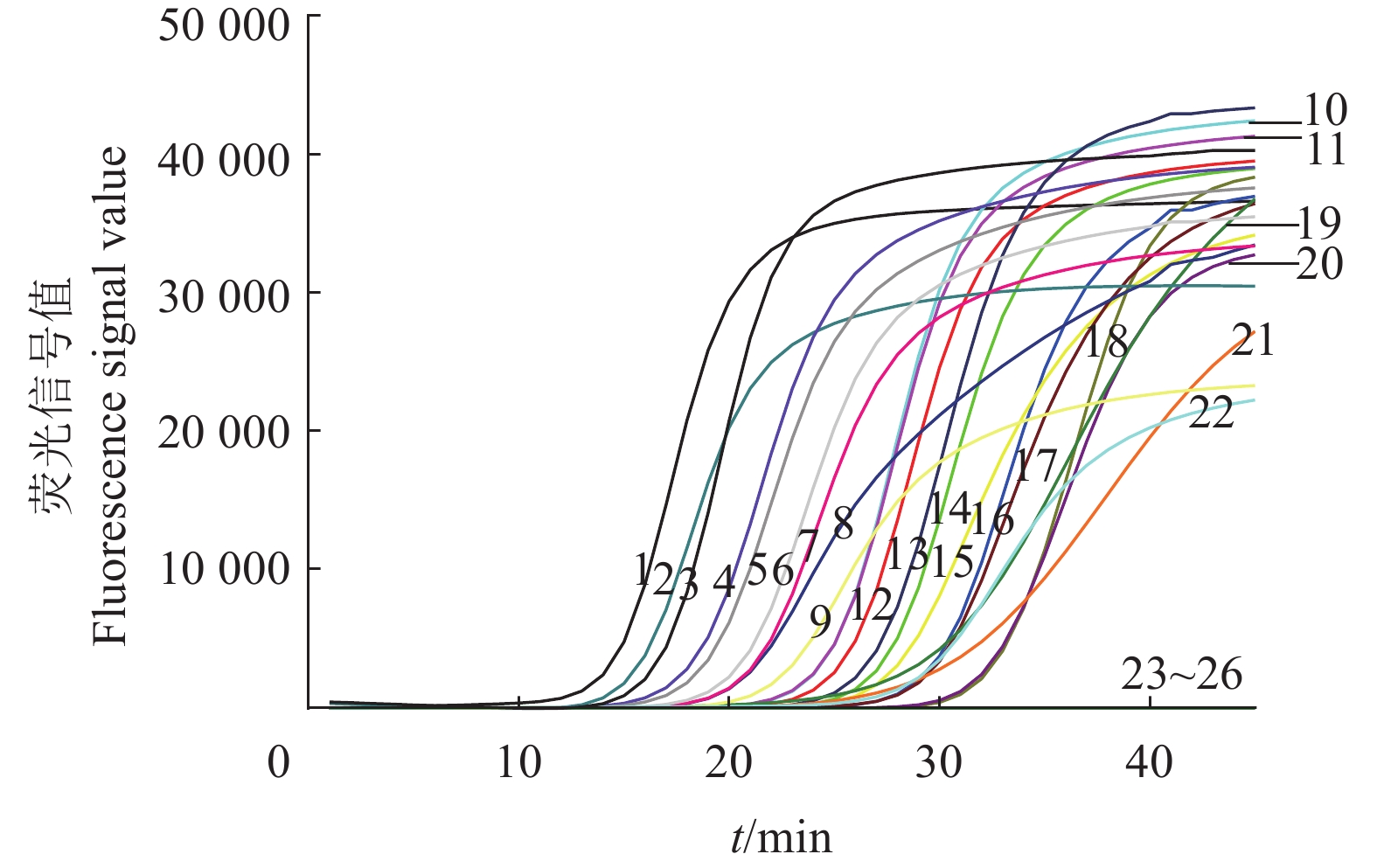
图 9 IMSA-LAMP对不同地区疑似桑树青枯病病样的检测结果
1:茄科雷尔氏菌YZqk1;2~5:广西来宾;6~9:广西宜州;10~12:广东英德;13~14:广东阳山;15~16:广东罗定;17~18:广东广州;19~21:广西都安;22~23:广西环江;24~25:广西忻城;26:健康桑树DNA
Figure 9. Detection results of suspected mulberry bacterial wilt samples from different districts by IMSA-LAMP
1: Ralstonia solanacearum YZqk1; 2–5: Laibin of Guangxi; 6–9: Yizhou of Guangxi; 10–12: Yingde of Guangdong; 13–14: Yangshan of Guangdong; 15–16: Luoding of Guangdong; 17–18: Guangzhou of Guangdong; 19–21: Du'an of Guangxi; 22–23: Huanjiang of Guangxi; 24–25: Xincheng of Guangxi; 26: Healthy mulberry DNA
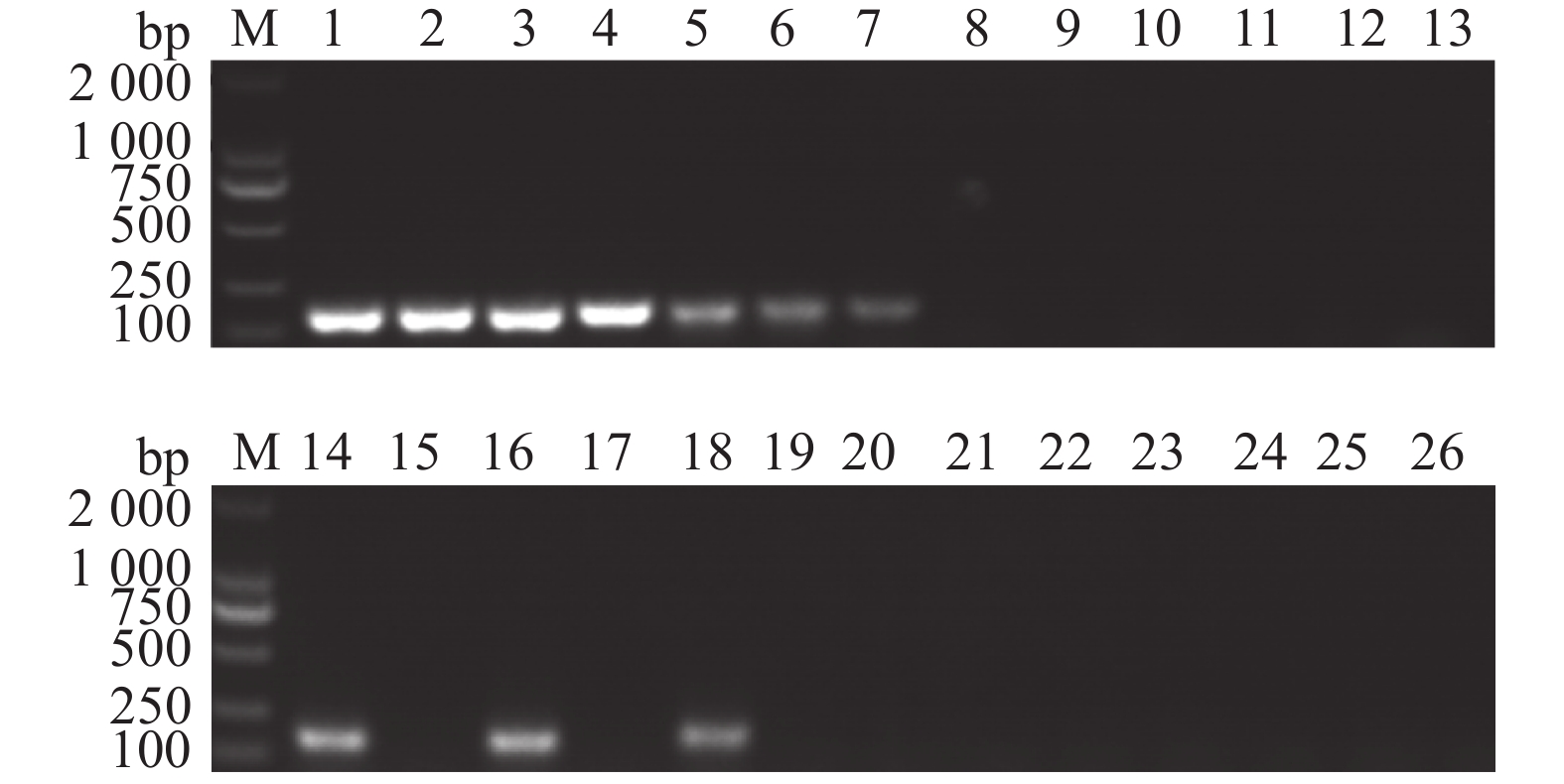
图 10 PCR对不同地区疑似桑树青枯病病样的检测结果
1:茄科雷尔氏菌YZqk1;2~5:广西来宾;6~9:广西宜州;10~12:广东英德;13~14:广东阳山;15~16:广东罗定;17~18:广东广州;19~21:广西都安;22~23:广西环江;24~25:广西忻城;26:健康桑树DNA
Figure 10. Detection results of suspected mulberry bacterial wilt samples from different districts by PCR
1: Ralstonia solanacearum YZqk1; 2–5: Laibin of Guangxi; 6–9: Yizhou of Guangxi; 10–12: Yingde of Guangdong; 13–14: Yangshan of Guangdong; 15–16: Luoding of Guangdong; 17–18: Guangzhou of Guangdong; 19–21: Du'an of Guangxi; 22–23: Huanjiang of Guangxi; 24–25: Xincheng of Guangxi; 26: Healthy mulberry DNA
表 1 桑树青枯病田间病样
Table 1 Field samples of mulberry bacterial wilt
地区 District 坐标 Coordinate 品种 Cultivar 数量 Quantity 广东阳山 Yangshan, Guangdong E112.641°,N24.465° 伦教40 Lunjiao 40 2 广东罗定 Luoding, Guangdong E111.570°,N22.768° 伦教40 Lunjiao 40 2 广东广州 Guangzhou, Guangdong E113.359°,N23.170° 伦教40 Lunjiao 40 2 广东英德 Yingde, Guangdong E113.454°,N24.179° 伦教40 Lunjiao 40 3 广西都安 Du’an, Guangxi E108.105°,N23.931° 粤桑11 Yuesang 11 3 广西来宾 Laibin, Guangxi E109.234°,N23.727° 粤桑11 Yuesang 11 4 广西环江 Huanjiang, Guangxi E108.258°,N24.826° 农桑14 Yuesang 11 2 广西忻城 Xincheng, Guangxi E108.665°,N24.066° 粤桑11 Yuesang 11 2 广西宜州 Yizhou, Guangxi E108.636°,N24.485° 粤桑11 Yuesang 11 4 表 2 用于扩增茄科雷尔氏菌果胶裂解酶基因的引物序列
Table 2 Primer sequences used for amplifying pectate lyase genes of Ralstonia solanacearum
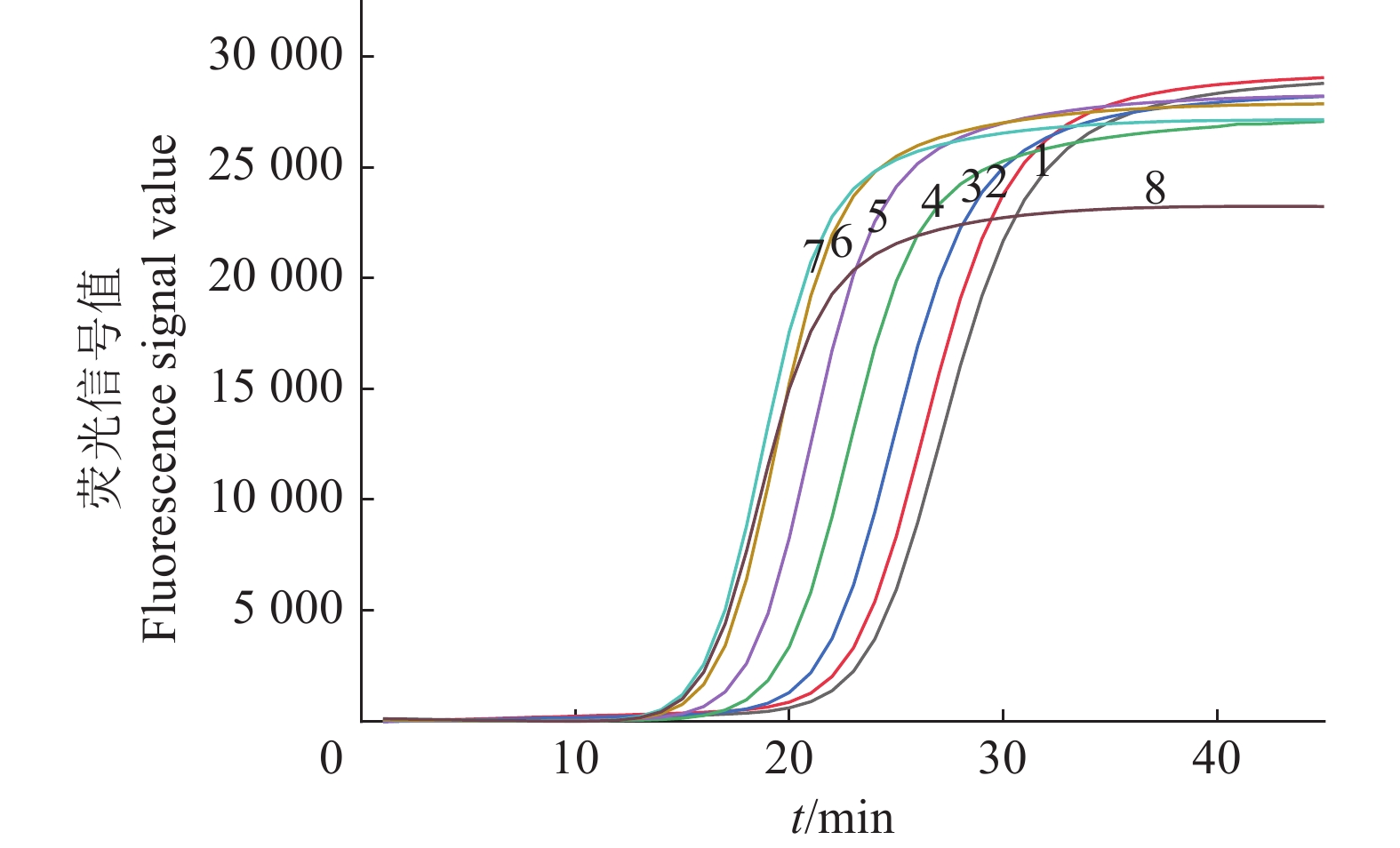
引物组编号
Primer mix number引物名称
Primer name引物序列(5′→3′)
Primer sequence (5′→3′)长度/bp
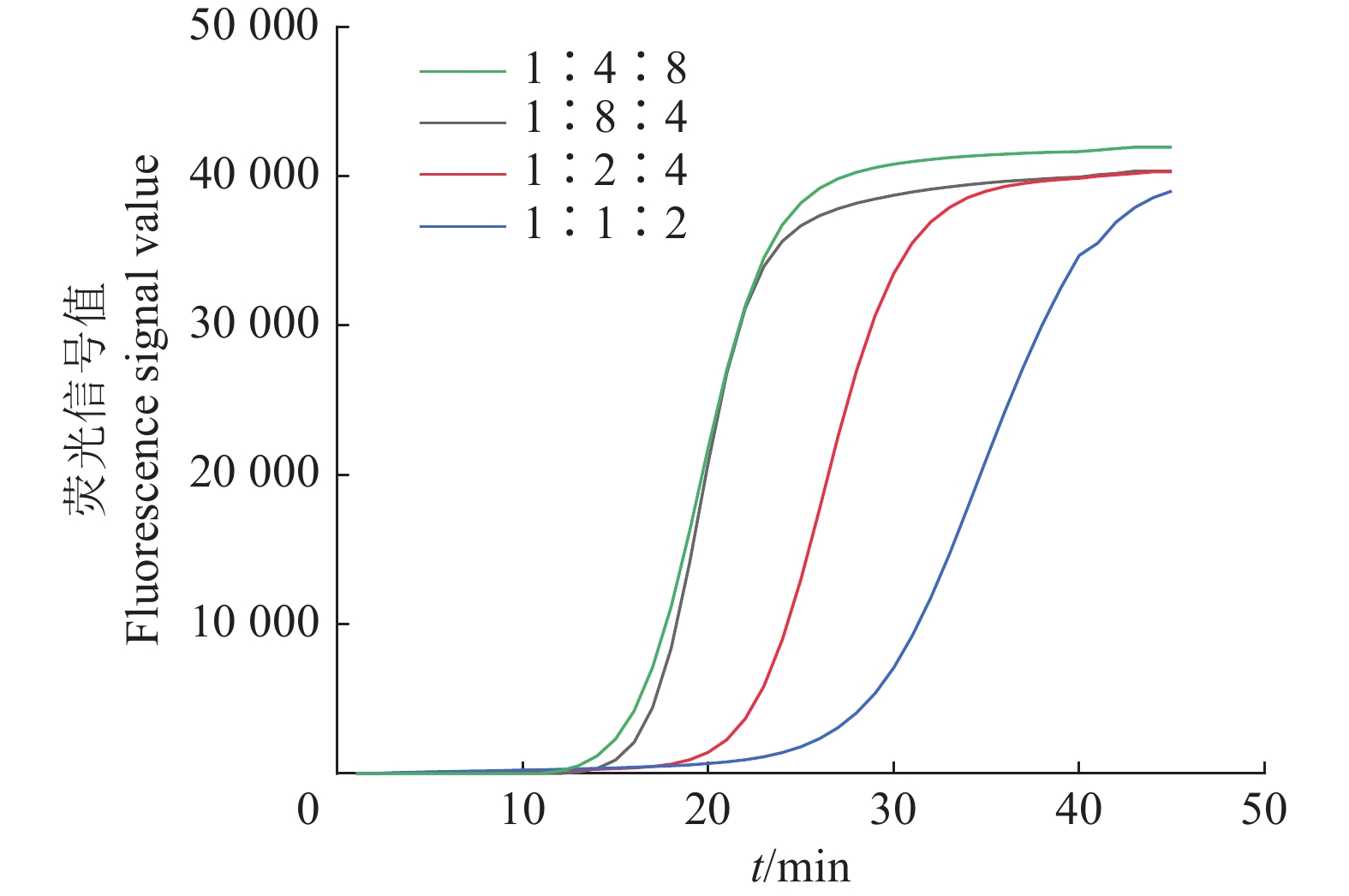
Length1 DsF-1 GTGTCTCAGTCCCAGTGTGGCCTAGTTGGTGGGGTAAAGGC 41 DsR-1 GACAATGGGGGCAACCCTGATCCCAGGTATTACCCAGTGCGA 42 FIT-1 CTGCCTCCCGTAGGAGCCTGCCAAGGCGAACGATCAGTAG 40 RIT-1 CAGGCTCCTACGGGAGGCAGTCTTTCCGGACAAAAGTGCT 40 SteF-1 GACAATGGGGGCAACCCTGATC 22 SteR-1 GTGTCTCAGTCCCAGTGTGGC 21 2 DsF-2 GTACTGCGCGCTGGAGCTGGGAACAACCATTTCCAGACGC 40 DsR-2 GGAACATGCTGAACCAGCCGGGGCCGTTTGCACCGAACC 39 FIT-2 AGCTTGCTCGCTTTGAGCTGCCCTCGACGGGGAATCAC 38 RIT-2 GCAGCTCAAAGCGAGCAAGCTGCCGCCATGATGACCG 37 SteF-2 GGAACATGCTGAACCAGCCGGG 22 SteR-2 GTACTGCGCGCTGGAGCTGG 20 3 DsF-3 GTACTGCGCGCTGGAGCTGGACCATTTCCAGACGCC 36 DsR-3 GGAACATGCTGAACCAGCCGGGGCCGTTTGCACCGAACC 39 FIT-3 GAACAGCTTGCTCGCTTTGAGCTCTCGACGGGGAATCACGA 41 RIT-3 AGCTCAAAGCGAGCAAGCTGTTCGCCGCCATGATGACCG 39 SteF-3 GGAACATGCTGAACCAGCCGGG 22 SteR-3 GTACTGCGCGCTGGAGCTGG 20 4 DsF-4 AACATGCTGAACCAGCCGGGCGCCGTTTGCACCGAACC 38 DsR-4 GTACTGCGCGCTGGAGCTGGACAACCATTTCCAGACGCC 39 FIT-4 GAACAGCTTGCTCGCTTTGAGCTTCGACGGGGAATCACGA 40 RIT-4 AGCTCAAAGCGAGCAAGCTGTTCCGAGCCGCCATGATGAC 40 SteF-4 AACATGCTGAACCAGCCGGGC 21 SteR-4 GTACTGCGCGCTGGAGCTGG 20 5 DsF-5 AGCAGTTGTACTGCGCGCTGGCCATTTCCAGACGCCCTC 39 DsR-5 CGACAACGCCGGCCAGAAGGCCGTTTGCACCGAAC 35 FIT-5 CGAACAGCTTGCTCGCTTTGAGGAATCACGATGCGGGTTCC 41 RIT-5 TCAAAGCGAGCAAGCTGTTCGTCGAGCCGCCATGATGAC 39 SteF-5 CGACAACGCCGGCCAGAA 18 SteR-5 AGCAGTTGTACTGCGCGCTGG 21 6 DsF-6 AGCAGTTGTACTGCGCGCTGCCATTTCCAGACGCCCTC 38 DsR-6 CGACAACGCCGGCCAGAAGGCCGTTTGCACCGAAC 35 FIT-6 CGAACAGCTTGCTCGCTTTGAGAATCACGATGCGGGTTCC 40 RIT-6 TCAAAGCGAGCAAGCTGTTCGGGAATCGAGCCGCCATGATGAC 43 SteF-6 CGACAACGCCGGCCAGAA 18 SteR-6 AGCAGTTGTACTGCGCGCTG 20 表 3 外、茎、内引物体积配比
Table 3 Volume ratio of outer, stem and inner primers
μL 外、茎、内引物体积比
Volume ratio of primers
(Outer∶Stem∶Inner)外引物
Outer primer茎引物
Stem primer内引物
Inner primer无菌水
Sterilized ddH2O总和
TotalDsF DsR SteF SteR FIT RIT 1∶4∶8 2 2 8 8 16 16 48 100 1∶2∶4 2 2 4 4 8 8 72 100 1∶1∶2 2 2 2 2 4 4 84 100 1∶8∶4 2 2 16 16 8 8 48 100 -
[1] LIM S H, CHOI C I. Pharmacological properties of Morus nigra L. (black mulberry) as a promising nutraceutical resource[J]. Nutrients, 2019, 11(2): 437. doi: 10.3390/nu11020437.
[2] YUAN Q, ZHAO L. The mulberry (Morus alba L. ) fruit: A review of characteristic components and health benefits[J]. Journal of Agricultural and Food Chemistry, 2017, 65(48): 10383-10394. doi: 10.1021/acs.jafc.7b03614
[3] CAI M, MU L, WANG Z, et al. Assessment of mulberry leaf as a potential feed supplement for animal feeding in P. R. China[J]. Asian-Australasian Journal of Animal Sciences, 2019, 32(8): 1145-1152. doi: 10.5713/ajas.18.0671
[4] 王越, 童金林, 叶伟清, 等. 桑青枯病发生原因及防治对策[J]. 中国蚕业, 2006, 27(4): 25-26. doi: 10.3969/j.issn.1007-0982.2006.04.009 [5] 肖练章, 朱志德, 何坤良, 等. 桑细菌性青枯病发病规律研究[J]. 广东蚕丝通讯, 1982(2): 3-5. [6] 朱燕, 叶志毅, 吕志强, 等. 桑树青枯病的分布危害和防治的研究进展[J]. 蚕桑通报, 2005, 36(1): 6-9. doi: 10.3969/j.issn.0258-4069.2005.01.002 [7] 毛铿祖. 广东桑青枯病的发生与防治[J]. 中国蚕业, 1996, 30(4): 64-66. [8] 赖文姜, 曾宪铭, 谭炳安, 等. 桑青枯病病原细菌的鉴定[J]. 华南农学院学报, 1982, 3(1): 66-73. [9] LOWE-POWER T M, KHOKHANI D, ALLEN C. How Ralstonia solanacearum exploits and thrives in the flowing plant xylem environment[J]. Trends in Microbiology, 2018, 26(11): 929-942. doi: 10.1016/j.tim.2018.06.002
[10] BRAGARD C, DEHNEN-SCHMUTZ K, DI SERIO F, et al. Pest categorisation of the Ralstonia solanacearum species complex[J]. EFSA Journal, 2019, 17(2): 5618. doi: 10.2903/j.efsa.2019.5618.
[11] NAKANO M, ICHINOSE Y, MUKAIHARA T. Ralstonia solanacearum type III effector RipAC targets SGT1 to suppress effector-triggered immunity[J]. Plant and Cell Physiology, 2020, 61(12): 2067-2076.
[12] SUN T, WU W, WU H, et al. Ralstonia solanacearum elicitor RipX induces defense reaction by suppressing the mitochondrial atpA gene in host plant[J]. International Journal of Molecular Sciences, 2020, 21(6): 2000. doi: 10.3390/ijms21062000.
[13] SCHÖNFELD J, HEUER H, VAN ELSAS J D, et al. Specific and sensitive detection of Ralstonia solanacearum in soil on the basis of PCR amplification of fliC fragments[J]. Applied and Environmental Microbiology, 2003, 69(12): 7248-7256. doi: 10.1128/AEM.69.12.7248-7256.2003
[14] OPINA N, TAVNER F, HOLLWAY G, et al. A novel method for development of species and strain-specific DNA probes and PCR primers for identifying Burkholderia solanacearum(formerly Pseudomonas solanacearum)[J]. Asia Pacific Journal of Molecular Biology and Biotechnology, 1997, 5(1): 19-30.
[15] PIRC M, ALIČ Š, DREO T. Rapid loop-mediated isothermal amplification for detection of the Ralstonia solanacearum species complex bacteria in symptomatic potato tubers and plants[J]. Methods in Molecular Biology, 2021, 2354: 401-413.
[16] KYOSEI Y, YAMURA S, NAMBA M, et al. Antigen tests for COVID-19[J]. Biophysics and Physicobiology, 2021, 18: 28-39. doi: 10.2142/biophysico.bppb-v18.004
[17] 黄雯, 徐进, 张昊, 等. 植物青枯菌LAMP检测方法的建立[J]. 中国农业科学, 2016, 49(11): 2093-2102. doi: 10.3864/j.issn.0578-1752.2016.11.006 [18] KUBOTA R, VINE B G, ALVAREZ A M, et al. Detection of Ralstonia solanacearum by loop-mediated isothermal amplification[J]. Phytopathology, 2008, 98(9): 1045-1051. doi: 10.1094/PHYTO-98-9-1045
[19] 马学军, 丁雄, 聂凯, 等. 新型等温多自配引发扩增技术(IMSA): CN104388581A[P]. 2015-03-04. [20] 丁雄. 新型等温核酸扩增技术(IMSA)的建立及其对传染病病原EV71、CVA16、H7N9 和HIV-1的快速检测应用[D]. 广州: 华南理工大学, 2014. [21] ZHAI J, YAN Z, PING F, et al. Establishment and application of isothermal amplification techniques for the detection of heat-stable I enterotoxin of enterotoxigenic Escherichia coli[J]. PLoS One, 2020, 15(4): e0230881. doi: 10.1371/journal.pone.0230881
[22] 张梦. 溧阳市肺结核病流行情况及等温多自配引发扩增技术在检测结核分枝杆菌中的应用分析[D]. 苏州: 苏州大学, 2018. [23] 乐振窍, 许泽仰, 张细玲, 等. FQ-PCR与IMSA检测转基因豆奶外源基因的比较研究[J]. 大豆科学, 2018, 37(6): 943-949. [24] 王琪, 徐文娟, 石盼盼. IMSA技术快速检测肠出血大肠杆菌O157∶H7方法的建立及应用[J]. 食品工业科技, 2021, 42(17): 263-269. [25] 杨宏宇. 桑枯萎病病原鉴定及分子生物学研究[D]. 广州: 华南农业大学, 2018. [26] DING X, NIE K, SHI L, et al. Improved detection limit in rapid detection of human enterovirus 71 and coxsackievirus A16 by a novel reverse transcription-isothermal multiple-self-matching-initiated amplification assay[J]. Journal of Clinical Microbiology, 2014, 52(6): 1862-1870. doi: 10.1128/JCM.03298-13
[27] 董朝霞, 于翠, 邓文, 等. 桑树青枯病的发生与防治研究进展[J]. 北方蚕业, 2019, 40(4): 1-7. doi: 10.3969/j.issn.1673-9922.2019.04.001 [28] WANG D, YU J, WANG Y, et al. Development of a real-time loop-mediated isothermal amplification(LAMP) assay and visual LAMP assay for detection of African swine fever virus(ASFV)[J]. Journal of Virological Methods, 2020, 276: 113775. doi: 10.1016/j.jviromet.2019.113775.
[29] HUANG W E, LIM B, HSU C C, et al. RT-LAMP for rapid diagnosis of coronavirus SARS-CoV-2[J]. Microbial Biotechnology, 2020, 13(4): 950-961. doi: 10.1111/1751-7915.13586
[30] TECHATHUVANAN C, DRAUGHON F A, D'SOUZA D H. Loop-mediated isothermal amplification (LAMP) for the rapid and sensitive detection of Salmonella Typhimurium from pork[J]. Journal of Food Science, 2010, 75(3): M165-M172. doi: 10.1111/j.1750-3841.2010.01554.x
[31] 刘吉平, 程伟, 宋小景, 等. 一种家蚕蚕卵微孢子虫的LAMP检测引物及其应用: CN104372082A[P]. 2015-02-25. [32] 刘吉平, 周轶楠, 孙勋勋. 一组桑花叶病的LAMP检测引物及试剂盒: CN109055616A[P]. 2018-12-21. [33] 杨宏宇, 周轶楠, 孙勋勋, 等. 桑源阴沟肠杆菌LAMP检测方法的建立和应用[J]. 蚕业科学, 2019, 45(3): 321-330. [34] CHEN X, WANG H, LIU C, et al. Technical note: Development of a closed-tube isothermal multiple self-matching-initiated amplification assay for visual detection of Staphylococcus aureus in milk samples[J]. Journal of Dairy Science, 2021, 104(3): 3569-3574. doi: 10.3168/jds.2020-19023
[35] LIU W, YUAN C, ZHANG L, et al. Establishment and application of isothermal multiple-self-matching-initiated amplification (IMSA) in detecting Type II heat-labile enterotoxin of Escherichia coli[J]. PLoS One, 2019, 14(5): e0216272. doi: 10.1371/journal.pone.0216272
[36] KUBICEK C, STARR T, GLASS N. Plant cell wall-degrading enzymes and their secretion in plant-pathogenic fungi[J]. Annual Review of Phytopathology, 201, 52: 427-451.
[37] CHARKOWSKI A O, ALFANO J R, PRESTON G, et al. The Pseudomonas syringae pv. tomato HrpW protein has domains similar to harpins and pectate lyases and can elicit the plant hypersensitive response and bind to pectate[J]. Journal of Bacteriology, 1998, 180(19): 5211-5217.
[38] OKIRO L A, TANCOS M A, NYANJOM S G, et al. Comparative evaluation of LAMP, qPCR, conventional PCR, and ELISA to detect Ralstonia solanacearum in Kenyan potato fields[J]. Plant Disease, 2019, 103(5): 959-965. doi: 10.1094/PDIS-03-18-0489-RE
[39] 李信申, 黄小梅, 吴淑秀, 等. 植物青枯病菌环介导等温扩增快速检测技术研究[J]. 生物技术通报, 2021, 37(1): 272-281. [40] GOU H, BIAN Z, CAI R, et al. The colorimetric isothermal multiple-self-matchinginitiated amplification using cresol red for rapid and sensitive detection of porcine circovirus 3[J]. Frontiers in Veterinary Science, 2020, 7: 407. doi: 10.3389/fvets.2020.00407.
[41] ZHOU Y, YANG H, LIU J. Complete genome sequence of Enterobacter roggenkampii srain KQ-01, isolated from bacterial wilt-resistant mulberry cultivar YS283[J]. Plant Disease, 2021, 105(3): 688-690. doi: 10.1094/PDIS-07-20-1468-A
[42] 王继承. 桑枯萎病中菠萝泛菌的分离鉴定及防治研究[D]. 广州: 华南农业大学, 2018. [43] 罗龙辉, 王继承, 刘吉平. 桑细菌性枯萎病病原菌的分离鉴定与全基因组序列分析[J]. 植物保护, 2022, 48(1): 44-51.



 下载:
下载: