Correlation between soluble sugar and tolerance to drought stress of cassava stem under low temperature storage
-
摘要:目的
研究木薯种茎在不同温度贮藏不同时间后的失水状况、可溶性糖含量以及相关糖代谢信号通路中有关酶基因表达量的变化,分析不同温度下海藻糖含量与种茎失水率的相关性。
方法以‘木薯60444’种茎为试验材料,采后分别贮藏于低温(20±2)℃、常温(36±2)℃ 0~30 d,测定种茎失水率、相关可溶性糖含量,运用实时荧光定量PCR分析种茎糖代谢相关基因的表达,木薯种茎海藻糖含量和失水率的相关性分析采用Pearson法。
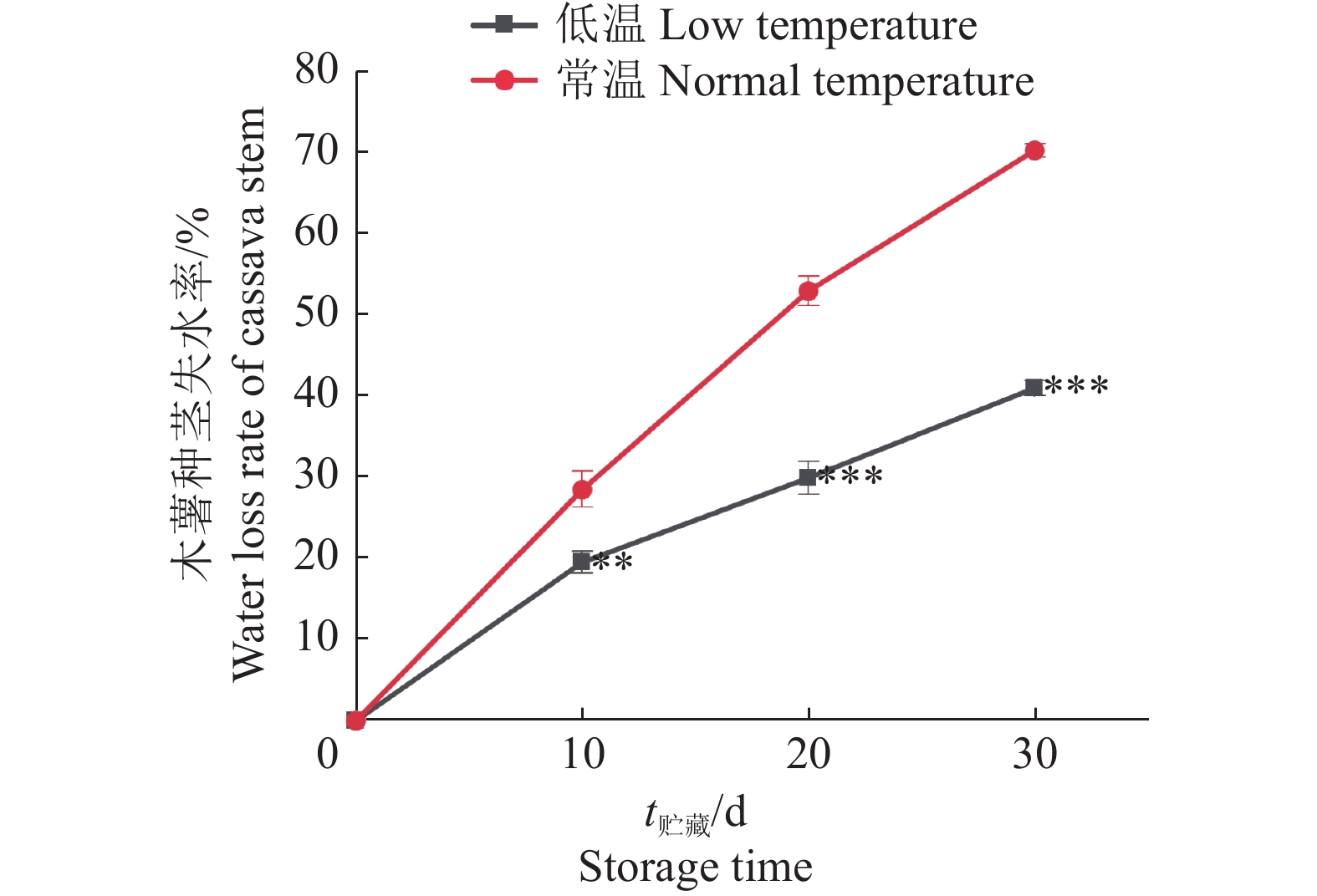
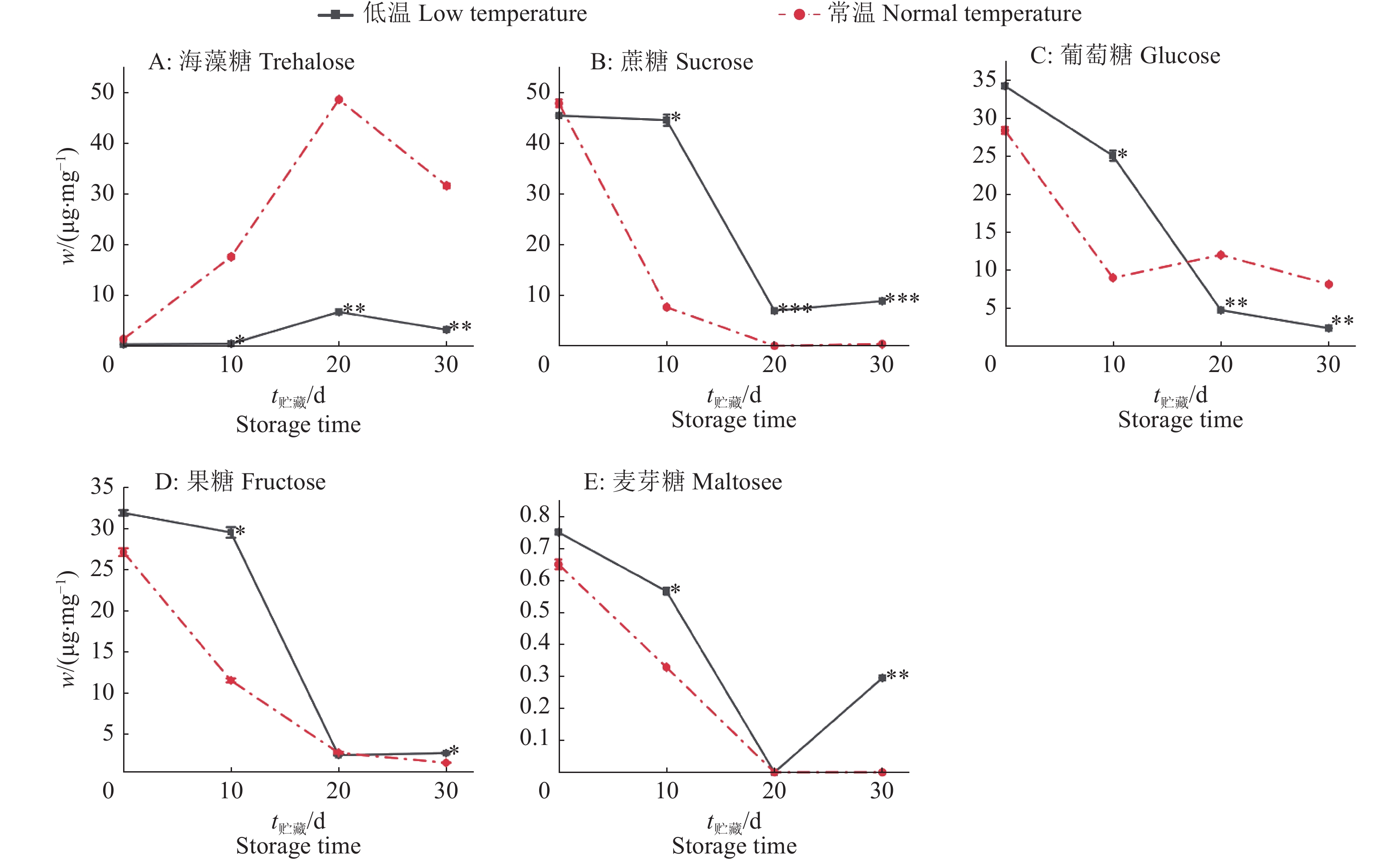
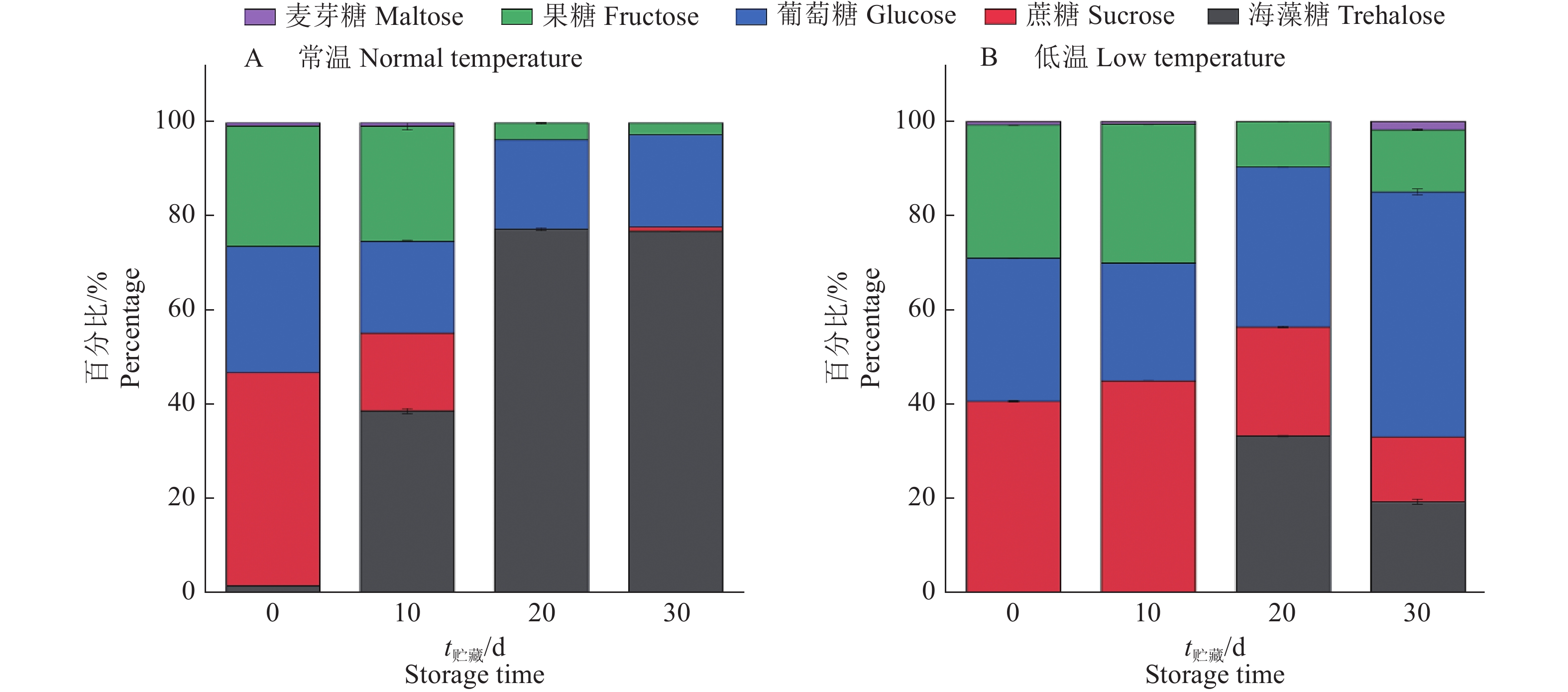
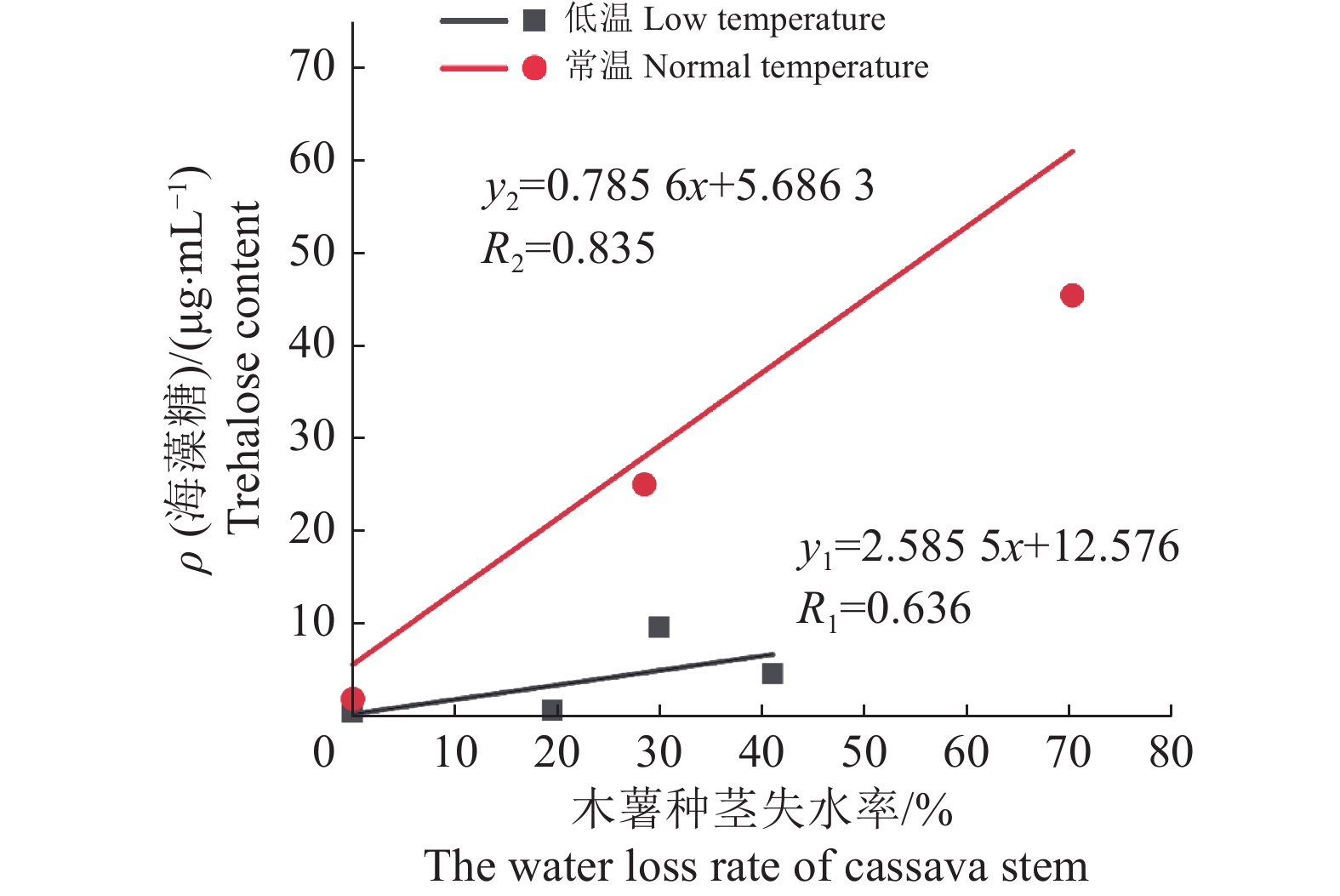
结果低温贮藏组种茎失水率在10、20、30 d显著低于常温贮藏组(P<0.01)。低温与常温贮藏种茎海藻糖含量随贮藏时间的延长整体呈不同程度地提升,且低温贮藏组在10、20、30 d显著低于常温贮藏组(P<0.05);蔗糖、葡萄糖、果糖、麦芽糖含量均随贮藏时间的延长整体呈下降趋势。相关性分析表明,低温贮藏组与常温贮藏组种茎海藻糖含量与种茎失水率呈强线性相关,且2个贮藏组回归方程存在显著差异,低温贮藏组相关系数低于常温贮藏组。实时荧光定量PCR分析表明,低温贮藏不同程度地降低了糖酵解相关基因表达,低温贮藏组海藻糖–6–磷酸合成酶基因(MeTPS-1)的表达量在贮藏10、20、30 d显著低于常温贮藏组(P<0.05)。
结论低温贮藏有助于木薯种茎保水,减缓糖酵解速度,延长贮藏时间。海藻糖与木薯种茎失水胁迫呈强相关性,海藻糖含量上升有助于提升木薯种茎的保水能力。
-
关键词:
- 木薯种茎 /
- 低温贮藏 /
- 海藻糖 /
- 可溶性糖 /
- 海藻糖–6–磷酸合成酶
Abstract:ObjectiveThe changes of water loss status, soluble sugar content and relative enzyme gene expression in related glyco metabolism signal pathway of cassava stem under different storage temperature and time were studied, and the correlation between trehalose content and water loss rate of cassava stem was analyzed.
MethodThe stem of ‘cassava 60444’ was used as the experimental material. The stem was stored under low temperature of (20±2)℃ and normal temperature of (36±2)℃ for 0–30 d after harvest. The water loss status and soluble sugar content were determined, the change of related enzyme gene expression in the signal pathway of sugar metabolism was analyzed by real-time fluorescence quantification PCR, and the correlation between trehalose content and water loss rate of cassava stem was analyzed by Pearson method.
ResultThe water loss rates of cassava stem in low temperature storage group at 10, 20, 30 d were significantly lower than those in normal temperature storage group (P<0.01). The trehalose contents of cassava stems under low and normal temperature storage overall increased to different degrees with the extension of storage time, and the content of low temperature storage group was significantly lower than that of normal temperature storage group at 10, 20, 30 d (P<0.05). The contents of sucrose, glucose, fructose and maltose in low and normal temperature storage groups all showed a decreasing trend with storage time. Correlation analysis showed that there was a strong linear correlation between trehalose content and water loss rate in low and normal temperature storage groups, and there was significant difference in the regression equations between the two storage groups with the smaller correlation coefficient under low temperature storage. Real-time quantitative PCR analysis showed that the expression of glycolysis related genes increased under low and normal temperature for 10–30 d, most related genes in low temperature storage group had lower expression level, and the expression of trehalose-6-phosphate synthase gene (METPS-1) at 10, 20, 30 d was significantly low than that in normal temperature storage group (P<0.05).
ConclusionLow temperature storage of cassava stem contributes to retaining water, slowing down glycolysis rate and prolonging storage time. There is a strong correlation between trehalose and water loss stress of cassava stem, and the increase of trehalose content is helpful to improve the water retention capacity of cassava stem.
-
Keywords:
- Cassava stem /
- Low temperature storage /
- Trehalose /
- Soluble sugar /
- Trehalose-6-phosphate synthase
-
单倍体诱导技术是培育玉米新品种最快速、经济的手段.Stock6[1]是玉米中发现的第1个孤雌生殖诱导系,利用其所选育的诱导系有WS14[2]、MHI[3]等.但Stock6在诱导率、繁殖性能等方面存在严重缺陷,吉林农业大学玉米育种课题组对Stock6进行了遗传改良,成功地获得了诱导率10%以上、遗传标记明显、花粉量大、持粉时间长、抗病性好的新型诱导系JS6.本研究以诱导系JS6的姊妹系JS6-11 ~ JS6-15作父本,以高抗丝黑穗病自交系K88和高感丝黑穗病自交系G115的杂交F1代作为母本材料,杂交诱导产生单倍体,探讨不同诱导因素下单倍体诱导率的变化特点,对有效利用单倍体诱导系及单倍体诱导技术,提高育种效率并选育自有的单倍体诱导系,快速培育玉米自交系并用其选育玉米新品种具有重要意义.
可供加倍的单倍体材料有限,玉米单倍体加倍技术尚不成熟.研究报道,许多玉米材料单倍体自然加倍率低于5%,有些材料根本不发生自然加倍[4-5].因此,要获得大量玉米Double haploid(DH)系并从中选育出优良自交系供生产上利用,必须借助单倍体人工染色体加倍.玉米单倍体的化学加倍方法有很多[5-9],其中秋水仙素应用最为广泛.本研究通过设计4种秋水仙素加倍方式,进一步探讨秋水仙素加倍技术,以期为生产上玉米单倍体的加倍提供理论参考.
1. 材料与方法
1.1 杂交诱导试验
以高抗丝黑穗病自交系K88和高感丝黑穗病自交系G115的杂交F1代作为母本,以吉林农业大学玉米育种课题组选育的5个诱导系JS6-11 ~ JS6-15作为父本,于2011年在吉林农业大学育种基地杂交诱导单倍体.试验设置花丝长短和授粉时期2个因素.花丝长短设2个处理:在长花丝(≥7 cm)和短花丝(≤4 cm)条件下用诱导系花粉授粉;授粉时期设2个处理:伏期(07-15—08-01)和伏后(08-15—09-01)授粉.用于研究的母本材料分别于2011年5月中旬和6月上旬播种.
于母本吐丝后进行授粉,收获后选择结实较好的果穗,在果穗上挑选无色胚芽、紫色粒顶、胚近三角形的准单倍体,所有准单倍体于2012年春种植于吉林农业大学长春玉米育种基地进行鉴定.其中单倍体植株田间表现为矮小、叶片和茎秆均呈绿色、多为不育.根据杂交当代子粒和单倍体子粒数,计算单倍体诱导率:

1.2 单倍体加倍试验
单倍体加倍药剂为西格玛-奥德里奇公司生产的秋水仙素原药、2%(φ)DMSO(二甲基亚砜)和5%(φ)甘油辅助剂.采取4种处理方法,每种方法分3个浓度梯度(0.2、0.4和0.6 mg·mL-1).1)浸根法:单倍体种子浸泡在清水中6 h后置于28 ℃培养箱中催根,待幼苗长到2 ~ 3片叶时,将其置入4 ℃冰箱中炼苗2 ~ 3 h,而后用自编的带有小孔且上面附有1层保湿滤纸的铁丝网将幼芽固定,并将幼根浸泡于不同浓度(0.2、0.4、0.6 mg·mL-1)的秋水仙素+ 2%(φ)DMSO + 5%(φ)甘油溶液中,溶液漫过幼根生长点,浸泡6 h后,再用流水清洗2 h,移栽至大田.2)浸芽法:采用毛巾卷法催芽,当幼芽长约2 cm时用刀片将幼芽顶端胚芽鞘切掉1 ~ 2 mm,使之露出1个小口(但不要伤害到嫩芽),将其在室温下密闭浸泡在不同浓度(0.2、0.4、0.6 mg·mL-1)的秋水仙素+ 2%(φ)DMSO + 5%(φ)甘油溶液中6 h,流水清洗2 h后将其种在育苗盘中,幼苗长到4 ~ 5片叶时移栽至大田.3)滴心叶法:选择长势一致的单倍体幼苗,待其生长到3 ~ 5叶时,分别抽取约1 mL的(0.2、0.4、0.6 mg·mL-1)秋水仙素+ 2%(φ)DMSO + 5%(φ)甘油溶液至单倍体植株的心叶处. 4)针刺生长点法:长势一致的单倍体幼苗田间长到6 ~ 7叶时,用微量移液器抽取5 μL的(0.2、0.4、0.6 mg·mL-1)秋水仙素+ 2%(φ)DMSO + 5%(φ)甘油溶液注射于幼苗茎秆的盾片节处的生长点.
加倍材料源于试验1.1中杂交诱导产生的单倍体,将准单倍体均分4等份(100粒)后根据不同的秋水仙素加倍处理后种植田间,去除非单倍体植株.田间观察成活率、散粉率、结实率和药害情况.以单倍体植株是否散粉和结实来判断玉米单倍体植株是否加倍成功.为防外来花粉授粉结实,试验选取单倍体自交后代结实较好的果穗于2012年冬和2013年春分别在三亚和长春种植观察,以进一步鉴别其加倍情况.



1.3 数据处理
数据采用Excel和DPS[10]软件进行处理及分析.
2. 结果与分析
2.1 不同因素对诱导率的影响
2.1.1 不同花丝长度的单倍体诱导率
从表 1中可以看出,花丝长度对单倍体诱导率有很大影响,花丝≥7 cm时的平均诱导率(17.0%)明显大于花丝长度≤4 cm时的平均诱导率(5.2%).其中在花丝长度≤4 cm时的诱导系中,诱导率最高的是JS6-14,诱导率为7.9%.花丝长度≥7 cm时诱导率最高的诱导系为JS6-13,诱导率为21.2%.诱导系长花丝处理单倍体诱导率高于短花丝处理,说明长花丝诱导效果比短花丝效果好.
表 1 不同花丝长度授粉单倍体诱导率Table 1. Haploid induced rates at different silk length pollination
2.1.2 花丝长度与诱导系对诱导率的影响
花丝长度和诱导系对诱导率的影响的方差分析见表 2.结果表明:不同诱导系诱导率存在显著差异,不同花丝长度诱导率存在极显著差异,说明诱导系和花丝长度对诱导率均有很大影响,且长花丝条件下授粉可以提高诱导率.
表 2 花丝长度与诱导系间的方差分析Table 2. Variance analysis between the silk length and inducer
2.1.3 不同授粉时期的单倍体诱导率
由表 3可知,授粉时期对单倍体诱导率亦有很大影响,伏后授粉时的平均诱导率(18.4%)明显大于伏期授粉时的平均诱导率(5.4%).其中在伏期授粉时,诱导率最高的是诱导系JS6-14(8.1%).伏后授粉时诱导率最高的诱导系为JS6-13(22.8%).诱导系伏后授粉时单倍体平均诱导率(18.4%)高于伏期授粉(5.4%),说明伏后授粉效果更好.
表 3 不同授粉时期单倍体诱导率Table 3. Haploid induced rates at different pollinating dates
2.1.4 授粉时期与诱导系对诱导率的影响
授粉时期和诱导系对诱导率的影响的方差分析见表 4.结果表明:诱导系、授粉时期诱导率均达到了极显著水平,说明不同授粉时期对诱导率有很大影响,且伏后授粉时可以提高单倍体诱导率.此外,相对于花丝长度,授粉时期对诱导率影响更大.
表 4 授粉时期与诱导系间的方差分析Table 4. Variance analysis between the pollinating dates and inducer
2.2 不同方法对单倍体加倍效果的影响
2.2.1 加倍方法对单倍体植株成活率的影响
从表 5可知,滴心叶法的适宜浓度为0.4 mg·mL-1,浸芽法的适宜浓度为0.2 mg·mL-1.针刺生长点法的适宜浓度为0.6 mg·mL-1.在秋水仙素各浓度梯度下浸根法处理时单倍体植株受害程度比其他3种方法严重,0.2、0.4、0.6 mg·mL-1存活率分别为39.3%、42.2%和25.6%.
表 5 不同方法、不同浓度秋水仙素处理单倍体的成活、散粉和结实情况Table 5. The survival, fertility and seed setting of haploid plants under different colchicines concentrations and methods
2.2.2 加倍方法对单倍体植株散粉和结实的影响
由表 5可知,4种加倍方法中,针刺生长点法的效果最好,散粉率均超过10%,在秋水仙素为0.6 mg·mL-1时散粉率达到45.9%;结实率也最高,为15.2%.滴心叶法在0.4 mg·mL-1下散粉率为28.9%,结实率为11.1%;浸根法的散粉率都低于10%,在秋水仙素为0.4和0.6 mg·mL-1下结实率都极低(1.1%);浸芽法虽在0.4 mg·mL-1下散粉率超过10%,但其结实率却很低(1.1%).综上可以看出,在散粉性和结实率方面,针刺生长点法和滴心叶法相对较好.
3. 讨论与结论
3.1 诱导条件对玉米单倍体诱导率的影响
在花丝长度≥7 cm和花丝长度≤4 cm授粉时进行杂交诱导,前者单倍体诱导率较高(21.2%);在伏期授粉(07-15—08-01)时的单倍体诱导率(8.1%)远低于伏后授粉(08-15—09-01)的单倍体诱导率(22.8%).其中花丝长度对玉米单倍体诱导率的影响可能原因是花粉中2个精细胞形成雄性生殖单位是保证2个精核同步转运的重要条件,较长的花丝增加了2个精核在花粉管中运输的不同步性[11].刘志增等[12]研究表明,精核间距在诱导单倍体过程中起重要作用,花丝长使得花粉粒萌发后花粉管到达胚囊距离延长,进而造成2个精核的间距加大,更容易诱导形成单倍体.授粉时期对单倍体诱导率的影响可能同气温有密切关系.授粉期早时温度相对较高,玉米花粉管生长速度快,新陈代谢非常旺盛,能量和物质的消耗都加快了,而供给的能量和物质不会相应地增加,相对于本身内含物就很少的玉米孤雌生殖诱导系花粉粒来说,这种状况会加速花粉管的衰老,不正常花粉的竞争力减弱,从而导致单倍体的产生减少.而授粉晚时,温度相对较低,新陈代谢相对较慢,玉米孤雌生殖诱导系的不正常花粉粒的2个精核在花粉管中有充足的时间分开运输,从而单受精产生玉米单倍体.
姜龙等[13]以玉米单倍体诱导系JS6-1为父本和8个不同母本基础组合在长春、长岭和三亚的研究结果表明,不同基因型诱导基础材料的单倍体诱导率为海南三亚冬繁明显高于长春和长岭,表明昼夜温差大有利于玉米单倍体的诱导.
花丝长短和授粉时期也可能影响了精卵结合的过程,随着花丝的增长,但极核和卵核接受精核的能力均减弱,极核与精核结合的能力相对较强,由此导致胚乳正常发育,而雌配子由于没有受精而发育为单倍体.低温对受精过程也可能有类似影响.从花丝不同时期接受花粉的能力来看,雌穗在吐丝后3 ~ 4 d内抽出的花丝活力较强[14],6 ~ 9 d后活力开始下降[15].考虑到本研究母本基因型较少,有关温度、花丝活力和母本基因型等因素对诱导性能的影响仍需进一步研究.
3.2 人工染色体加倍处理对玉米单倍体加倍的影响
Chase[16]曾提出用秋水仙素溶液注射玉米幼苗的盾片节进行加倍,Gayen等[17]曾采用浸种法,使单倍体加倍率达到了18%.魏俊杰等[18]在6叶期和拔节期用不同浓度的秋水仙素配以DMSO注射处理茎尖生长点,发现在6叶期,以0.5%(φ)秋水仙素配以2.0%(φ)的DMSO处理效果最好,加倍率高达32.3%.敬成俊等[19]研究表明秋水仙素加倍作用是通过与幼嫩组织正在分裂的细胞接触,引起纺锤丝缩减并且结构发生变化,细胞整齐地被阻止在分裂中期,因而使重组核具有加倍的染色体数.秋水仙素在植物组织中迅速扩散,通过维管系统在植物体内运转,实现使植株组织加倍达到长效的目的[9].
本研究秋水仙素处理结果表明:浸根法对植株伤害较严重,存活率低于50%;针刺生长点法(0.6 mg·mL-1)和滴心叶法(0.4 mg·mL-1)的散粉率较高(45.9%,28.9%),相应的结实率也较高(15.2%,11.1%),说明针刺生长点法处理效果最好,滴心叶法次之.其生理生化机制可能是:
1) 玉米根系的最重要功能是从土壤中吸收水分和营养物质,当用一定浓度的秋水仙素处理后,玉米根系的发育受到一定的阻碍,而且秋水仙素也破坏了玉米根系中的根毛和根尖幼嫩组织.移栽到大田后,幼苗吸收水分和营养物质困难,容易过早死亡.二倍体植株具有发达的根系,相对于单倍体根系具有较强的抵抗秋水仙素药害的作用,因此在田间发育良好[20].
2) 针刺生长点法是处理茎尖分生组织,相对于浸根法、浸芽法来说造成的损伤较大,其原因可能是针刺生长点法中秋水仙素注射于茎尖分生组织后并长期作用于茎尖分生组织,而且田间的高温加重了药害,植株的死亡率也很高,即使植株存活下来也表现为叶片发黄、萎缩,但由于秋水仙素长期有效地作用于茎尖分生组织,对植株的加倍效果也很明显,只要植株成活都有可能加倍成功[21].
3) 针刺生长点法和滴心叶法结实率不高的原因可能是多方面的,除了上述秋水仙素造成的药害外,还有加倍成功的植株雌雄花期不协调和生殖器官变态等原因,这样的植株也不会散粉和结实[9].
综上所述,在浸根法和浸芽法中,应该降低秋水仙素的浓度以减小药害,同时浸根法中应该尝试着处理侧根以使植株移栽到大田后能吸收水分和营养物质.针刺生长点法中处理后,应当多浇水,做好田间管理以增加植株存活率.
-
图 1 低温贮藏组与常温贮藏组木薯种茎的失水率
“**”和“***”分别表示相同时间低温储藏组与常温储藏组在P<0.01和P<0.001水平差异显著(t检验)
Figure 1. Water loss rate of cassava stem reposited under low temperature and normal temperature
“**” and “***” indicate significant differences between low temperature storage group and normal temperature storage group at the same time at P<0.01 and P<0.001 levels respectively (t test)
图 2 木薯种茎低温贮藏和常温贮藏0~30 d可溶性糖含量变化
“*”“**”和“***”分别表示在相同储藏时间低温贮藏组与常温贮藏组在P<0.05、P<0.01和P<0.001水平差异显著(t检验)
Figure 2. Changes of soluble sugar contents in cassava stems stored under low and normal temperature for 0–30 d
“*” “**” and “***” indicate significant differences between low and normal temperature storage at the same time at P<0.05, P<0.01 and P<0.001 levels respectively (t test)
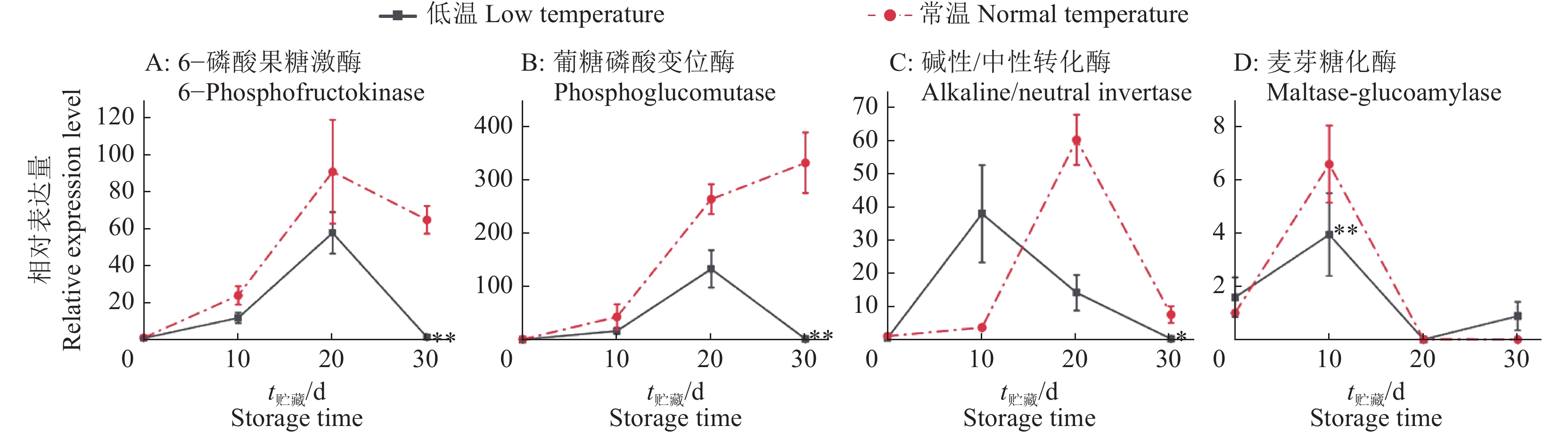
图 5 木薯种茎低温贮藏和常温贮藏0~30 d可溶性糖代谢相关基因表达
“*”和“**”分别表示在相同储藏时间低温贮藏组与常温贮藏组在P<0.05和P<0.01水平差异显著(t检验)
Figure 5. Expression of genes related to soluble sugar metabolism in cassava stems stored under low and normal temperature for 0−30 d
“*” and “**” indicate significant differences between low and normal temperature storage at the same time at P<0.05 and P<0.01 levels respectively (t test)
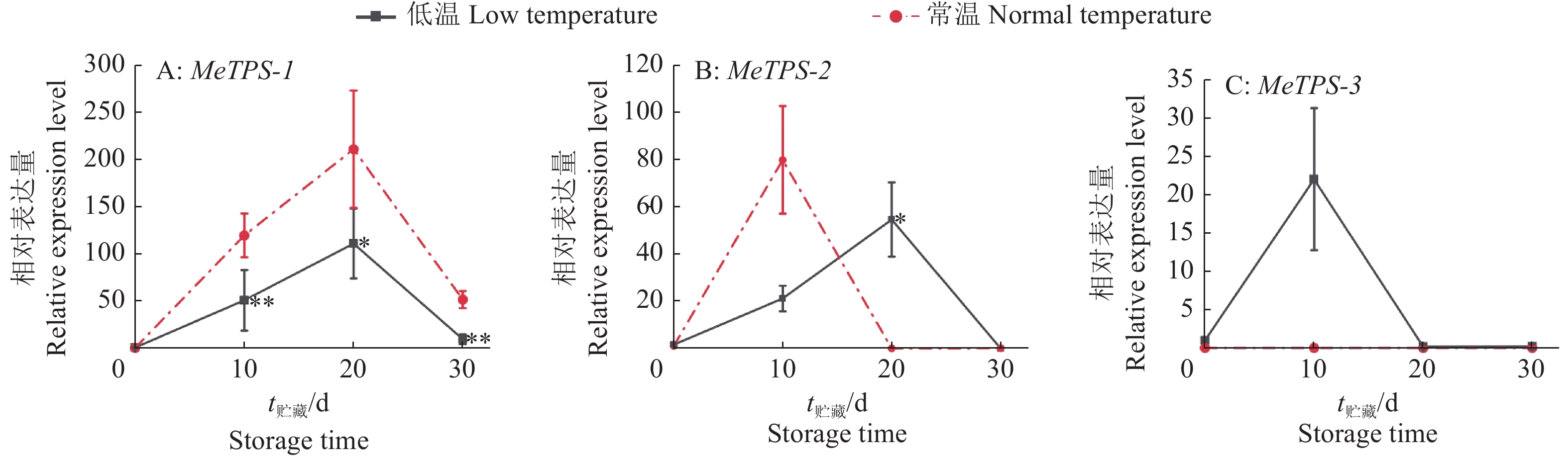
图 6 木薯种茎低温贮藏和常温贮藏0~30 d海藻糖–6–磷酸合成酶(TPS)基因家族部分基因相对表达量
“*”和“**”分别表示在相同储藏时间低温贮藏组与常温贮藏组在P<0.05和P<0.01水平差异显著(t检验)
Figure 6. Relative expression levels of some genes in TPS gene family in cassava stems stored under low and normal temperature for 0−30 d
“*” and “**” indicate significant differences between low and normal temperature storage at the same time at P<0.05 and P<0.01 levels respectively (t test)
表 1 引物序列
Table 1 Primer sequence
名称
Name基因ID
Gene ID正向引物(5′→3′)
Forward primer (5′→3′)反向引物(5′→3′)
Reverse primer (5′→3′)MeActin Manes.12G150600 TGATGAGTCTGGTCCATCCA CCTCCTACGACCCAATCTCA MeTPS-1 Manes.05G087900 TATTGTCAGTGGGAGGGGGA GCCATACCAGAGCACTCTCC MeTPS-2 Manes.01G198900 AGGAGAGTGCATTGGTGTGG CAACAATATGTTGGCCCCGC MeTPS-3 Manes.16G042700 CGCTGCTGAACATGGCTATT TCAGCATCCCTATGATGCCA 6–磷酸果糖激酶
6-PhosphofructokinaseManes.05G021200 ACCTAAACACCACCGACCTC TGAACTGTGGGCTTGGAGAG 麦芽糖化酶
Maltase-glucoamylaseManes.08G060600 AGGAAGCATCCCAGAAAGGC CCCGACCAGACATGTTTCCA 葡糖磷酸变位酶
PhosphoglucomutaseManes.06G141300 GCATCCTCTTCCACTGCCAT CCTTCCTTGCCAACCAGGAT 碱性/中性转化酶
Alkaline/neutral invertaseManes.03G208400 GAACTGCACCCCTTGATGGA ACCACAACCCGGAATCAACA -
[1] 谢向誉, 陆柳英, 曾文丹, 等. 木薯嫩枝茎不同贮藏方式生理特性研究[J]. 中国热带农业, 2016(1): 48-51. doi: 10.3969/j.issn.1673-0658.2016.01.016 [2] 沈光. 良种化和加工增值带动种植实现木薯产业化[J]. 热带农业科学, 2002(5): 57-60. doi: 10.3969/j.issn.1009-2196.2002.05.014 [3] 刘海刚, 孟富宣, 段元杰, 等. 蜡封对木薯种茎贮藏活力的影响[J]. 云南农业大学学报(自然科学), 2020, 35(3): 386-391. [4] YU S M. Cellular and genetic responses of plants to sugar starvation[J]. Plant Physiology, 1999, 121(3): 687-693. doi: 10.1104/pp.121.3.687
[5] JOURNET E P, BLIGNY R, DOUCE R. Biochemical changes during sucrose deprivation in higher plant cells[J]. The Journal of Biological Chemistry, 1986, 261(7): 3193-3199. doi: 10.1016/S0021-9258(17)35767-8
[6] YUAN H, WU Y, LIU W, et al. Mass spectrometry-based method to investigate the natural selectivity of sucrose as the sugar transport form for plants[J]. Carbohydrate Research, 2015, 407: 5-9. doi: 10.1016/j.carres.2015.01.011
[7] JIANG X, NIE Y, KABACK H R. Site-directed alkylation studies with LacY provide evidence for the alternating access model of transport[J]. Biochemistry, 2011, 50(10): 1634-1640. doi: 10.1021/bi101988s
[8] GEIGER D. Plant glucose transporter structure and function[J]. Pflügers Archiv: European Journal of Physiology, 2020, 472(9): 1111-1128.
[9] ZHONG Y, XIE J, WEN S, et al. TPST is involved in fructose regulation of primary root growth in Arabidopsis thaliana[J]. Plant Molecular Biology, 2020, 103(4/5): 511-525.
[10] ROSA M, PRADO C, PODAZZA G, et al. Soluble sugars–Metabolism, sensing and abiotic stress: A complex network in the life of plants[J]. Plant Signaling & Behavior, 2009, 4(5): 388-393.
[11] KEREPESI I, GALIBA G. Osmotic and salt stress-induced alteration in soluble carbohydrate content in wheat seedlings[J]. Crop Science, 2000, 40(2): 482-487. doi: 10.2135/cropsci2000.402482x
[12] BARTELS D, SUNKAR R. Drought and salt tolerance in plants[J]. Critical Reviews in Plant Sciences, 2005, 24(1): 23-58. doi: 10.1080/07352680590910410
[13] 单忠英, 罗兴录, 樊吴静, 等. 干旱胁迫对木薯苗生理特性影响研究[J]. 热带作物学报, 2015, 36(2): 339-343. doi: 10.3969/j.issn.1000-2561.2015.02.020 [14] SHI H, WANG Y, CHENG Z, et al. Analysis of natural variation in Bermudagrass (Cynodon dactylon) reveals physiological responses underlying frought tolerance[J]. PLoS One, 2012, 7(12): e53422. doi: 10.1371/journal.pone.0053422.
[15] GUSSIN A E S. Does trehalose occur in angiospermae?[J]. Phytochemistry, 1972, 11(5): 1827-1828. doi: 10.1016/0031-9422(72)85044-1
[16] ASTRID W. The function of trehalose biosynthesis in plants[J]. Phytochemistry, 2002, 60(5): 437-440. doi: 10.1016/S0031-9422(02)00137-1
[17] NUNES C, SCHLUEPMANN H, DELATTE T L, et al. Regulation of growth by the trehalose pathway: Relationship to temperature and sucrose[J]. Plant Signaling & Behavior, 2013, 8(12): e26626.
[18] ELEUTHERIO E C, ARAUJO P S, PANEK A D. Protective role of trehalose during heat stress in Saccharomyces cerevisiae[J]. Cryobiology, 1993, 30(6): 591-596. doi: 10.1006/cryo.1993.1061
[19] 赵超, 王海燕, 刘美珍, 等. 干旱胁迫下木薯茎杆可溶性糖、淀粉及相关酶的代谢规律[J]. 植物生理学报, 2017, 53(5): 795-806. [20] 张丹. 木薯海藻糖合成酶基因MeTPS1-3的克隆与功能分析[D]. 海口: 海南大学, 2013. [21] HAN B, FU L, ZHANG D, et al. Interspecies and intraspecies analysis of trehalose contents and the biosynthesis pathway gene family reveals crucial roles of trehalose in osmotic-stress tolerance in cassava[J]. International Journal of Molecular Sciences, 2016, 17(7): 1077. doi: 10.3390/ijms17071077.
[22] LUNN J E, FEIL R, HENDRIKS J H, et al. Sugar-induced increases in trehalose 6-phosphate are correlated with redox activation of ADPglucose pyrophosphorylase and higher rates of starch synthesis in Arabidopsis thaliana[J]. Biochemical Journal, 2006, 397(1): 139-148. doi: 10.1042/BJ20060083
[23] 张雯. 钾对苹果果实品质的影响及其与6–磷酸海藻糖代谢途径的关系[D]. 杨凌: 西北农林科技大学, 2017. [24] PEGO J V, KORTSTEE A J, HUIJSER C, et al. Photosynthesis, sugars and the regulation of gene expression[J]. Journal of Experimental Botany, 2000, 51: 407-416. doi: 10.1093/jexbot/51.suppl_1.407
[25] JANG J C, SHEEN J. Sugar sensing in higher plants[J]. The Plant Cell, 1994, 6(11): 1665-1679.
[26] MIRANDA J A, AVONCE N, SUÁREZ R, et al. A bifunctional TPS-TPP enzyme from yeast confers tolerance to multiple and extreme abiotic-stress conditions in transgenic Arabidopsis[J]. Planta, 2007, 226(6): 1411-1421. doi: 10.1007/s00425-007-0579-y
[27] ZANG B, LI H, LI W, et al. Analysis of trehalose-6-phosphate synthase (TPS) gene family suggests the formation of TPS complexes in rice[J]. Plant Molecular Biology, 2011, 76(6): 507-522. doi: 10.1007/s11103-011-9781-1
[28] VANDESTEENE L, RAMON M, LE ROY K, et al. A single active trehalose-6-P synthase (TPS) and a family of putative regulatory TPS-like proteins in Arabidopsis[J]. Molecular plant, 2010, 3(2): 406-419. doi: 10.1093/mp/ssp114
[29] SHIM J S, SEO J S, SEO J S, et al. Heterologous expression of bacterial trehalose biosynthetic genes enhances trehalose accumulation in potato plants without adverse growth effects[J]. Plant Biotechnology Reports, 2019, 13(4): 409-418. doi: 10.1007/s11816-019-00554-z



 下载:
下载: