Effect of biochar on microbial composition and function in continuous cropping ginseng soil
-
摘要:目的
探究栽培人参Panax ginseng C. A. Mey.后土壤细菌群落多样性与功能变化,以及增施生物质炭对土壤细菌群落多样性与功能的影响。
方法对人参连作土壤进行不同生物质炭改良的田间试验,结合高通量测序技术,分析土壤细菌群落多样性与功能变化。
结果植参土壤(前茬作物为三年生人参)中Spartobacteria_genera_incertae_sedis、Sphingomonas、Gemmatimonas、 Afipia 、Gp1、Gp2、Gp3、Gp6、Rummeliibacillus 9个属细菌数量显著降低,表明栽培人参或人参根系分泌物可能抑制上述细菌的生长。另外,植参土壤Gaiella属细菌数量显著增加,添加生物质炭后该属优势度进一步增加;说明栽培人参或人参根系分泌物以及施用生物质炭均可促进该细菌的生长。相较于新林土,植参土壤细菌数量、群落多样性、细菌分类组成及优势属占比均不同程度地下降,单优势种群比例上升。生物质炭处理对上述劣变趋势具有一定的正向调节作用,细菌分类组成及数量变化趋势趋向于新林土,并协助提升细菌染色质结构和动力学,转录,复制、重组和修复,信号转导机制与细胞防御功能。
结论增施生物质炭能够提升植参土壤细菌多样性,调节细菌群落结构以及细菌功能,使老参地土壤朝良好的方向发展。研究结果为连作人参土壤的修复及人参栽培提供了理论参考。
Abstract:ObjectiveTo explore the changes of soil bacterial community diversity and function after planting ginseng (Panax ginseng C. A. Mey.), and the effects of biochar application on soil bacterial community diversity and function.
MethodThe field experiments with different biomass charcoals were conducted to improve the soil of continuous cropping ginseng field, and the changes of bacterial community diversity and function were analyzed by high-throughput sequencing technology.
ResultThe bacteria number of Spartobacteria_genera_incertae_sedis, Sphingomonas, Gemmatimonas,Afipia, Gp1, Gp2, Gp3, Gp6, and Rummeliibacillus in the soil after planting ginseng significantly decreased, indicating that cultivating ginseng or ginseng root secretions might inhibit the growth of these bacteria. In addition, the number of Gaiella bacteria in soil of planting ginseng field increased significantly, and further increased after applying biochar, indicating that all cultivating ginseng, ginseng root exudates and applying biochar could promote the growth of bacteria. Compared with the new forest soil, the number of soil bacteria, community diversity, bacterial taxonomic composition and the proportion of dominant genera in the continuous cropping ginseng field declined to varying degrees, and showed an increase in proportion of single dominant population. Biomass charcoal treatment had a certain positive regulation effect on the above-mentioned deterioration trend, and the change trend of bacterial classification and quantity tends to those of the new forest soil. The biomass charcoal assisted in improving bacteria chromatin structure and dynamics, transcription, replication recombination and repair, signal transduction mechanism and cell defense function.
ConclusionBiochar application can improve soil bacterial diversty, regulate bacterial community structure and function, and make soil development of continuous cropping ginseng field in a good direction. The result provides therotical reference for soil restoration and ginseng cultivation in the continuous cropping ginseng field.
-
褐飞虱Nilaparvata lugens(Stål)属半翅目同翅亚目飞虱科(Homoptera: Delphacidae),是典型的r–对策型害虫,具有易暴发、远距离迁飞等特点,自20世纪60年代以来已成为我国水稻Oryza sativa的首要害虫[1-2]。褐飞虱除直接危害水稻外,还可以传播水稻从矮缩病等植物病毒病,引起水稻等作物的大面积受害,造成严重的经济损失[3-4]。化学防治一直是控制褐飞虱的重要途径[5],但长期大面积使用单一农药品种,不仅污染环境,而且会使褐飞虱抗药性水平不断提高,亚洲不少国家和地方的褐飞虱几乎对当前所有常用农药品种均产生了不同程度的抗药性[6-11]。20世纪80年代中后期,噻嗪酮被引入我国用于防治褐飞虱,2005年监测到褐飞虱对噻嗪酮已产生低水平抗性[12],2010监测到褐飞虱对噻嗪酮已产生高水平抗性[10]。新烟碱类杀虫剂吡虫啉1995年被引入我国防治褐飞虱,一直是稻飞虱的主要防治药剂,但在2005年检测到褐飞虱对吡虫啉已产生极高抗性,随后农业部发文要求暂停使用吡虫啉防治高抗褐飞虱,但最近报道发现褐飞虱对吡虫啉抗性依然有上升趋势[8-9, 13-14]。2005年,吡虫啉在褐飞虱的防治上被停用后,噻虫嗪和吡蚜酮成为我国褐飞虱防治的主要药剂[8-9],导致褐飞虱对噻嗪酮和吡蚜酮的抗药性不断上升。
褐飞虱属迁飞性害虫,各地用药水平不同,而广东作为褐飞虱从东南半岛迁入我国的第一站,也是稻飞虱回迁东南半岛的出口,因此,在亚洲稻区褐飞虱的发生和防治上,广东稻区处于极其重要的地理位置。有必要长期、系统地监测广东不同地方褐飞虱种群对常用药剂的抗性水平,为科学指导田间用药和开展褐飞虱抗药性治理提供依据。本研究采用稻苗浸渍法,测定广东省7个不同稻区褐飞虱种群对噻嗪酮、吡虫啉、噻虫嗪和吡蚜酮等4种常用杀虫剂的抗药性。
1. 材料与方法
1.1 材料
2015年10月和2016年8—10月,分别从广东省广州市、雷州市、连州市、南雄市、海丰县、大埔县和怀集县等7个地方稻田采集褐飞虱高龄若虫或成虫,在温室内的人工气候箱中采用未经药剂处理过的水稻(水稻品种为‘TN1’)幼苗饲养,隔离饲养至下一代,然后挑选3龄若虫进行抗药性测定。
96%(w)噻嗪酮原药和96%(w)吡虫啉原药购自广东大丰植保科技有限公司;99.1%(w)噻虫嗪原药购自先正达(中国)投资有限公司;25%(w)吡蚜酮可湿性粉剂购自苏安邦电化有限公司。
1.2 方法
采用稻苗浸渍法测定抗药性。选取‘TN1’种子进行浸泡和催芽处理,在温室内用塑料杯(直径6 cm,高7.5 cm)种植,每杯均匀播种 5~7 粒。20 d后,用剪刀剔除多余的稻苗,每杯留3株生长最为健壮的稻苗待用。在电子天平(精度为万分之一)上准确称取药剂,用丙酮稀释成一定浓度的母液, 用含有φ为0.1%的吐温–80的蒸馏水稀释母液,每种药剂按等比系列稀释成6个浓度,将稻苗分别在不同浓度的药液中浸泡 30 s,以含有φ为0.1%吐温–80的蒸馏水作为对照,每个浓度重复4次,接入3龄若虫,每杯 20 头,罩上纱网罩。静置2 h后,剔除损伤个体,然后将装置放入(26±1) ℃,光周期为 16 h光∶8 h暗的人工气候箱中。4 d后检查若虫死亡数量,以细毛笔触动虫体后不能运动作为死亡标准。对照组死亡率超过20%时试验无效。
1.3 数据处理
根据测定数据计算并得到药剂毒力回归方程、LC50值及95%置信区间和相关系数,利用统计软件DPS处理相关数据。以LC50的95%置信区间是否重叠判断不同来源地褐飞虱种群对同一种杀虫剂的抗性是否差异显著[9]。
抗性倍数(Resistance ratio,RR)=所测种群LC50/敏感种群LC50。
抗性水平按文献[15]分级: RR< 3为敏感阶段; 3.1≤RR<5.0为敏感性下降阶段; 5.1≤RR<10.0为低水平抗性; 10.1≤RR<40.0为中等水平抗性; 40.1≤RR<160.0为高水平抗性; RR>160.1为极高水平抗性。褐飞虱对噻嗪酮、吡虫啉、噻虫嗪和吡蚜酮的敏感基线分别为0.07、0.08、0.11和2.57 mg·L–1[9]。
2. 结果与分析
2.1 广东褐飞虱种群对噻嗪酮的抗性
从表1可以看出,除广州市褐飞虱种群对噻嗪酮抗性倍数为93.4倍,属高水平抗性外,其他6个地方褐飞虱种群对噻嗪酮抗性倍数为324.6~1497.8倍,属极高水平抗性。广东省不同地方褐飞虱种群对噻嗪酮的抗性差异较大,其中大埔县褐飞虱种群对噻嗪酮的抗性为广州市褐飞虱种群对噻嗪酮的抗性的16倍。从LC50置信限来看,广州市褐飞虱种群对噻嗪酮的抗性与广东省其他6个地方褐飞虱对噻嗪酮的抗性差异显著;南雄市、怀集县和海丰县褐飞虱种群对噻嗪酮的抗性差异不显著;连州市、雷州市和大埔县褐飞虱种群对噻嗪酮的抗性差异不显著。
表 1 广东褐飞虱种群对噻嗪酮的抗性Table 1. Resistance of Nilaparvata lugens populations to buprofezin in Guangdong Province种群来源 毒力回归方程1) LC50/(mg·L–1) LC5095%置信限2)/(mg·L–1) 相关系数 抗性倍数 广州市 y=4.502 8+0.609 8x 6.536 4 0.905 6~12.766 2 0.966 4 93.4 南雄市 y=3.434 4+1.154 2x 22.720 6 16.430 1~31.035 8 0.937 2 324.6 怀集县 y=3.784 4+0.856 7x 26.238 9 16.034 9~36.756 4 0.912 8 374.8 海丰县 y=3.954 2+0.735 9x 26.378 2 16.766 2~47.039 7 0.948 2 376.8 连州市 y=3.328 4+0.889 7x 75.650 3 52.998 3~110.365 2 0.946 3 1 080.7 雷州市 y=2.800 5+3.040 9x 77.390 4 55.076 7~103.894 1 0.931 4 1 105.6 大埔县 y=3.593 5+0.696 1x 104.847 8 62.190 5~186.993 5 0.938 1 1 497.8 1) x 表示杀虫剂质量浓度,y 表示峰面积;2) 数据范围有重叠表明不同来源地褐飞虱种群对噻嗪酮的抗性差异不显著 2.2 广东褐飞虱种群对吡虫啉的抗性
表2结果表明,广东省不同地方褐飞虱种群对吡虫啉抗性倍数为161.9~3 576.4倍,均高于160.1倍,属极高水平抗性。广东省不同地方褐飞虱种群对吡虫啉的抗性差异较大,其中连州市褐飞虱种群对吡虫啉的抗性为广州市褐飞虱种群吡虫啉的抗性的22倍。从LC50置信限来看,广州市褐飞虱种群对吡虫啉的抗性与广东省其他6个地方褐飞虱对吡虫啉的抗性差异显著;海丰县、南雄市和雷州市3个地方褐飞虱种群对吡虫啉抗性差异不显著;连州市褐飞虱种群对吡虫啉抗性与大埔县褐飞虱种群对吡虫啉抗性差异不显著,但与广东省其他5个地方褐飞虱种群对吡虫啉的抗性差异显著。
表 2 广东褐飞虱种群对吡虫啉的抗性Table 2. Resistance of Nilaparvata lugens populations to imidacloprid in Guangdong Province种群来源 毒力回归方程1) LC50/(mg·L–1) LC5095%置信限2)/(mg·L–1) 相关系数 抗性倍数 广州市 y=4.161 6+1.850 3x 12.954 6 5.811 5~20.468 0 0.954 6 161.9 海丰县 y=3.877 2+0.305 4x 41.679 0 33.513 0~52.518 0 0.981 1 521.0 南雄市 y=3.710 4+0.761 0x 49.502 8 31.029 9~118.548 1 0.955 3 618.8 雷州市 y=2.114 0+1.609 0x 62.195 1 46.408 8~81.447 1 0.966 7 777.4 怀集县 y=2.487 0+1.283 5x 90.753 1 67.393 7~138.809 9 0.986 6 1 134.4 大埔县 y=3.650 4+0.594 9x 185.682 4 101.728 8~302.342 6 0.943 6 2 321.0 连州市 y=2.863 0+0.869 9x 286.111 9 166.087 2~407.362 6 0.906 7 3 576.4 1) x 表示杀虫剂质量浓度,y 表示峰面积;2) 数据范围有重叠表明不同来源地褐飞虱种群对吡虫啉的抗性差异不显著 2.3 广东褐飞虱种群对噻虫嗪的抗性
从表3可以看出,广州市、南雄市和怀集县褐飞虱种群对噻虫嗪抗性倍数分别为61.0、102.1和122.6倍,属高水平抗性,其他4个地方褐飞虱种群对噻虫嗪抗性倍数为171.0~517.8倍,属极高水平抗性。广东省不同地方褐飞虱种群对噻虫嗪的抗性差异较大,从LC50置信限来看,广州市褐飞虱种群对噻虫嗪的抗性与南雄市褐飞虱种群对噻虫嗪的抗性差异不显著,但与广东省其他5个地方褐飞虱对噻虫嗪的抗性差异显著;南雄市、怀集县、大埔县3个地方褐飞虱种群对噻虫嗪抗性差异不显著;大埔县、海丰县、连州市和雷州市4个地方褐飞虱种群对噻虫嗪抗性差异不显著。
表 3 广东褐飞虱种群对噻虫嗪的抗性Table 3. Resistance of Nilaparvata lugens populations to thiamethoxam in Guangdong Province种群来源 毒力回归方程1) LC50/(mg·L–1) LC5095%置信限2)/(mg·L–1) 相关系数 抗性倍数 广州市 y=3.060 6+2.345 1x 6.714 6 3.870 9~9.367 9 0.928 3 61.0 南雄市 y=2.108 8+2.752 0x 11.235 6 8.444 6~13.788 1 0.953 1 102.1 怀集县 y=2.914 3+1.845 6x 13.490 9 10.691 8~16.249 64 0.962 1 122.6 大埔县 y=3.729 9+0.996 6x 18.812 8 12.372 9~26.429 7 0.976 7 171.0 海丰县 y=3.365 6+1.256 7x 19.978 3 14.592 4~28.888 6 0.984 3 181.6 连州市 y=3.039 2+1.267 4x 35.246 1 26.804 1~49.442 7 0.980 8 320.4 雷州市 y=3.338 4+0.603 0x 56.958 9 15.242 8~168.715 2 0.940 4 517.8 1) x 表示杀虫剂质量浓度,y 表示峰面积;2) 数据范围有重叠表明不同来源地褐飞虱种群对噻虫嗪的抗性差异不显著 2.4 广东褐飞虱种群对吡蚜酮的抗性
从表4可以看出,南雄市褐飞虱种群和广州市褐飞虱种群对吡蚜酮的抗性倍数分别为3.7和4.6倍,说明南雄市褐飞虱种群和广州市褐飞虱种群对吡蚜酮表现为敏感下降;雷州市、海丰县、连州市和怀集县褐飞虱种群对吡蚜酮的抗性倍数为5.5~9.4倍,表明这4个地方褐飞虱种群对吡蚜酮已产生低水平抗性;大埔县褐飞虱种群对吡蚜酮的抗性倍数为11.0倍,说明大埔县褐飞虱种群对吡蚜酮已产生中等抗性水平。从LC50置信限来看,除南雄市褐飞虱种群对吡蚜酮抗性与大埔县褐飞虱种群对吡蚜酮抗性差异显著外,其余6个地方褐飞虱种群对吡蚜酮抗性差异不显著。
表 4 广东褐飞虱种群对吡蚜酮的抗性Table 4. Resistance of Nilaparvata lugens populations to pymetrozine in Guangdong Province种群来源 毒力回归方程1) LC50/(mg·L–1) LC5095%置信限2)/(mg·L–1) 相关系数 抗性倍数 南雄市 y=2.458 3+2.580 8x 9.427 7 6.570 8~12.030 5 0.930 7 3.7 广州市 y=4.143 5+0.798 1x 11.833 6 5.221 6~18.540 6 0.954 4 4.6 雷州市 y=3.998 4+0.871 2x 14.112 7 12.838 0~32.732 6 0.982 8 5.5 海丰县 y=4.482 2+0.442 6x 14.790 2 8.853 2~32.564 6 0.974 0 5.8 连州市 y=2.558 3+1.183 9x 15.439 2 8.483 4~27.066 9 0.990 7 6.0 怀集县 y=3.965 3+0.747 5x 24.229 4 12.758 7~35.849 5 0.975 0 9.4 大埔县 y=4.318 2+0.470 4x 28.149 5 12.481 1~57.011 7 0.938 9 11.0 1)x 表示杀虫剂质量浓度,y 表示峰面积;2) 数据范围有重叠表明不同来源地褐飞虱种群对吡蚜酮的抗性差异不显著 3. 讨论与结论
噻嗪酮是一种通过抑制昆虫几丁质合成和干扰新陈代谢的选择性杀虫剂, 2005 年之前褐飞虱对噻嗪酮依然为敏感至敏感性下降阶段[12];2005 年之后,褐飞虱对噻嗪酮的抗药性快速上升,研究表明已达高至极高的抗性水平[9, 16-18]。褐飞虱对噻嗪酮抗性发展变化,可能与我国防治褐飞虱时使用的农药有关。2005年之前,噻嗪酮先后被吡虫啉、氟虫腈这 2 种药剂所取代[19],药物取代使得噻嗪酮停用,从而延缓了褐飞虱对其抗性的发展。2005年后,随着吡虫啉的被限用和氟虫腈在稻田的禁用,轮换药剂的减少和噻嗪酮用量的增加,致使褐飞虱对噻嗪酮抗性快速上升。本研究结果表明,除广州市褐飞虱对噻嗪酮产生高水平抗性外,广东其余 6 个地方褐飞虱均对噻嗪酮均已产生极高水平抗性。
自 2005 年,我国首次监测到褐飞虱种群对吡虫啉产生高水平抗药性以来,尽管吡虫啉被要求暂停用于防治稻飞虱,但田间褐飞虱种群对吡虫啉抗药性仍处于高到极高水平抗性阶段[9, 17, 20-22]。这可能有以下两方面原因:一是近年来白背飞虱 Sogatella furcifeca 和由白背飞虱传播的水稻南方黑条矮缩病发生越来越严重,吡虫啉对白背飞虱具有极高的敏感性[23-25],而农民通常选择吡虫啉来防治白背飞虱,这就加大了和白背飞虱同时发生的选择压力;二是尽管我国要求暂停使用吡虫啉防治褐飞虱,但我国褐飞虱种群的来源地东南亚国家仍在使用吡虫啉防治褐飞虱[26-27]。本研究结果显示,广东省褐飞虱种群对吡虫啉抗性倍数(161.9~3 576.4 倍) 均高于 100 倍,属极高水平抗性。
刘叙杆等[19]研究发现2005—2009 年大于90%的褐飞虱种群对噻虫嗪的抗性倍数为2.0~15.8 倍,还处于敏感性下降和刚开始产生抗性的阶段,而到了2010 年,45%的褐飞虱监测种群对噻虫嗪的抗性上升到中等水平抗性。李燕芳等[28]2013 年报道广州市钟落潭田间褐飞虱种群对噻虫嗪仍属敏感水平 (2.67 倍),但本文监测到广州市钟落潭田间褐飞虱种群对噻虫嗪抗性为 61.0 倍,已达高水平抗性。噻虫嗪抗药性的快速上升,一方面是随着吡虫啉的限用,噻虫嗪使用量不断增加,加大了其选择压力;另一方面可能与噻虫螓和吡虫啉这 2 种药剂之间具有一定的交互抗性有关。褐飞虱对噻虫嗪的抗性上升明显,应该引起有关部门的重视。广东褐飞虱种群对噻虫嗪的抗性倍数为 61.0~517.8 倍,表明广东褐飞虱种群对噻虫嗪已产生中等水平至高水平抗性。
凌炎等[29]2010年监测了我国和越南14个褐飞虱田间种群,发现褐飞虱对吡蚜酮均处于敏感至低水平抗性阶段(0.17~6.56倍)。王鹏等[9]报道2010年7个监测褐飞虱种群对吡蚜酮的抗性倍数为1.9~5.1倍,属于敏感至低水平抗性,2011年监测的褐飞虱种群对吡蚜酮的抗性倍数为15.7~25.4倍,已达中等水平抗性。康晓霞等[22]报道邗江地方2012和2013年褐飞虱种群对吡蚜酮已达中等至高水平抗性(25.9和71.0倍)。不同地方褐飞虱种群对吡蚜酮抗性水平不同,说明不同地方的用药水平不同。广东褐飞虱种群对吡蚜酮抗性处于敏感至中等水平抗性。
褐飞虱抗药性的产生严重影响其防治效果,褐飞虱种群抗药性的监测及治理就显得尤为重要。根据本文的监测结果,建议在广东省水稻褐飞虱种群防治中,暂时停止使用吡虫啉、噻嗪酮和噻虫嗪,交替轮流使用吡蚜酮、烯定虫胺和呋虫胺等不同作用机理的药剂,以延缓褐飞虱抗药性的产生。
-
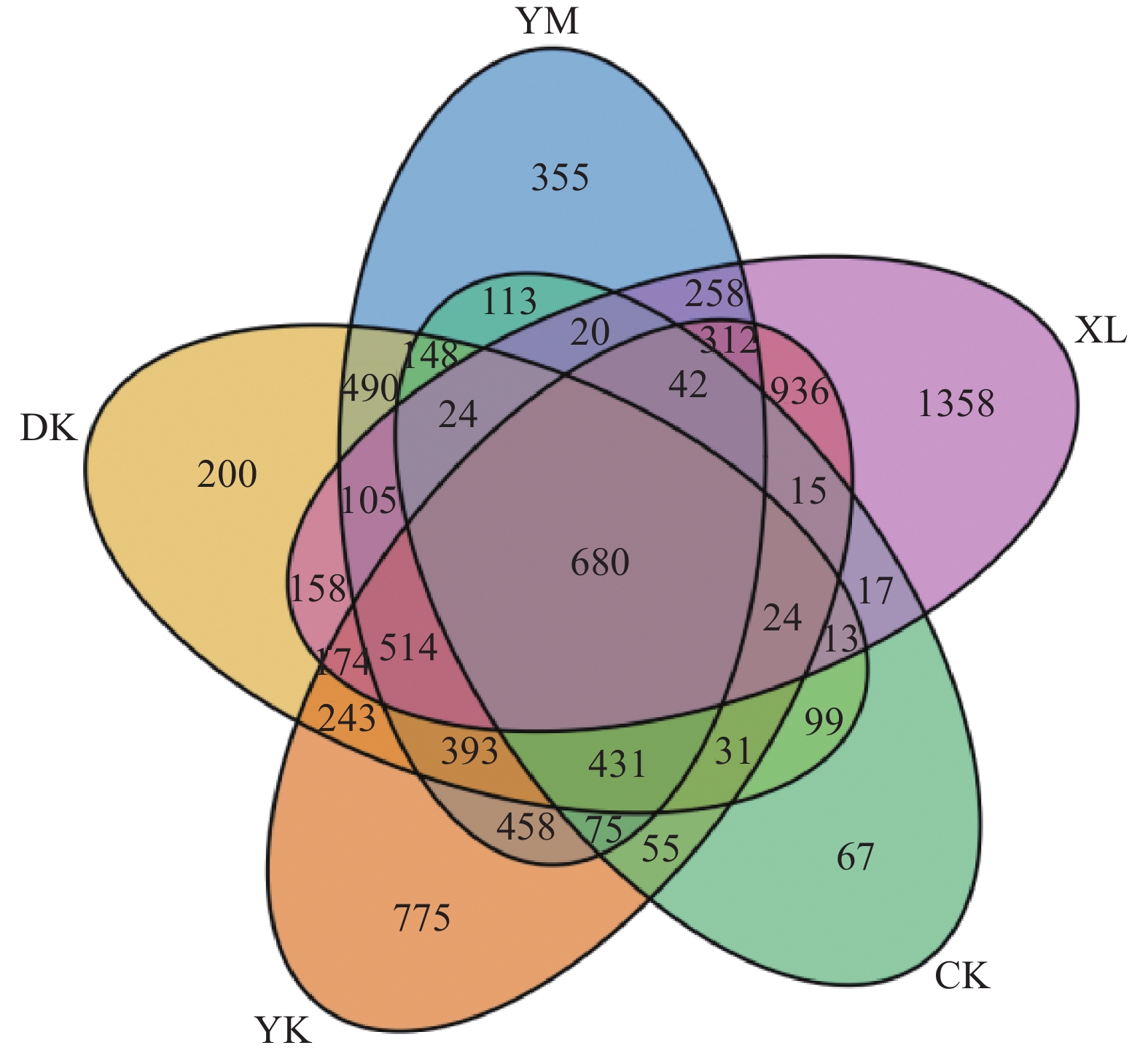
图 1 不同处理下老参地土壤OTUs的维恩图
YM:老参地+玉米秸秆炭,DK:老参地+稻壳炭,YK:老参地+椰壳炭,CK:老参地,XL:新林土
Figure 1. Venn diagram of soil OTUs in the continuous cropping ginseng field under different treatments
YM: Continuous cropping ginseng field + corn stalk biochar, DK: Continuous cropping ginseng field + rice husk biochar, YK: Continuous cropping ginseng field + coconut shell biochar, CK: Continuous cropping ginseng field, XL: New forest soil
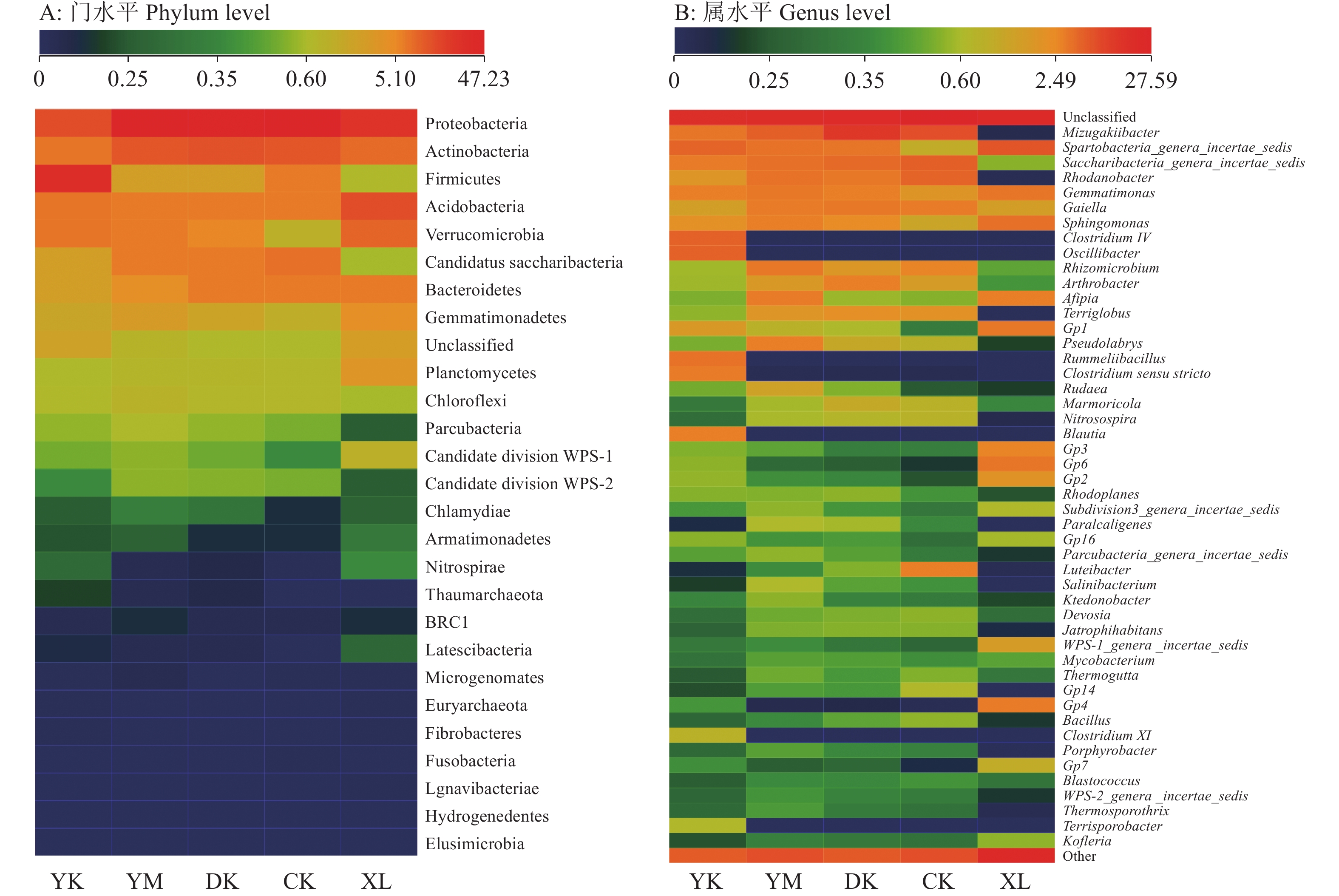
图 2 生物质炭对连作参地土壤细菌群落门类和属水平的影响
YM:老参地+玉米秸秆炭,DK:老参地+稻壳炭,YK:老参地+椰壳炭,CK:老参地,XL:新林土
Figure 2. Effect of biomass charcoal on the phylum and genus level of soil bacterial community in continuous cropping ginseng field
YM: Continuous cropping ginseng field+corn stalk biochar, DK: Continuous cropping ginseng field+rice husk biochar, YK: Continuous cropping ginseng field+coconut shell biochar, CK: Continuous cropping ginseng field, XL: New forest soil
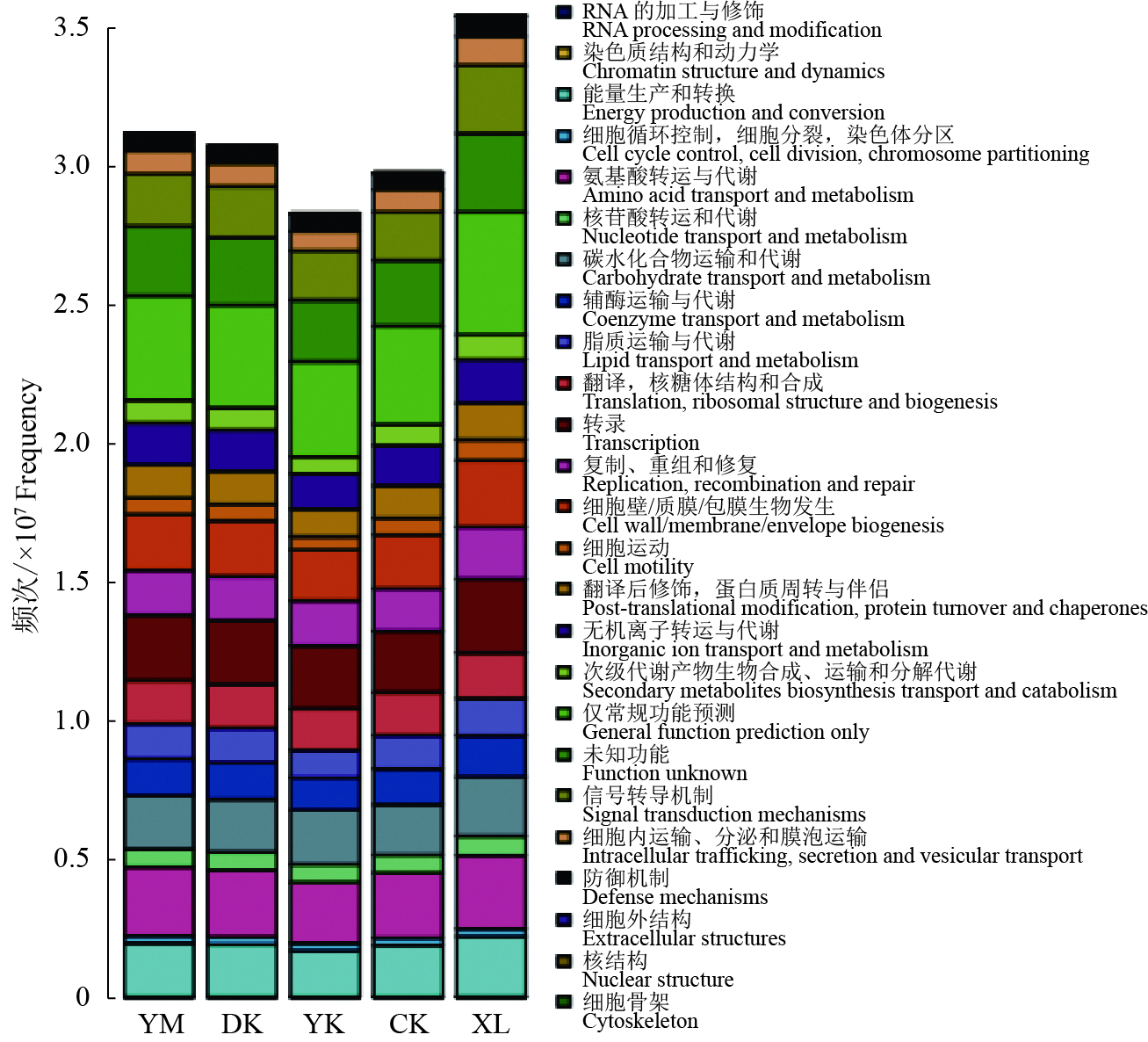
图 4 不同处理土壤细菌功能变化图
YM:老参地+玉米秸秆炭,DK:老参地+稻壳炭,YK:老参地+椰壳炭,CK:老参地,XL:新林土
Figure 4. Changes in soil bacterial function in different treatments
YM: Continuous cropping ginseng field+corn stalk biochar, DK: Continuous cropping ginseng field+rice husk biochar, YK: Continuous cropping ginseng field+coconut shell charcoal, CK: Continuous cropping ginseng field, XL: New forest soil
表 1 不同土壤样本序列数据统计与细菌群落Alpha多样性的差异
Table 1 Statistics of different soil sample sequence data and differences in Alpha diversity of bacterial communities
处理
Treatment高质量序列数
High quality sequence number占比/%
ProportionACE指数
ACE indexChao1指数
Chao1 indexShannon指数
Shannon index老参地+玉米秸秆炭
Continuous cropping ginseng field+corn stalk biochar72 646 98.02 4 651.70 3 719.71 5.48 老参地+稻壳炭
Continuous cropping ginseng field+rice husk biochar50 467 97.54 4 694.36 3 626.08 5.28 老参地+椰壳炭
Continuous cropping ginseng field+coconut shell biochar69 651 98.31 4 451.57 3 507.81 5.13 老参地 Continuous cropping ginseng field 56 868 98.09 3 861.62 2 893.23 5.00 新林土 New forest soil 54 219 97.38 5 412.14 5 134.09 7.05 总计 Total 303 851 97.90 表 2 不同处理土壤优势属组成、占比及OTUs1)
Table 2 Composition, proportion and OTUs of soil dominant genera in different treatments
% 处理
TreatmentMizugakiibacter Saccharibacteria_
genera_
incertae_sedisRhodanobacter Spartobacteria_
genera_
incertae_sedisGaiella Gemmatimonas Arthrobacter Afipia Rhizomicrobium Rudaea Sphingomonas YM 8.82
(5 075)6.00
(3 455)4.96
(2 856)3.72
(2 138)3.48
(2 004)3.39
(1 952)3.16
(1 818)2.91
(1 675)2.55
(1 470)2.52
(1 452)2.48
(1 426)DK 11.01
(4 918)5.65
(2 522)6.75
(3 016)4.72
(2 109)4.17
(1 864)2.78
(1 242)4.95
(2 212)— 2.34
(1 045)— 2.48
(1 107)YK 12.45
(7 059)8.77
(4 971)6.17
(3 500)6.42
(3 638)3.84
(2 176)3.97
(2 253)— — 2.16
(1 225)1.74
(986)1.78
(1 012)CK 12.08
(6 216)8.81
(4 535)7.36
(3 789)1.50
(773)3.05
(1 570)2.15
(1 107)1.96
(1 007)— 2.49
(1 280)— 1.66
(853)XL — — — 10.79
(4 914)1.90
(864)4.54
(2 067)— 2.58
(1 173)— — 5.26
(2 397)处理
TreatmentTerriglobus Pseudolabrys Gp1 Parcubacteria_
genera_
incertae_sedisRhodoplanes Luteibacter Marmoricola Nitrosospira Gp14 Arachidicoccus Gp2 YM 2.11
(1 217)1.89
(1 090)1.76
(1 015)1.63
(939)1.22
(702)— — — — — — DK 1.71
(762)1.27
(567)1.05
(467)— — — 1.73
(772)1.17
(524)— — — YK 2.31
(1 312)1.41
(797)1.05
(596)1.16
(657)1.33
(754)— — — — — — CK 2.23
(1 147)1.30
(668)— — — 2.67
(1 376)1.28
(659)1.26
(650)1.09
(563)1.02
(525)— XL — — 3.59
(1 637)— — — — — — — 2.18
(991)处理
TreatmentGp3 Gp4 Gp6 Gp7 WPS-1_
genera_
incertae_sedisMassilia Subdivision3_
genera_
incertae_sedisParalcaligenes Derxia YM — — — — — — — — — DK — — — — — — — 1.15
(515)— YK — — — — — — — — 1.27
(720)CK — — — — — — — — — XL 2.49
(1 133)3.28
(1 493)4.33
(1 971)1.48
(674)1.94
(882)1.04
(476)1.04
(472)— — 1) YM:老参地+玉米秸秆炭,DK:老参地+稻壳炭,YK:老参地+椰壳炭,CK:老参地,XL:新林土;括号内为OTUs;“—”表示未检出
1) YM: Continuous cropping ginseng field + corn stalk biochar, DK: Continuous cropping ginseng field + rice husk biochar, YK: Continuous cropping ginseng field + coconut shell biochar, CK: Continuous cropping ginseng field, XL: New forest soil; OTUs are given in brackets; “—”indicates undetectable -
[1] 奚广生. 不同土地利用方式下西洋参根际土壤养分与微生物特性研究[D]. 徐州: 中国矿业大学, 2020. [2] 李莉, 李东升, 赵晓松. 吉林省东部山区人参栽培基地土壤中微生物的生态分布[J]. 安徽农业科学, 2008, 36(31): 13729-13730. [3] ZORNOZA R, ACOSTA J A, FAZ A, et al. Microbial growth and community structure in acid mine soils after addition of different amendments for soil reclamation[J]. Geoderma, 2016, 272: 64-72. doi: 10.1016/j.geoderma.2016.03.007
[4] 陈晓天. 土壤改良剂及放线菌剂对镉(Cd)污染农田的修复作用研究[D]. 杨凌: 西北农林科技大学, 2020. [5] 刘文辉, 梁翔宇, 孙小涵, 等. 生物质炭作为土壤改良剂在农业上的应用研究进展[J]. 中国资源综合利用, 2020, 38(6): 108-110. [6] XIAO R, AWASTHI M K, LI R, et al. Recent developments in biochar utilization as an additive in organic solid waste composting: A review[J]. Bioresource Technology, 2017, 246(S1): 203-213.
[7] KAVITHA B, REDDY P V L, KIM B, et al. Benefits and limitations of biochar amendment in agricultural soils: A review[J]. Journal of Environmental Management, 2018, 227: 146-154.
[8] 吕玉德. 玉米秸秆生物炭对耕作土中硫形态转化及微生物群落结构的影响[D]. 兰州: 兰州交通大学, 2019. [9] LIU J, WU F Z, YANG Y. Effects of cinnamic acid on bacterial community diversity in rhizosphere soil of cucumber seedlings under salt stress[J]. Agricultural Sciences in China, 2010, 9(2): 266-274. doi: 10.1016/S1671-2927(09)60092-4
[10] ZHENG J, CHEN J, PAN G, et al. Biochar decreased microbial metabolic quotient and shifted community composition four years after a single incorporation in a slightly acid rice paddy from southwest China[J]. Science of the Total Environment, 2016, 571: 206-217. doi: 10.1016/j.scitotenv.2016.07.135
[11] DOMENE X, MATTANA S, HANLEY K, et al. Medium-term effects of corn biochar addition on soil biota activities and functions in a temperate soil cropped to corn[J]. Soil Biology & Biochemistry, 2014, 72: 152-162.
[12] ZHENG H, WANG X, LUO X, et al. Biochar-induced negative carbon mineralization priming effects in a coastal wetland soil: Roles of soil aggregation and microbial modulation[J]. Science of the Total Environment, 2018, 610: 951-960.
[13] MAESTRINI B, HERRMANN A M, NANNIPIERI P, et al. Ryegrass-derived pyrogenic organic matter changes organic carbon and nitrogen mineralization in a temperate forest soil[J]. Soil Biology & Biochemistry, 2014, 69: 291-301.
[14] KOLTON M, GRABER E R, TSEHANSKY L, et al. Biochar-stimulated plant performance is strongly linked to microbial diversity and metabolic potential in the rhizosphere[J]. New Phytologist, 2017, 213(3): 1393-1404. doi: 10.1111/nph.14253
[15] GE T, LIU C, YUAN H, et al. Tracking the photosynthesized carbon input into soil organic carbon pools in a rice soil fertilized with nitrogen[J]. Plant and Soil, 2015, 392(1/2): 17-25.
[16] NIELSEN S, MINCHIN T, KIMBER S, et al. Comparative analysis of the microbial communities in agricultural soil amended with enhanced biochars or traditional fertilisers[J]. Agriculture Ecosystems & Environment, 2014, 191(S1): 73-82.
[17] YE J, ZHANG R, NIELSEN S, et al. A combination of biochar-mineral complexes and compost improves soil bacterial processes, soil quality, and plant properties[J]. Frontiers in Microbiology, 2016, 7: 372. doi: 10.3389/fmicb.2016.00372.
[18] 应益昕. 人参连作对土壤微生物群落的影响研究[D]. 北京: 北京协和医学院, 2013. [19] BAIS H P, WEIR T L, PERRY L G, et al. The role of root exudates in rhizosphere interactions with plants and other organisms[J]. Annual Review of Plant Biology, 2006, 57: 233-266. doi: 10.1146/annurev.arplant.57.032905.105159
[20] 张婷婷. 增温及秸秆施用对豆−麦轮作土壤微生物群落结构的影响[D]. 南京: 南京信息工程大学, 2020.



 下载:
下载: