QTL analysis of low nitrogen tolerance in rice seedlings based on chromosome segment substitution lines
-
摘要:目的
通过定位与水稻Oryza sativa耐低氮相关的数量性状位点(QTL),为今后相关基因的精细定位、克隆以及功能研究奠定基础,也为耐低氮水稻品种的培育提供理论参考。
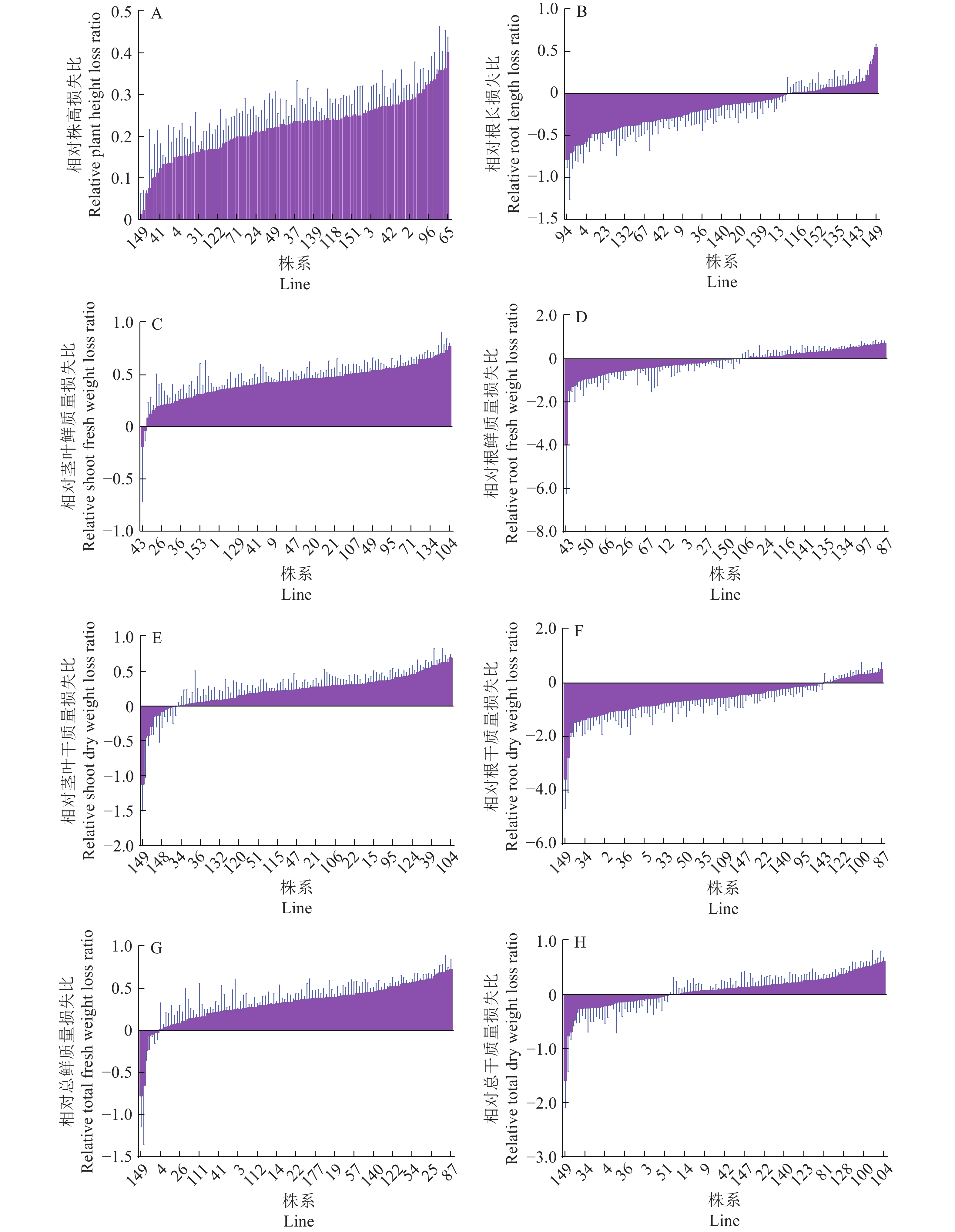
方法以Koshihikari (受体)和Nona Bokra (供体)为亲本构建的全基因组单片段代换系作为研究材料,在水稻苗期进行低氮胁迫处理,对水稻株高、根长、根鲜质量、根干质量、茎叶鲜质量、茎叶干质量、总鲜质量、总干质量共8个表型进行相对损失比分析和QTL定位。
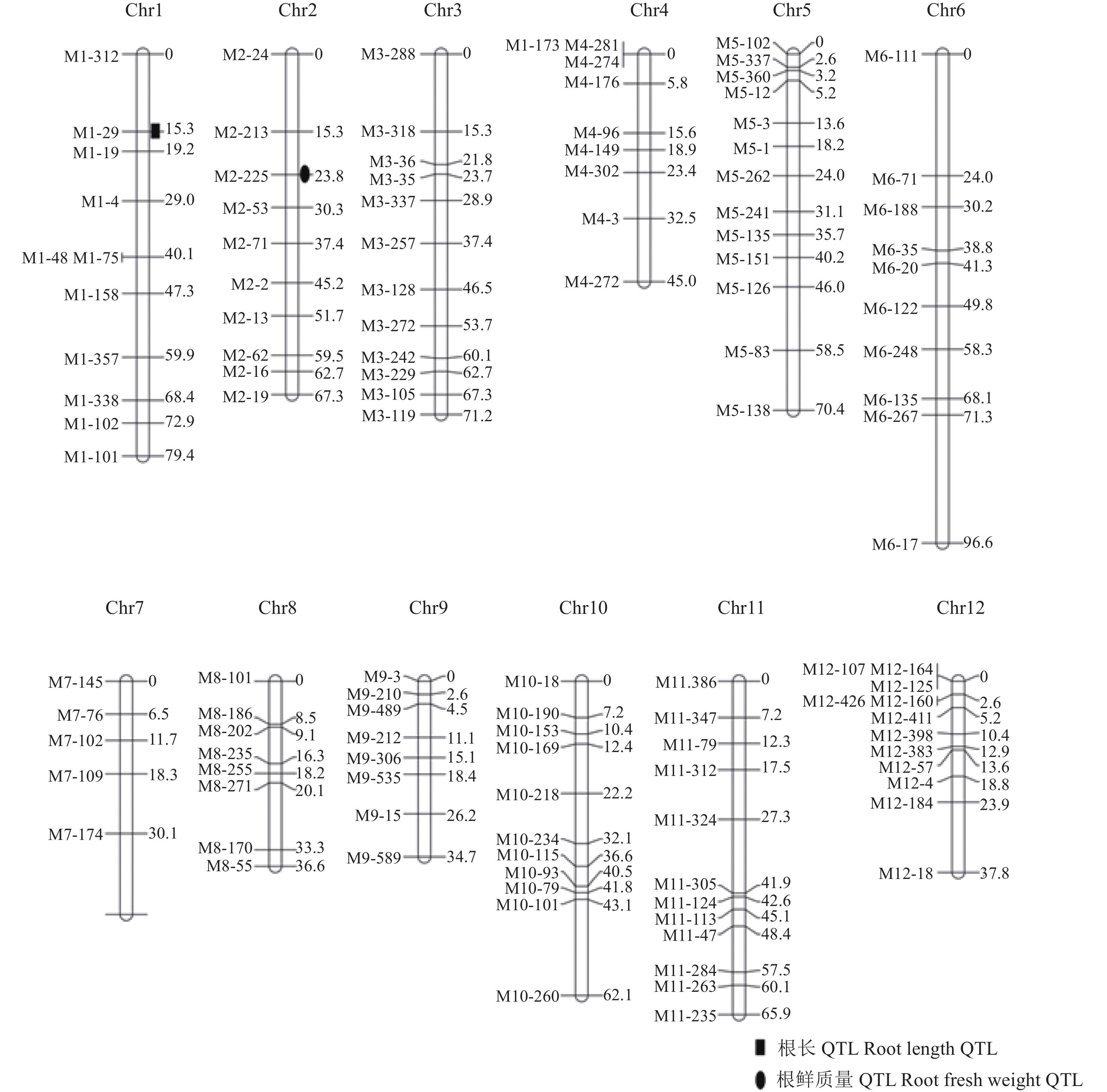
结果定位到2个与水稻低氮胁迫耐受相关的位点,分别是qRL1-1和qRFW2-1,这2个QTL位点分别在低氮胁迫下控制水稻根长和根鲜质量。其中,qRL1-1定位于1号染色体M1-29标记附近,LOD值为2.89,可解释的表型变异为11.23%;qRFW2-1定位于2号染色体M2-225标记附近,LOD值为2.53,可解释的表型变异为9.90%。其他6个表型未检测到相关位点。
结论初步定位了与低氮胁迫下控制水稻根长、根鲜质量相关基因,为进一步的基因精细定位奠定基础。
Abstract:ObjectiveTo map the quantitative trait loci (QTL) associated with low nitrogen tolerance in rice (Oryza sativa), provide a basis for future fine mapping, cloning and functional characterization of related genes and offer theoretical references for breeding of low nitrogen tolerant rice.
MethodA set of chromosomal segment substitution lines which was constructed by crossing Koshihikari (recurrent parent) and Nona Bokra (donor parent) were used as test materials. Low nitrogen stress treatment was applied at rice seedling stage. The relative loss ratios of eight phenotypes including rice plant height, root length, root fresh weight, root dry weight, shoot fresh weight, shoot dry weight, total fresh weight and total dry weight were analyzed, and QTL mapping was performed.
ResultTwo loci related to low nitrogen tolerance of rice were successfully mapped. These two QTLs were qRL1-1 and qRFW2-1 which were related to root length and root fresh weight respectively under low nitrogen stress. qRL1-1 was closed to the M1-29 marker on chromosome 1 with a LOD score of 2.89 and explained about 11.23% of total phenotypic variance. qRFW2-1 was closed to the M2-225 marker on chromosome 2 with a LOD score of 2.53 and explained about 9.90% of total phenotypic variance. No loci was found for other six phenotypic indexes.
ConclusionQTLs related to root length and root fresh weight under low nitrogen stress are mapped, which lays the foundation for further genetic fine mapping and cloning of the underlying genes.
-
球孢白僵菌Beauveria bassiana是目前研究较深入、应用广泛的一种昆虫病原真菌, 其致病性强、杀虫范围广, 在多种害虫的防治中取得了显著的经济、社会和生态效益[1]。我国曾大规模地应用球孢白僵菌防治马尾松毛虫Dendrolimus punctatus Walker, 并取得了巨大的成功[2-3]。球孢白僵菌也广泛应用于防治亚洲玉米螟Ostrinia furnacalis, 特别是我国东北地区利用白僵菌防治越冬代玉米螟成为玉米螟生物防治的重要方法[4-5]。
球孢白僵菌侵染寄主昆虫一般要经历分生孢子的附着、萌发与穿透表皮, 菌丝在血腔内生长、产生毒素、致死寄主、入侵所有器官继而穿出表皮, 产生新一代分生孢子、继续扩散流行等阶段。球孢白僵菌的致病机理不像化学农药那样依靠自身毒力杀死害虫, 而是通过吸收寄主体内水分和养分满足自身菌丝生长, 导致寄主体内生理代谢紊乱或代谢发生障碍而死亡。关于寄主昆虫对球孢白僵菌的免疫作用已有一些研究, 大腊螟Galleria mellonalla幼虫感染球孢白僵菌后在最佳条件和热激条件下产生不同的体液免疫能力[6]; 接种球孢白僵菌分生孢子对桑天牛Apriona germari幼虫血细胞数量有显著的影响[7]。对亚洲玉米螟幼虫注射不同剂量球孢白僵菌芽生孢子后, 其血细胞总数发生变化, 活体与离体血细胞均对芽生孢子产生包囊作用, 但是在活体条件下血细胞粘附在芽生孢子表面形成包囊, 而在离体条件下包囊形成的速度较慢, 其致密程度不如活体状态, 表明亚洲玉米螟对球孢白僵菌芽生孢子具有细胞防御能力[8]。膜翅目寄生蜂腰带长体茧蜂Macrocentrus cingulum是亚洲玉米螟的重要天敌, 腰带长体茧蜂的卵不会被亚洲玉米螟血细胞囊胞化, 因而可以在其体内完成发育, 这一现象说明寄主昆虫与寄生物具有复杂的免疫与抗免疫关系[9-10]。
亚洲玉米螟血细胞系SYSU-OfHe-C由中山大学胡建博士创建, 可连续继代培养[11]。本研究将考察球孢白僵菌对亚洲玉米螟血细胞SYSU-OfHe-C的毒性及其形态的影响, 进一步研究亚洲玉米螟幼虫与球孢白僵菌的免疫互作关系, 促进利用球孢白僵菌防治亚洲玉米螟生物防治技术的发展。
1. 材料与方法
1.1 材料
亚洲玉米螟幼虫血细胞系SYSU-OfHe-C由中山大学生命科学学院胡建博士馈赠。球孢白僵菌BbTS01菌株是华南农业大学天然农药与化学生物学教育部重点实验室从西藏日喀则市白朗县土壤中分离获得。
EX-CELL420培养基(美国Sigma公司); 胎牛血清(Gibco公司); MTT(南京凯基生物科技发展有限公司); CCK-8(日本同仁公司); 二甲基亚砜DMSO(美国Sigma公司); 吐温80(天津市富宇精细化工有限公司)。
酶标仪(iMark, 伯乐生命医学产品有限公司); 倒置显微镜(MF52型, 广州市明美光电技术有限公司); 96孔板(美国Corning Incorporated公司), 血球计数板(上海求精生化试剂仪器有限公司)。
1.2 方法
亚洲玉米螟幼虫血细胞系SYSU-OfHe-C采用EX-CELL420培养基添加φ为10%的胎牛血清, 27 ℃恒温培养, 每隔3~4 d传代1次, 取对数期细胞用于试验。球孢白僵菌BbTS01菌株取斜面菌种接种于PDA平板上培养约2周, 收集分生孢子。取分生孢子100 mg, 用2 g·L-1的吐温水1 mL配成悬浮液, 采用血球计数板计数, 调整浓度为107 mL-1备用。
1.2.1 球孢白僵菌对血细胞系SYSU-OfHe-C细胞的毒力测定
1) MTT法:96孔板每孔加入90 μL受试细胞悬浮液, 静置培养24 h, 待细胞浓度为1×105 mL-1时, 分别滴加10 μL球孢白僵菌分生孢子悬浮液, 使球孢白僵菌分生孢子终浓度分别达到3.5×106、3.5×105、3.5×104、3.5×103 mL-1, 以2 g·L-1吐温水为对照, 以不加细胞的完全培养基为本底, 每个处理重复4次。在27 ℃恒温培养箱中培养24 h后, 每孔加入50 μL的1×MTT, 27 ℃培养4 h, 吸出上清液(悬浮细胞用此法时经1 000 r·min-1离心后去除上清液), 每孔加入150 mL DMSO使甲臜溶解, 摇匀; 酶标仪测定波长处检测每孔的D490 nm。2) CCK-8法:细胞培养与处理方法同上述MTT法, 接种球孢白僵菌分生孢子并培养24 h后, 向每孔加入10 μL CCK-8溶液, 注意不形成气泡, 将培养板在培养箱内孵育1~4 h, 酶标仪测定D450 nm。
1.2.2 球孢白僵菌对血细胞系SYSU-OfHe-C细胞形态的影响
96孔板每孔加入90 μL受试细胞悬浮液, 静置24 h, 接种球孢白僵菌分生孢子悬浮液使其终浓度为3.5×104 mL-1, 倒置显微镜下监测球孢白僵菌与血细胞的生长情况, 每隔30 min拍照记录。取上述接种球孢白僵菌后培养24 h的亚洲玉米螟血细胞, 在光学显微镜与扫描电子显微镜下观察其形态变化, 并拍照记录。
1.3 数据处理
试验结果采用SPSS软件分析细胞死亡率, 改良寇氏法[12]计算IC50值。

式中, Xm为处理最大浓度的对数值; i为各浓度倍比浓度的对数值; ΣP为各组死亡率之和; 0.5为经验常数。
2. 结果与分析
2.1 球孢白僵菌对血细胞系SYSU-OfHe-C细胞的毒力测定
球孢白僵菌对SYSU-OfHe-C细胞的毒力测定结果见图 1, 不同浓度的球孢白僵菌分生孢子悬浮液处理24 h后, SYSU-OfHe-C细胞的死亡率不同, 随着球孢白僵菌分生孢子悬浮液浓度的增大, SYSU-OfHe-C细胞的死亡率增加, 总体上看, CCK-8法与MTT法的结果相差不大, 但前者测得的SYSU-OfHe-C细胞死亡率更高一点, 当球孢白僵菌分生孢子悬浮液浓度为3.5×106 mL-1, CCK-8法测得的SYSU-OfHe-C细胞死亡率达77.3%, MTT法为66.4%;球孢白僵菌分生孢子悬浮液浓度为3.5×103 mL-1, CCK-8法与MTT法的死亡率分别为15.2%和15.6%。CCK-8法与MTT法测得球孢白僵菌对SYSU-OfHe-C细胞的毒力回归方程见表 1, 从表 1可知MTT法测得球孢白僵菌分生孢子对SYSU-OfHe-C细胞的IC50(2.8×105 mL-1)稍高于CCK-8法的IC50(1.4×105 mL-1)。
表 1 球孢白僵菌对SYSU-OfHe-C细胞的毒力回归方程和IC50值Table 1. The toxicity regression equation and IC50 value of Beauveria bassiana against SYSU-OfHe-C cells
2.2 球孢白僵菌对血细胞系SYSU-OfHe-C细胞形态的影响
在光学显微镜下观察发现, 在接种球孢白僵菌分生孢子后, 大约10 h分生孢子萌发长出菌丝, 此后菌丝不断伸长, 亚洲玉米螟血细胞开始移动、数量变少且形态改变, 至24 h左右, 球孢白僵菌菌丝长满整个视野, 未见囊胞化与吞噬作用(图 2)。
接种球孢白僵菌分生孢子24 h后, SYSU-OfHe-C细胞部分从近似圆形变长或者变为不规则形状, 似乎还原成浆血细胞和类绛色细胞的原始形状, 但未见吞噬与囊胞化等细胞免疫现象发生。另外, 也发现少数SYSU-OfHe-C细胞聚集、破碎、细胞减少, 以及出现空泡和瘤状突起等现象(图 3)。在扫描电镜下还观察到球孢白僵菌菌丝穿透SYSU-OfHe-C细胞的现象(图 4)。
3. 讨论与结论
本研究运用MTT和CCK-8法测定了球孢白僵菌对SYSU-OfHe-C细胞的毒力, 结果有一定差异, 可能原因是:使用MTT法检测时, 需要使用裂解液溶解甲臜晶体沉淀, 可能遇到颗粒不完全溶解、吸取上清的操作中带走部分细胞等问题, 导致MTT法的结果容易出现细胞死亡率比实际情况偏低的情况; 而CCK-8是一种综合指标较好的细胞毒性检测试剂, 对细胞的毒性相当低, 其检测原理和检测条件与MTT法略有差异。CCK-8法产生的甲臜是水溶性的, 可以省去后续的溶解步骤, 减少一定的误差, 使试验结果更加稳定, 尽管当有还原物质存在时会影响CCK-8的测定, 但CCK-8法一般比MTT法更加灵敏、稳定, 而且重复性较好。
昆虫细胞免疫反应是由血细胞介导的, 主要依赖血细胞对外来异物的吞噬、集结和包囊[13]。包囊反应在昆虫细胞免疫反应中占有很重要的位置, 对昆虫细胞免疫反应的研究必定要进行囊胞化分析。本试验未发现亚洲玉米螟细胞系SYSU-OfHe-C对球孢白僵菌的囊胞化与吞噬作用等细胞免疫现象, 可能原因之一是SYSU-OfHe-C本身特性决定的, 其缺乏血浆的某些成份, 影响了其囊胞化效率[11]; 也与球孢白僵菌本身的特性有关, 球孢白僵菌是一种通过营养竞争策略使寄主昆虫生病的虫生真菌, 通过增加入侵量和快速分裂或生长来逃避寄主昆虫的免疫防御[14]; 也可能与血细胞的密度有关[15], 自然情况下, 亚洲玉米螟体内血细胞密度约为1.0×107~4.0×107 mL-1[9], 本研究采用细胞密度为1.0×105 mL-1, 低于亚洲玉米螟体内血细胞密度, 有可能造成SYSU-OfHe-C细胞囊胞化作用降低。
球孢白僵菌等微生物制剂的广泛应用是农业发展的重要方向, 亚洲玉米螟是我国重要的农业害虫, 生物因子在控制亚洲玉米螟种群数量方面起着十分重要的作用[16]。通过研究球孢白僵菌对亚洲玉米螟血细胞系SYSU-OfHe-C的毒力作用和对其细胞形态及生长的影响, 为进一步深入研究亚洲玉米螟幼虫与球孢白僵菌的免疫互作奠定基础, 有利于促进球孢白僵菌对亚洲玉米螟的生物防治。
-
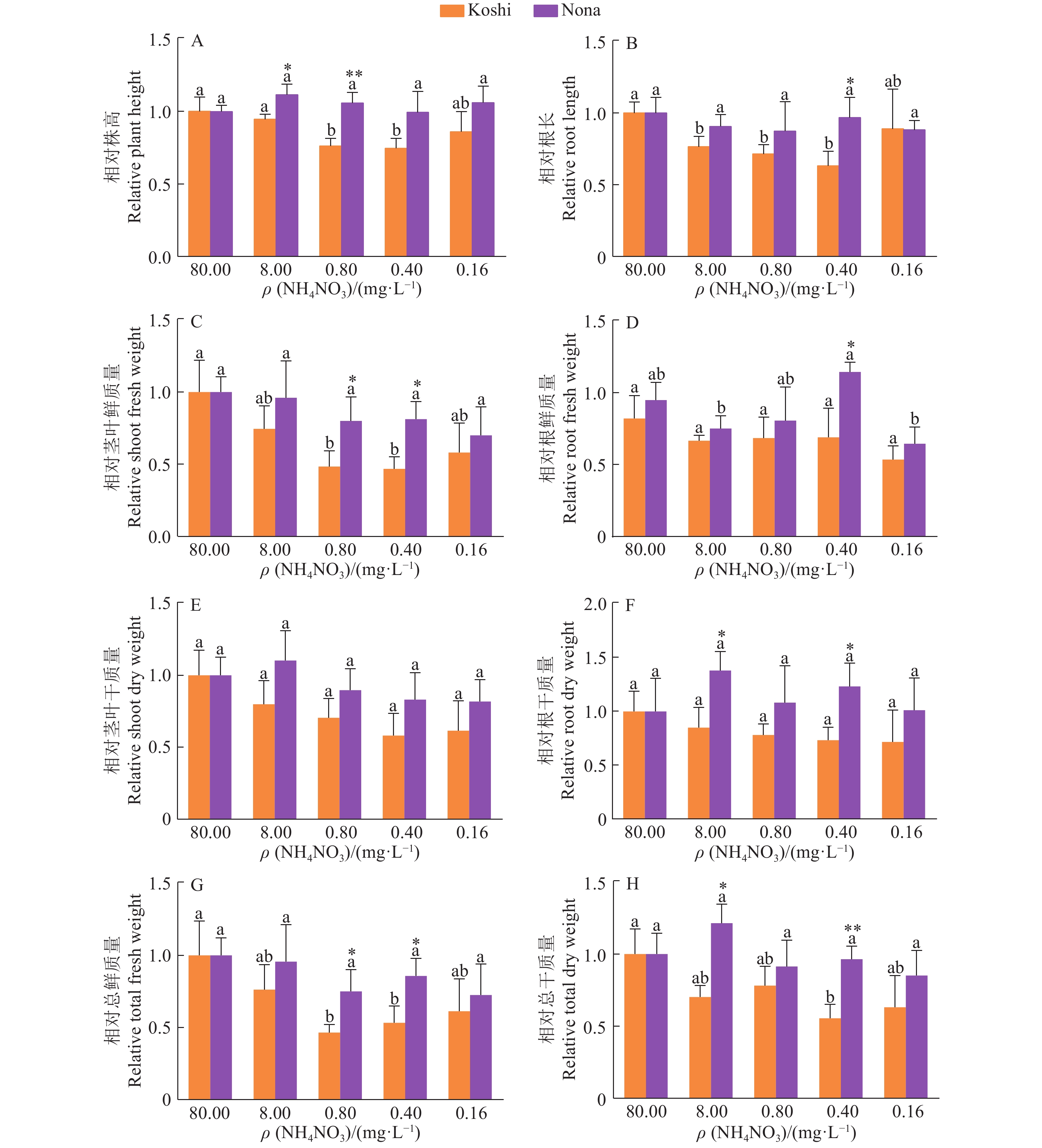
图 2 亲本合适低氮浓度筛选
各图中,相同颜色柱子上方的不同的小写字母表示Koshi或Nona组内差异显著(P<0.05, LSD法);“*” 和 “**”分别表示同一NH4NO3质量浓度的Koshi与Nona组间差异达到0.05和0.01的显著水平(t检验)
Figure 2. Selection of suitable low nitrogen level for parents
In each figure, different lowercase letters on bars of the same color indicate significant difference in Koshi or Nona group (P<0.05, LSD method); “*” and “**” represent significant difference between Koshi and Nona groups of the same NH4NO3 content at 0.05 and 0.01 levels respectively (t test)
表 1 亲本表型与氮素浓度相关性分析
Table 1 Correlation analysis between parental phenotype and nitrogen level
亲本
Parent表型
PhenotypePearson 相关系数1)
Pearson correlation coefficientP Koshi 株高 Plant height 0.732** 0.002 根长 Root length 0.776** 0.001 茎叶鲜质量 Shoot fresh weight 0.880** 0.000 根鲜质量 Root fresh weight 0.743** 0.002 茎叶干质量 Shoot dry weight 0.850** 0.000 根干质量 Root dry weight 0.666** 0.007 总鲜质量 Total fresh weight 0.873** 0.000 总干质量 Total dry weight 0.821** 0.000 Nona 株高 Plant height − 0.125 0.658 根长 Root length 0.775** 0.001 茎叶鲜质量 Shoot fresh weight 0.707** 0.003 根鲜质量 Root fresh weight 0.308 0.264 茎叶干质量 Shoot dry weight 0.707** 0.003 根干质量 Root dry weight 0.014 0.960 总鲜质量 Total fresh weight 0.652** 0.008 总干质量 Total dry weight 0.029 0.918 1) “*” 和 “**” 分别表示在 0.05 和 0.01 水平显著相关
1) “*” and “**” represent significant correlation at 0.05 and 0.01 levels respectively表 2 低氮胁迫下SN代换系群体表型分析
Table 2 Analysis of the phenotypes in the chromosomal segment substitution lines of SN population under low nitrogen stress
表型 Phenotype 对照 (80.00 mg/L NH4NO3)
Control低氮处理(0.40 mg/L NH4NO3)
Low N treatment平均值
Mean变异范围
Variation range变异系数/%
Variation coefficient平均值
Mean变异范围
Variation range变异系数/%
Variation coefficient株高/cm Plant height 43.886 28.500~56.766 9.61 33.690 26.333~43.200 9.96 根长/cm Root length 21.648 17.433~28.433 11.30 25.317 18.900~33.333 12.68 茎叶鲜质量/g Shoot fresh weight 0.613 0.446~0.817 13.15 0.326 0.223~0.496 14.33 根鲜质量/g Root fresh weight 0.170 0.135~0.231 13.11 0.178 0.135~0.242 14.73 茎叶干质量/g Shoot dry weight 0.094 0.075~0.113 11.68 0.073 0.047~0.094 14.16 根干质量/g Root dry weight 0.020 0.015~0.025 13.28 0.034 0.025~0.043 14.67 总鲜质量/g Total fresh weight 0.099 0.077~0.131 10.80 0.076 0.053~0.101 13.36 总干质量/g Total dry weight 0.111 0.075~0.146 14.31 0.105 0.076~0.128 13.82 表 3 低氮胁迫相关性状的QTL位点分析
Table 3 Analysis of QTL identified trait related to low nitrogen tolerance
性状
Trait数量性状位点
QTL染色体编号
Chr. number标记
MarkerLOD 加性效应
Additive effect可解释的表型变异/%
PVE根长 Root length qRL1-1 1 M1-29 2.89 −0.15 11.23 根鲜质量 Root fresh weight qRFW2-1 2 M2-225 2.53 −0.31 9.90 -
[1] 许学宏, 王红慧. 肥料对农产品品质的影响综述[J]. 磷肥与复肥, 2003(4): 66-68. doi: 10.3969/j.issn.1007-6220.2003.04.026 [2] 顾骏飞, 周振翔, 李志康, 等. 水稻低叶绿素含量突变对光合作用及产量的影响[J]. 作物学报, 2016, 42(4): 551-560. [3] BACON P E. Nitrogen fertilization in the environment[J]. Biol Rev, 1995, 32(3): 296-348.
[4] 邓若磊. 水稻铵转运蛋白基因OsAMT1.4和OsAMT5的克隆、表达和遗传转化[D]. 保定: 河北农业大学, 2007. [5] SUN H, QIAN Q, WU K, et al. Heterotrimeric G proteins regulate nitrogen-use efficiency in rice[J]. Nat Genet, 2014, 46(6): 652-657. doi: 10.1038/ng.2958
[6] YANAGISAWA S, AKIYAMA A, KISAKA H, et al. Metabolic engineering with Dof1 transcription factor in plants: Improved nitrogen assimilation and growth under low-nitrogen conditions[J]. P Natl Acad Sci USA, 2004, 101(20): 7833-7838. doi: 10.1073/pnas.0402267101
[7] SHAN Y H, WANG Y L, PAN X B. Mapping of QTLs for nitrogen use efficiency and related traits in rice (Oryza sativa L.)[J]. Agr Sci China, 2005, 4(10): 721-727.
[8] 王彦荣, 代贵金, 大杉立, 等. 水稻苗期氮素吸收及其相关性状的QTL分析[J]. 中国水稻科学, 2010, 24(5): 463-468. doi: 10.3969/j.issn.1001-7216.2010.05.003 [9] 方萍, 陶勤南, 吴平. 水稻吸氮能力与氮素利用率的QTLs及其基因效应分析[J]. 植物营养与肥料学报, 2001(2): 159-165. doi: 10.3321/j.issn:1008-505X.2001.02.007 [10] YOSHIDA S, FORNO D A, COCK J H, et al. Laboratory manual for physiological studies of rice[M]. 2nd ed. Los Banos: IRRI, 1972: 57-63.
[11] WANG J K, WAN X Y, CROSSA J, et al. QTL mapping of grain length in rice (Oryza sativa L.) using chromosome segment substitution lines[J]. Genet Res, 2006, 88(2): 93-104. doi: 10.1017/S0016672306008408
[12] MCCOUCH S R, CHO Y G, YANO M, et al. Report on QTL nomenclature[J]. Rice Genet Newsl, 1997, 14: 11-13.
[13] 王玉雯, 郭九信, 孔亚丽, 等. 氮肥优化管理协同实现水稻高产和氮肥高效[J]. 植物营养与肥料学报, 2016, 22(5): 1157-1166. [14] CHOUDHURY A, KENNEDY I R. Nitrogen fertilizer losses from rice soils and control of environmental pollution problems[J]. Commun Soil Sci Plant, 2005, 36(11/12): 1625-1639.
[15] 阮成江, 何祯祥, 钦佩. 我国农作物QTL定位研究的现状和进展[J]. 植物学通报, 2003(1): 10-22. doi: 10.3969/j.issn.1674-3466.2003.01.002 [16] 吕海霞, 周广生, 丁泽红, 等. 水稻染色体片段代换系对氮反应的QTL分析[J]. 分子植物育种, 2010, 8(6): 1074-1081. doi: 10.3969/mpb.008.001074 [17] GEIOFF G C. Intact-plant screening for tolerance of nutrient deficiency stress[J]. Plant Soil, 1987, 99(1): 3-16. doi: 10.1007/BF02370149
[18] 梁永书, 周军杰, 南文斌, 等. 水稻根系研究进展[J]. 植物学报, 2016, 51(1): 98-106. [19] LIU K, HE A, YE C, et al. Root morphological traits and spatial distribution under different nitrogen treatments and their relationship with grain yield in super hybrid rice[J]. Sci Rep, 2018, 8(1): 131-139. doi: 10.1038/s41598-017-18576-4
[20] 赵春芳, 赵凌, 张亚东, 等. 水稻苗期耐低氮相关性状的QTL定位[J]. 华北农学报, 2015, 30(6): 1-7. [21] FENG Y, CAO L Y, WU W M, et al. Mapping QTLs for nitrogen-deficiency tolerance at seedling stage in rice (Oryza sativa L.)[J]. Plant Breeding, 2010, 129(6): 652-656. doi: 10.1111/j.1439-0523.2009.01728.x
[22] CHO Y I, JIANG W, CHIN J H, et al. Identification of QTLs associated with physiological nitrogen use efficiency in rice[J]. Mol Cells, 2007, 23(1): 72-79.




 下载:
下载: