Assessment of multi-function of Pinus tabulaeformis plantation in Qingyang area
-
摘要:目的
研究陇东地区甘肃省庆阳市油松人工林多功能发挥情况,构建评价模型,为该地区森林经营提供科学依据。
方法以庆阳市油松人工林为研究对象,在下属7县选取63块样地进行调查,采用层次分析法构建多功能评价指标体系,从油松人工林涵养水源、固碳放氧、生物多样性保护和优质种源保存4种功能中筛选11项评价指标,结合调查数据和专家打分的方式确定各指标权重,计算各样地的多功能贡献总分,采用正态等距划分将处于不同地区的油松林多功能评价指标划分为5个等级。
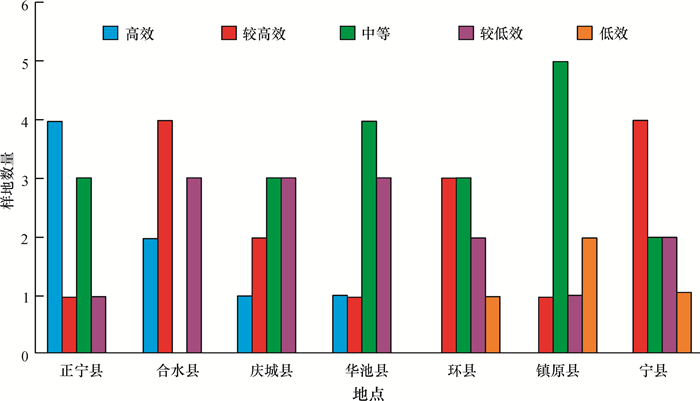
结果庆阳地区油松人工林多功能发挥水平最高的是水源涵养功能,其次是生物多样性保护功能;固碳放氧功能和优良种源保存功能发挥水平偏低。油松人工林多功能发挥高效、较高效、中效、较低效和低效的比例分别为12.7%、25.4%、31.75%、25.4%和4.76%,总体多功能发挥一般,发挥最好的地区是正宁县,最差的地区为镇原县。
结论运用层次分析法能有效进行森林多功能评价,应采取经营抚育措施提高庆阳市森林多功能的发挥。
Abstract:ObjectiveTo investigate the multi-function of Pinus tabulaeformis plantation in Qingyang, Gansu Province, establish an evaluation system, and provide a scientific basis for the forest management in Qingyang area.
MethodWe surveyed 63 sample plots of P. tabulaeformis plantations from seven counties of Qingyang, and used analytic hierarchy process(AHP) to establish the multi-function evaluation index system. Eleven indexes were chosen from four functions including water conservation, carbon fixation and oxygen release, biodiversity conservation and excellent provenance preservation. The weights of different indexes were determined using the surveyed data and expert scoring. The total scores for multi-functions of different sample plots were calculated. Using normal equidistant partition, evaluation indexes of plantations of different counties were divided into five categories.
ResultFor the P. tabulaeformis plantation in Qingyang, the water conservation function had the highest effect, followed by the biodiversity protection function. The functions of carbon fixation and oxygen release and excellent provenance preservation had relatively low effect. The proportions of sample plots that had high effect, moderate high effect, medium effect, moderate low effect and low effect for their multi-functions were 12.7%, 25.4%, 31.75%, 25.4% and 4.76% respectively. The performance was the best in Zhengning County and the worst in Zhenyuan County. The overall effect of multi-function of P. tabulaeformis plantation in Qianyang was ordinary.
ConclusionAHP can be used to effectively evaluate forest multi-function. We should take management measures to improve the multi-function of Qingyang forests.
-
随着我国工业化快速发展,土壤重金属污染越发严重[1]。重金属污染影响植物的生长、产量和品质,甚至会通过食物链迁移到人体内威胁人类健康[2-3]。镉(Cd)污染作为重金属污染的头号元凶,对其研究的紧迫性日益剧增。Cd是作物生长的限制因素,会降低植物体内的叶绿素含量,进而影响正常光合作用[4];还会诱发高活性氧自由基,导致植物由于过氧化而提前衰老[5]。Cd对植株的毒害程度取决于多方面因素,包括植物种类、Cd浓度和Cd胁迫时间等。丁海东等[6]发现1 µmol/L低浓度Cd溶液能提高番茄种子发芽势,2 mmol/L的高浓度Cd溶液会降低种子发芽势、发芽率,抑制根的生长;Ederli等[7]研究表明100 µmol/L Cd浓度胁迫下芦苇根结构没有明显变化;周全等[8]研究发现Cd质量分数高于0.5 mg/kg时12个水稻品种的苗高均显著下降,干物质量和叶绿素含量等也受到明显影响;Gzyl等[9]的结果同样证明了类似的观点。由此可见,不同植物对Cd胁迫的反应不同,有必要在不同植物上进行Cd处理研究。
Cd毒害不但显著抑制植物生长,还会影响植物对必需营养元素的吸收及营养元素在植物体内的有效性。He等[10]研究发现,Cd敏感型水稻突变体的总根长及根表面积会随Cd溶液浓度的增加而增加,导致根系对Cd的吸收量比野生型更高;有研究发现Cd抑制重金属超积累植物地上部对锌(Zn)、铁(Fe)和锰(Mn)的吸收以及根部对Fe、Mn的吸收[11];此外,Cd处理会显著降低甘蓝叶中Fe、Mn、镁(Mg)含量以及根中Mn含量[12]。这些研究表明植物的耐Cd能力可能与植物必需营养元素吸收有重要联系,目前相关报道还较少。
大豆Glycine max L.是世界上重要的粮食作物、油料作物和饲料来源,营养价值极高,富含蛋白质、氨基酸、脂肪和多种矿物质[13]。同时,大豆是Cd毒害敏感作物,在受Cd污染的土壤中生长的大豆的多种农艺性状都表现出毒害症状[14-15]。因此,Cd污染会严重影响大豆生产,研究大豆对Cd胁迫的响应十分重要。本研究以对Cd敏感程度不同的4种基因型大豆作为材料,研究不同浓度的Cd胁迫处理对大豆种子萌发、植株生长及元素积累的影响,从大豆根系性状以及体内元素积累和分配的角度解析不同基因型大豆Cd敏感性存在差异的原因,筛选耐Cd基因型用于大豆育种。
1. 材料与方法
1.1 供试材料
材料为4种基因型大豆:‘巴西10号’、‘本地2号’、‘桂夏豆2号’和‘华夏3号’。试验所用土壤来自华南农业大学增城教学科研基地,土壤基本理化性状参见文献[16]。所用石英砂均是商业购买,分粗砂和中砂。
1.2 营养液
营养液采用改良版大豆砂培1/2 Hoagland营养液,母液(1 000 ×)具体配方:252.76 g/L KNO3、43.57 g/L K2SO4、590.38 g/L Ca(NO3)2·4H2O、246.47 g/L MgSO4·7H2O、29.40 g/L Fe-EDTA(Na)、0.89 g/L MnCl2·4H2O、0.09 g/L ZnSO4·7H2O、0.04 g/L CuSO4·5H2O、0.20 g/L (NH4)6Mo7O24·4H2O、68.05 g/L KH2PO4和1.24 g/L H3BO3,pH 5.8~6.0。种子萌发培养基配方:1/2 Hogland营养液、10 g/L蔗糖、3 g/L琼脂粉。
1.3 方法
1.3.1 试验设计
Cd对大豆种子萌发影响的试验在培养室进行,设置不同Cd浓度的萌发培养基,镉质量分数分别为0(对照)、2、11、23、46、114、228 mg/kg CdCl2·5/2H2O,每个处理3次重复,每皿播6粒种子。不同基因型大豆Cd处理盆栽试验在网室大棚进行,设置3种Cd质量分数处理,分别为0(对照)、10、20 mg/kg CdCl2·5/2H2O,每个处理4次重复。
1.3.2 测定指标及方法
在大豆主根生长试验中,挑选4种基因型大豆饱满无伤痕的种子,置于培养皿内,单层排列,打开培养皿,放入干燥器中,将干燥器放入通风橱中。干燥器中放入烧杯,烧杯中加入100 mL次氯酸钠,然后沿着杯壁缓慢加入4.2 mL盐酸,次氯酸钠和盐酸反应产生氯气,盖上干燥器盖子,用氯气消毒10 h。之后打开干燥器盖子,盖上培养皿盖,拿出培养皿放在超净工作台内,打开培养皿盖通风约30 min,除去多余的氯气以免影响种子生长。将消毒后的种子种脐向下播种在培养基中,置于24 ℃培养室中光照培养。5 d后拍照,用尺子量主根长,记录数据。
盆栽试验采用砂土培。石英砂用清水冲洗干净后,121 ℃灭菌40 min,间隔24 h后重复灭菌1次,土壤与石英砂采用相同灭菌方式,然后将石英砂与土壤按照质量比4︰1的比例混匀。称取CdCl2·5/2H2O配置0(CK)、10、20 mg/kg Cd溶液,按比例倒入砂土混合基质中混匀,静置平衡20 d后装盆,每盆装2 kg混合砂土。大豆种子用氯气熏蒸灭菌后,每盆播3颗饱满健康的种子,浇适量营养液,出苗后每盆挑选生长一致的大豆植株保留1株。每周补充1次营养液,45 d后收获,测定植株生物量、根系性状和元素浓度等指标。根系用自来水冲洗干净后,用台式扫描仪(Epson 1460XL)扫描根系,用根系分析软件WinRHIZO (Regent Instruments Inc., 加拿大)分析总根长和根表面积。植株地上部与根系样品分别烘干粉碎称质量后,经马福炉在550 ℃条件下灰化8 h,用原子吸收分光光度计测定Cd、钙(Ca)、Mg、Fe、铜(Cu)、Zn、Mn和钾(K)的浓度,磷(P)浓度用钼锑抗比色法测定。
1.4 数据分析
试验数据均采用Microsoft Excel 2010 (Microsoft Company,美国)软件和SPSS 18.0进行数据处理和双因素方差分析,采用Duncan’s法对不同Cd处理或基因型进行多重比较。
2. 结果与分析
2.1 Cd处理对不同基因型大豆主根生长的影响
Cd处理极显著影响大豆主根生长(P<0.001),并且不同基因型大豆的主根长对加Cd处理的反应也存在极显著差异(P<0.001)(表1)。由图1a可知,与对照相比,2 mg/kg Cd处理下4种基因型大豆主根长有增加的趋势;随着Cd浓度增加,从11 mg/kg开始,主根长的伸长逐渐受到抑制,23 mg/kg时‘巴西10号’、‘本地2号’、‘桂夏豆2号’和‘华夏3号’主根长分别比对照下降了50%、20%、37%和50%;114、228 mg/kg Cd处理时4种基因型大豆的主根长均受到严重抑制,比对照减少1倍以上。同时Cd对不同基因型的抑制程度有所不同,‘华夏3号’的耐Cd能力较好,在11 mg/kg Cd处理下,主根长与对照相比没有明显变化,其他基因型均受到明显抑制;在Cd质量分数≥46 mg/kg处理下,所有基因型主根长均受到严重抑制。
![图 1 Cd处理对不同基因型大豆主根长和生物量的影响]() 图 1 Cd处理对不同基因型大豆主根长和生物量的影响各小图中相同Cd浓度处理柱子上方的不同小写字母表示不同基因型大豆间差异显著(P < 0.05,Duncan’s法)Figure 1. Effects of Cd treatments on taproot lengths and biomasses of different soybean genotypesDifferent lowercase letters on the columns of the same Cd concentration treatment in each figure indicate significant differences among different soybean genotypes (P < 0.05,Duncan’s method)表 1 Cd处理对不同基因型大豆生长指标影响的双因素方差分析Table 1. Two-way ANOVA of effects of Cd treatment on growth indicators of different soybean genotypes
图 1 Cd处理对不同基因型大豆主根长和生物量的影响各小图中相同Cd浓度处理柱子上方的不同小写字母表示不同基因型大豆间差异显著(P < 0.05,Duncan’s法)Figure 1. Effects of Cd treatments on taproot lengths and biomasses of different soybean genotypesDifferent lowercase letters on the columns of the same Cd concentration treatment in each figure indicate significant differences among different soybean genotypes (P < 0.05,Duncan’s method)表 1 Cd处理对不同基因型大豆生长指标影响的双因素方差分析Table 1. Two-way ANOVA of effects of Cd treatment on growth indicators of different soybean genotypes指标
IndexF 1) Cd处理
Cd treatment基因型
GenotypeCd处理×基因型
Cd treatment × Genotype主根长 Taproot length 120.06*** 11.68*** 2.47*** 生物量 Biomass 392.05*** 39.85*** 5.39*** 总根长 Total root length 762.59*** 20.36*** 5.19*** 根表面积 Root surface area 338.72*** 13.56*** 2.86* 地上部Cd浓度 Cd concentration of shoot 86.24*** 4.02* 1.90 根部Cd浓度 Cd concentration of root 198.65*** 30.80*** 12.75*** 地上部P浓度 P concentration of shoot 22.66*** 15.24*** 4.90*** 地上部K浓度 K concentration of shoot 211.23*** 22.77*** 5.44*** 地上部Ca浓度 Ca concentration of shoot 15.64*** 0.53 4.35** 地上部Mg浓度 Mg concentration of shoot 5.52** 13.55*** 0.27 地上部Fe浓度 Fe concentration of shoot 9.70*** 2.47 5.36*** 地上部Cu浓度 Cu concentration of shoot 53.64*** 9.87*** 8.15*** 地上部Zn浓度 Zn concentration of shoot 13.95*** 5.50** 2.04 地上部Mn浓度 Mn concentration of shoot 37.53*** 19.26*** 6.06*** 根部P浓度 P concentration of root 19.83*** 21.56*** 10.51*** 根部K浓度 K concentration of root 74.33*** 6.07** 12.51*** 根部Ca浓度 Ca concentration of root 0.26 2.01 4.20** 根部Mg浓度 Mg concentration of root 1.33 13.51*** 2.34 根部Fe浓度 Fe concentration of root 3.57* 5.11** 2.73* 根部Cu浓度 Cu concentration of root 18.92*** 4.06* 2.99* 根部Zn浓度 Zn concentration of root 10.26*** 7.58*** 3.73** 根部Mn浓度 Mn concentration of root 49.00*** 4.63** 3.96** 1) “*”表示P< 0.05,“**”表示P< 0.01,“***”表示P< 0.001(双因素方差分析)
1)“*” indicates P< 0.05,“**” indicatesP< 0.01,“***” indicatesP< 0.001(Two-way ANOVA)2.2 Cd处理对不同基因型大豆生物量的影响
Cd处理极显著影响大豆的生物量(P<0.001),并且不同基因型大豆的生物量也存在极显著差异(P<0.001)(表1)。由图1b可知,与对照相比,4种基因型大豆的生物量均随着Cd浓度的增加明显下降。在10、20 mg/kg Cd处理后,‘巴西10号’生物量分别比对照减少86%、84%,‘本地2号’减少74%、76%,‘桂夏豆2号’减少53%、56%,‘华夏3号’减少59%、70%。4种基因型大豆的耐Cd能力存在显著差异,不加Cd时,‘巴西10号’、‘本地2号’、‘桂夏豆2号’的生物量无显著差异,均显著低于‘华夏3号’;在10 mg/kg Cd处理下,4种基因型大豆的生物量差异显著,表现为‘巴西10号’<‘本地2号’<‘桂夏豆2号’<‘华夏3号’;在20 mg/kg Cd处理下,‘华夏3号’与‘桂夏豆2号’生物量无显著差异,均显著高于‘巴西10号’和‘本地2号’。结果表明,Cd会抑制植株正常生长,Cd处理后4种基因型大豆的生物量存在显著差异,‘华夏3号’和‘桂夏豆2号’的耐Cd能力显著优于‘巴西10号’和‘本地2号’。
2.3 Cd处理对不同基因型大豆根系性状的影响
Cd处理极显著影响大豆的总根长和根表面积(P<0.001),并且不同基因型大豆的总根长和根表面积也存在极显著差异(P<0.001)(表1)。由图2可知,4种基因型大豆总根长和根表面积随着Cd浓度的增加逐渐下降。与对照相比,‘巴西10号’的总根长在10、20 mg/kg Cd处理下均减少90%以上,‘华夏3号’分别减少66%和80%。不加Cd时,‘本地2号’和‘华夏3号’的总根长显著高于‘巴西10号’和‘桂夏豆2号’,‘本地2号’和‘华夏3号’之间差异不显著;‘华夏3号’的根表面积显著高于‘本地2号’和‘桂夏豆2号’。在10 mg/kg Cd处理下,‘华夏3号’的总根长和根表面积显著高于‘本地2号’和‘桂夏豆2号’,‘本地2号’和‘桂夏豆2号’之间无显著差异,‘巴西10号’的总根长和根表面积均显著低于其他3种基因型。在20 mg/kg Cd处理下,‘华夏3号’的总根长显著高于‘巴西10号’和‘本地2号’,‘华夏3号’和‘桂夏豆2号’之间无显著差异;‘桂夏豆2号’和‘华夏3号’的根表面积显著高于‘巴西10号’和‘本地2号’。
![图 2 Cd处理对不同基因型大豆总根长和根表面积的影响]() 图 2 Cd处理对不同基因型大豆总根长和根表面积的影响各小图中相同Cd浓度处理柱子上方的不同小写字母表示不同基因型大豆间差异显著(P < 0.05,Duncan’s法)Figure 2. Effects of Cd treatments on total root length and root surface area of different soybean genotypesDifferent lowercase letters on the columns of the same Cd concentration treatment in each figure indicate significant differences among different soybean genotypes (P < 0.05,Duncan’s method)
图 2 Cd处理对不同基因型大豆总根长和根表面积的影响各小图中相同Cd浓度处理柱子上方的不同小写字母表示不同基因型大豆间差异显著(P < 0.05,Duncan’s法)Figure 2. Effects of Cd treatments on total root length and root surface area of different soybean genotypesDifferent lowercase letters on the columns of the same Cd concentration treatment in each figure indicate significant differences among different soybean genotypes (P < 0.05,Duncan’s method)2.4 Cd处理对不同基因型大豆Cd浓度的影响
Cd处理极显著影响大豆地上部和根部Cd浓度(P<0.001),并且不同基因型大豆地上部Cd浓度对存在显著差异(P<0.05),根部Cd浓度存在极显著差异(P<0.001)(表1)。由图3可知,大豆根部的Cd浓度远高于地上部。与对照相比,在10、20 mg/kg处理下,4种基因型大豆的地上部和根部Cd浓度均增加了10倍以上。不加Cd时,‘本地2号’和‘华夏3号’地上部Cd浓度显著低于‘巴西10号’和‘桂夏豆2号’,同时‘巴西10号’和‘桂夏豆2号’,以及‘本地2号’和‘华夏3号’均无显著差异;‘桂夏豆2号’根部Cd浓度显著高于‘本地2号’和‘华夏3号’,与‘巴西10号’差异不显著。在10 mg/kg Cd处理下,‘本地2号’地上部Cd浓度显著高于‘桂夏豆2号’和‘华夏3号’,与‘巴西10号’差异不显著;‘巴西10号’根部Cd浓度显著低于‘本地2号’和‘华夏3号’,与‘桂夏豆2号’无显著差异。在20 mg/kg Cd处理下,4种基因型大豆地上部Cd浓度无显著差异;‘巴西10号’的根部Cd浓度最低,‘本地2号’最高,‘华夏3号’和‘桂夏豆2号’无显著差异。
![图 3 Cd处理对不同基因型大豆Cd浓度的影响]() 图 3 Cd处理对不同基因型大豆Cd浓度的影响各小图中相同Cd浓度处理柱子上方的不同小写字母表示不同基因型大豆间差异显著(P < 0.05,Duncan’s法)Figure 3. Effects of Cd treatments on Cd concentrations of different soybean genotypesDifferent lowercase letters on the columns of the same Cd concentration treatment in each figure indicate significant differences among different soybean genotypes (P < 0.05,Duncan’s method)
图 3 Cd处理对不同基因型大豆Cd浓度的影响各小图中相同Cd浓度处理柱子上方的不同小写字母表示不同基因型大豆间差异显著(P < 0.05,Duncan’s法)Figure 3. Effects of Cd treatments on Cd concentrations of different soybean genotypesDifferent lowercase letters on the columns of the same Cd concentration treatment in each figure indicate significant differences among different soybean genotypes (P < 0.05,Duncan’s method)2.5 Cd处理对不同基因型大豆营养元素浓度的影响
由表2可知,Cd处理显著影响不同基因型大豆地上部各种营养元素的浓度。与对照相比,4种基因型大豆地上部P、K、Cu、Fe浓度在2种Cd浓度胁迫处理下均有增加的趋势。在10 mg/kg Cd处理下,‘本地2号’地上部Ca浓度比对照显著增加,‘华夏3号’地上部Ca浓度比对照显著降低;在20 mg/kg Cd处理下,‘巴西10号’、‘桂夏豆2号’和‘华夏3号’地上部Ca浓度均比对照显著降低。在10 mg/kg Cd处理下,‘巴西10号’、‘本地2号’和‘桂夏豆2号’地上部Zn浓度比对照显著增加。10 mg/kg Cd处理下‘巴西10号’地上部Mn浓度比对照显著降低,20 mg/kg Cd处理下‘本地2号’、‘桂夏豆2号’和‘华夏3号’地上部Mn浓度比对照显著增加。
表 2 Cd处理对不同基因型大豆地上部营养元素浓度影响Table 2. Effects of Cd treatments on nutrient element concentrations in shoots of different soybean genotypes基因型
Genotypew(Cd)/
(mg·kg−1)w/(g·kg−1) w/(mg·kg−1) P K Ca Mg Fe Cu Zn Mn 巴西10号
Baxi No. 100 0.58±0.02b 20.91±0.66b 13.14±0.38a 3.37±0.11a 71.09±6.63b 6.11±1.09c 36.52±1.75b 21.07±1.90a 10 2.01±0.41a 45.45±2.06a 14.43±1.21a 4.11±0.69a 84.07±23.62ab 12.41±1.15b 55.24±3.62a 12.25±2.06b 20 1.89±0.08a 46.02±2.78a 10.34±0.77b 3.84±0.14a 143.02±48.14a 17.86±1.75a 53.95±7.92a 15.96±3.53ab 本地2号
Bendi No. 20 1.21±0.03a 17.11±0.37b 11.39±1.02b 4.49±0.46a 112.91±12.88b 6.05±0.52c 30.01±2.23b 23.05±2.68b 10 1.43±0.07a 32.22±0.98a 15.01±0.75a 5.35±0.32a 152.91±18.41a 16.80±2.61a 47.14±1.96a 24.86±1.02b 20 1.47±0.19a 35.95±1.18a 12.01±1.13ab 5.15±0.61a 126.43±2.78ab 11.88±1.00b 37.33±2.75b 48.84±3.74a 桂夏豆2号
Guixiadou No. 20 0.71±0.06b 23.78±0.71b 13.26±0.26a 3.30±0.10b 80.33±8.39b 5.99±0.68c 31.66±2.11b 21.38±1.86b 10 1.11±0.03a 38.93±1.29a 12.46±0.55a 3.79±0.08a 192.72±17.03a 11.61±0.59a 45.98±3.00a 23.56±0.46b 20 1.07±0.13a 38.10±1.49a 10.76±0.17b 3.72±0.17a 84.47±6.45b 8.22±0.55b 32.74±0.19b 40.24±4.55a 华夏3号
Huaxia No. 30 0.63±0.02b 23.52±0.85c 14.22±0.31a 3.38±0.07b 98.88±13.58b 5.96±0.61b 38.16±3.19a 27.35±1.70b 10 0.95±0.05a 32.28±0.38b 12.19±0.25b 3.99±0.04a 128.75±26.92ab 9.47±0.28a 40.73±5.99a 21.60±0.76b 20 0.94±0.06a 36.60±1.32a 11.23±0.34b 3.96±0.12a 169.07±24.23a 10.68±1.20a 35.58±1.70a 41.09±5.71a 1) 数据为平均值±SE;相同基因型同列数据后的不同小写字母表示不同Cd处理浓度间差异显著(P< 0.05,Duncan’s法)
1)The datum is mean±SE; Different lowercase letters in the same column and genotype indicate significant differences among different Cd treating concentrations (P< 0.05,Duncan’s test)由表3可知,Cd对不同基因型大豆根部营养元素浓度有很大影响。在 20 mg/kg Cd处理下,4种基因型大豆根部Mn浓度均比对照显著增加。结合表1可知,除Ca以外,根部营养元素浓度在基因型之间差异显著。与对照相比,在2种Cd处理下‘巴西10号’根部P、K、Zn浓度显著增加,根部Ca浓度显著降低;‘本地2号’根部K浓度比对照显著增加;‘桂夏豆2号’根部Cu浓度比对照显著增加。
表 3 Cd处理对不同基因型大豆根部营养元素浓度的影响1)Table 3. Effects of Cd treatments on nutrient element concentrations in roots of different soybean genotypes基因型
Genotypew(Cd)/
(mg·kg−1)w/(g·kg−1) w/(mg·kg−1) P K Ca Mg Fe Cu Zn Mn 巴西10号
Baxi No. 100 0.77±0.03b 27.03±1.01b 12.25±0.59a 4.06±0.19a 914.90±144.91b 13.45±1.71b 46.60±2.38b 10.04±0.89b 10 1.65±0.21a 38.62±1.46a 7.81±0.97b 3.26±1.02a 1 302.15±91.69a 16.48±6.69b 96.91±1.02a 13.90±1.79b 20 1.30±0.18a 34.78±1.63a 9.68±0.97b 2.87±0.20a 1 080.64±122.55ab 30.84±5.09a 85.39±13.22a 21.18±2.41a 本地2号
Bendi No. 20 0.64±0.04b 30.80±0.80c 9.06±0.22a 1.88±0.10b 1 403.30±172.15a 17.07±1.91b 57.32±4.75a 13.00±1.68b 10 0.97±0.07a 34.69±0.15b 8.74±1.89a 2.63±0.23a 1 525.43±158.69a 43.79±12.26a 82.65±20.22a 11.59±1.20b 20 1.07±0.03a 41.33±1.35a 7.82±0.96a 3.01±0.08a 1 189.80±142.57a 29.48±3.18ab 74.67±8.29a 31.94±3.01a 桂夏豆2号
Guixiadou No. 20 0.82±0.02b 28.66±0.76b 8.88±0.43b 4.34±0.14a 1 150.17±125.49a 10.27±0.64b 44.51±2.29b 13.45±1.86b 10 0.85±0.05ab 24.49±1.62c 10.53±0.78a 4.67±0.31a 1 158.35±189.60a 28.82±3.20a 66.85±1.61a 17.29±2.36ab 20 0.93±0.04a 40.78±0.96a 9.25±0.56ab 3.96±0.06a 1 476.97±144.46a 38.28±11.14a 49.94±2.04ab 20.86±1.72a 华夏3号
Huaxia No. 30 0.88±0.09a 28.59±2.59b 7.61±0.22b 4.46±0.30a 880.46±47.58b 13.56±1.37b 60.01±4.00a 13.05±1.78b 10 0.75±0.06a 31.44±0.14b 10.03±0.54a 4.35±0.26a 1 111.47±71.84ab 24.78±5.94ab 47.31±1.87a 11.26±0.41b 20 0.88±0.03a 40.13±1.78a 9.24±0.69ab 3.30±0.33b 1 242.21±90.77a 26.99±4.14a 54.81±3.57a 19.50±1.80a 1) 数据为平均值±SE;相同基因型同列数据后的不同小写字母表示不同Cd处理浓度间差异显著(P< 0.05,Duncan’s法)
1)The datum is mean±SE; Different lowercase letters in the same column and genotype indicate significant differences among different Cd treating concentrations (P< 0.05,Duncan’s test)3. 讨论与结论
Cd是危害作物生长发育的重金属元素,当植物体内Cd的累积量达到一定程度时便会对植物产生毒害作用。种子萌发作为植物生长的起始阶段,对外界环境胁迫最为敏感,变化特征反映了植物对Cd胁迫的耐受能力[17]。主根长通常用于衡量种子萌发后幼苗的生长状况。杜兰芳等[18]研究发现Cd胁迫对豌豆幼苗根长具有明显的抑制作用,且随着Cd浓度的增加,抑制作用逐渐增强;李冬等[19]发现在低浓度(10 µmol/L) Cd处理下,豌豆幼苗的主根长降低了65.20%。本研究培养基萌发试验结果表明不同基因型对Cd的耐受能力存在差异。相比于不加Cd对照,在2 mg/kg (相当于10 µmol/L) Cd处理下大豆主根长有增加的趋势;在大于11 mg/kg Cd处理下,除‘华夏3号’以外,其余基因型大豆主根的生长均受到明显抑制;在Cd质量分数大于23 mg/kg时,4种基因型大豆主根长均受到严重抑制;这一结果与前期研究[6]结果一致。‘华夏3号’耐Cd性优于其他基因型,说明不同基因型的耐Cd性存在差异[20-21]。
Cd胁迫下植物生物量和籽粒产量都会有明显下降[22];本研究的盆栽试验也发现,加Cd处理后4种基因型大豆的植株生物量均显著降低。Cd处理下‘桂夏豆2号’和‘华夏3号’的生物量显著高于‘巴西10号’和‘本地2号’,表明‘巴西10号’、‘本地2号’的植株生长对Cd敏感,属于Cd敏感基因型;‘桂夏豆2号’、‘华夏3号’比较耐Cd,属于耐Cd基因型,且‘华夏3号’的耐Cd能力显著高于‘巴西10号’;这一结果与Wang等[23]的研究结果一致。根系是植物吸收土壤中水分和营养元素的重要器官,可作为预防Cd进入植物体内的屏障[24-26]。有研究表明Cd可以通过抑制细胞分裂、养分吸收等抑制根系生长,耐性强的品种一般表现为根系生物量大、根长较长[24-25]。本研究中,加Cd处理后4种基因型大豆的总根长和根表面积均显著降低,耐Cd能力强的‘华夏3号’和‘桂夏豆2号’的根系生长发育比‘巴西10号’更好,具有更大的总根长和根表面积。由此可见,耐Cd能力不同是引起不同基因型根系性状的差异的主要原因之一。
在土壤Cd含量相同的条件下,大豆各器官的Cd含量存在显著差异,一般表现为根部>地上部[27-28]。本研究4种基因型大豆根部Cd浓度也都远远高于地上部,表明植物会把从土壤中吸收的Cd保留在根部,阻止过多的Cd转移到地上部对植株光合作用造成影响[29]。进一步观察胁迫条件下不同基因型之间的根部Cd浓度发现‘华夏3号’显著高于‘巴西10号’,说明耐Cd能力强的基因型根部对Cd的积累量更高,只有较少的Cd转移到地上部,这和张芬琴[30]的研究结果一致。此外,本研究在不加Cd处理的植株中也检测到Cd元素,这主要是由于本试验使用砂土混合物作为培养介质,土壤本身含有微量的Cd,但并不影响大豆的正常生长。从植株Cd累积量来看,黄运湘等[31]研究发现,在全Cd质量分数为0.10 mg/kg、有效Cd质量分数为0.04 mg/kg的红壤和河潮土上分别种植大豆,不加Cd处理时植株体内单株Cd累积量分别为5.33和5.00 µg,大豆没有出现任何Cd胁迫症状,这个Cd累积量与本研究不加Cd处理的大豆植株体内Cd累积量(单株2.03~5.19 µg)相当,间接证明混合砂土中土壤Cd含量没有达到影响大豆生长的阈值。
植物体内存在营养元素的平衡,Cd过量时会打破这种平衡。在Cd进入植物体的过程中,会与其他养分元素竞争转运的结合位点,从而引起植物体内元素浓度的改变,尤其会与一些二价金属如Ca2+、Fe2+、Mn2+和Zn2+等产生相互作用,影响这些有益元素的吸收[26, 32]。本研究中,相比于不加Cd处理,加Cd后植物体内的营养元素浓度发生了显著变化,尤其是地上部P、K、Cu、Fe浓度呈现一致上升的趋势。研究发现Cd胁迫抑制秋华柳根部Ca的吸收和积累[33]。本试验发现在10 mg/kg Cd处理下,Cd敏感基因型‘本地2号’地上部Ca浓度呈增加趋势,耐Cd基因型‘华夏3号’呈降低趋势;Cd敏感基因型‘巴西10号’根部Ca浓度显著降低,耐Cd基因型‘华夏3号’、‘桂夏豆2号’呈增加趋势。此外,研究发现Cd和Zn在大豆籽粒中表现为协同作用,在叶片中表现为拮抗作用[34],本试验中Cd胁迫处理下Cd敏感基因型‘巴西10号’地上部和根部Zn浓度均显著增加。Cd敏感与耐Cd基因型大豆在Cd处理后Ca、Zn浓度变化趋势有明显差异。以上结果表明,Cd处理后植株体内营养元素浓度变化明显,但变化的趋势并不一致,没有表现出一致的与Cd协同或拮抗的作用,这与前期研究结果[35]类似,具体机制还有待进一步研究。
综上所述,Cd胁迫显著抑制不同基因型大豆主根生长和植株生长,不同基因型的耐Cd能力表现不同。‘巴西10号’和‘本地2号’是Cd敏感基因型,‘桂夏豆2号’和‘华夏3号’属于耐Cd基因型。耐Cd基因型大豆主要通过根系生长和体内元素浓度变化缓解Cd毒害。
致谢: 党鹏在外业调查、土壤理化性质的测试以及数据分析中给予了帮助, 庆阳市各林业局的工作人员在试验的布设和调查中也给予了帮助,在此一并致谢! -
表 1 庆阳市油松人工林多功能评价指标体系
Table 1 Multi-function evaluation index system of Pinus tabularformis plantations in Qingyang
目标层(A) 准则层(B) 指标层(C) 编号 指标 编号 指标 油松人工林多功能评价 B1 水源涵养功能 C1 郁闭度 C2 枯落物厚度 C3 土壤厚度 C4 土壤孔隙度 C5 坡度 B2 固碳放氧功能 C6 林龄 C7 森林生物量 B3 生物多样性保护功能 C8 林下植被种类 C9 林下植被盖度 B4 优良种源保存功能 C10 单位面积蓄积量 C11 幼苗数量 表 2 专家打分矩阵1)
Table 2 The expert scoring matrix
A B1 B2 B3 B4 Wi B1 1 7 5 9 0.640 B2 1/7 1 7 7 0.144 B3 1/5 1/7 1 1 0.176 B4 1/9 1/7 1 1 0.041 1) CR=0.096 7,λmax=4.258 3。 B1 C1 C2 C3 C4 C5 Wi C1 1 3 5 8 8 0.498 C2 1/3 1 3 5 8 0.261 C3 1/5 1/3 1 3 7 0.144 C4 1/8 1/5 1/3 1 3 0.063 C5 1/8 1/8 1/7 1/3 1 0.034 1) CR=0.070 6,λmax=5.316 3。 表 3 庆阳市油松人工林多功能评价指标权重
Table 3 The weights of multi-function evaluation indexes of Pinus tabidaeformis plantations in Qingyang
目标层 准则层 分层权重 指标层 分层权重 指标权重 A B1 0.640 C1 0.498 0.318 C2 0.261 0.167 C3 0.144 0.092 C4 0.063 0.041 C5 0.034 0.022 B2 0.144 C6 0.167 0.037 C7 0.833 0.021 B3 0.176 C8 0.722 0.127 C9 0.278 0.049 B4 0.041 C10 0.722 0.030 C11 0.278 0.011 表 4 油松人工林多功能快速评价指标等级划分标准
Table 4 The grading standard of multi-function evaluation indexes of Pinus tabularformis plantations in Qingyang
评价指标1) 不同等级划分标准 好 较好 中等 较差 差 C1 [60, 80) ≥80 [40, 60) [20, 40) < 20 C2 ≥4 [3, 4) [2, 3) [1, 3) < 1 C3 ≥60 [50, 60) [40, 50) [30, 40) < 30 C4 [45, 65) [40, 45); [65, 70) [35, 40); [70, 75) [30, 35); [75, 80) < 30; ≥80 C5 ≥5 [5, 15) [15, 25) [25, 35) < 35 C6 [25, 35) [20, 25); [35, 40) [15, 20); [40, 50) [10, 15); [50, 60) [1, 10); ≥60 C7 ≥120 [90, 120) [60, 90) [30, 60) < 30 C8 ≥20 [15, 20) [10, 15) [5, 10) < 5 C9 ≥70 [50, 70) [30, 50) [10, 30) < 10 C10 ≥80 [60, 80) [40, 60) [20, 40) < 20 C11 ≥2 000 [1 600, 2 000) [1 200, 1 600) [8000, 1 200) < 800 1) C1为郁闭度(%),C2为枯落物厚度(cm),C3为土壤厚度(cm),C4为土壤孔隙度(%),C5为坡度(°),C6为林龄(a),C7为森林生物量(m3·hm-2),C8为林下植被种类(种),C9为林下植被盖度(%),C10为单位面积蓄积量(m3·hm-2),C11为幼苗数量(个·hm-2)。 表 5 样地多功能评价结果
Table 5 The evaluation scores of multi-functions of sample plots
样地编号1) 水源涵养功能 固碳放氧功能 生物多样性保护功能 优良种源保存功能 总贡献得分 P1 40.615 2.366 10.566 2.000 55.546 P2 41.046 1.952 13.110 2.000 58.106 P3 38.390 3.114 10.566 2.227 54.297 P4 49.885 3.114 9.001 2.227 64.227 P5 50.316 3.863 10.566 3.045 67.789 P6 55.924 4.277 14.088 2.681 76.971 P7 63.104 5.440 8.022 3.045 79.611 P8 60.448 5.440 8.022 3.863 77.773 P9 62.724 5.440 10.566 3.863 82.593 P10 37.713 1.952 10.566 2.000 52.230 P11 33.621 1.952 13.110 2.000 50.682 P12 40.666 2.700 9.588 1.409 54.362 P13 50.316 3.529 9.001 2.227 65.072 P14 47.845 3.863 10.566 3.045 65.319 P15 52.592 4.277 14.088 2.454 73.411 P16 63.104 5.026 4.500 3.045 75.675 P17 51.178 5.026 8.022 3.863 68.088 P18 57.719 5.026 10.566 3.045 76.355 P19 39.179 4.611 8.022 3.045 54.857 P20 39.558 1.952 13.110 2.000 56.619 P21 29.068 1.952 13.110 2.000 46.129 P22 38.390 3.114 11.544 1.636 54.684 P23 44.512 3.114 11.544 2.227 61.398 P24 47.414 3.863 10.566 3.045 64.888 P25 47.414 3.863 13.110 2.454 66.840 P26 51.557 5.026 7.044 3.045 66.672 P27 57.546 5.026 9.588 3.272 75.431 P28 40.666 5.026 10.566 3.045 59.302 P29 39.558 1.952 10.566 1.636 53.712 P30 30.914 1.952 13.110 2.000 47.974 P31 38.390 3.114 9.001 2.227 52.732 P32 44.512 3.114 11.544 2.227 61.398 P33 47.414 3.863 10.566 3.045 64.888 P34 47.414 3.863 13.110 2.454 66.840 P35 48.225 5.026 7.044 3.045 63.339 P36 57.115 5.026 9.588 3.272 75.000 P37 28.258 1.952 13.110 1.409 44.728 P38 30.914 1.952 14.088 2.000 48.953 P39 38.390 3.114 9.588 2.227 53.318 P40 44.512 3.114 10.566 2.227 60.420 P41 47.414 3.863 10.566 3.045 64.888 P42 47.414 3.863 10.566 2.454 64.297 P43 54.593 4.611 7.044 2.454 68.703 P44 51.178 5.026 9.588 2.681 68.472 P45 53.403 4.611 10.566 3.045 71.625 P46 29.499 1.952 13.110 1.409 45.969 P47 26.412 1.952 11.544 2.000 41.908 P48 37.713 3.114 11.544 2.227 54.599 P49 44.512 3.114 11.544 2.227 61.398 P50 44.758 4.277 10.566 3.045 62.646 P51 47.414 3.863 10.566 2.454 64.297 P52 48.225 4.611 7.044 2.227 62.107 P53 51.178 4.611 9.588 2.681 68.058 P54 46.603 4.611 10.566 2.818 64.598 P55 29.499 1.952 13.110 1.409 45.969 P56 28.258 3.114 11.544 2.000 44.916 P57 40.615 1.952 9.588 2.227 54.381 P58 44.512 3.863 11.544 2.227 62.146 P59 45.569 4.277 10.566 2.818 63.230 P60 50.747 3.863 10.566 2.227 67.402 P61 48.225 5.026 9.588 2.227 65.065 P62 49.332 4.611 9.588 2.681 66.212 P63 46.603 4.611 13.110 3.045 67.369 1) 正宁县样地编号为P1~P9,合水县样地编号为P10~P18,庆城县样地编号为P19~P27,华池县样地编号为P28~P36,环县样地编号为P37~P45,镇原县样地编号为P46~P54,宁县样地编号为P55~P63。 -
[1] HARRISON P, VANDEWALLE M, SYKES M, et al. Identifying and prioritising services in European terrestrial and freshwater ecosystems[J]. Biodivers and Conserv, 2010, 19(10): 2791-2821. doi: 10.1007/s10531-010-9789-x
[2] 王兵, 魏文俊, 冷泠.宁夏六盘山不同森林类型土壤贮水与入渗研究[J].内蒙古农业大学学报(自然科学版), 2006, 27(3):1-5. http://www.cnki.com.cn/Article/CJFDTOTAL-NMGM200603000.htm [3] 赵红宇.林业在生态建设中的特殊地位[J].内蒙古林业调查设计, 2011, 34(6):6. http://www.cnki.com.cn/Article/CJFDTOTAL-NMLD201106005.htm [4] 侯元兆, 王琦.中国森林资源核算研究[J].世界林业研究, 1995(3):51-56. http://www.cnki.com.cn/Article/CJFDTOTAL-GTLH201411004.htm [5] LOVELL S, MENDEZ V, ERICKSON D, et al. Extent, pattern, and multi-functionality of treed habitats on farms in Vermont, USA[J]. Agroforest Syst, 2010, 80(2): 153-171. doi: 10.1007/s10457-010-9328-5
[6] 李金良, 郑小贤.北京地区水源涵养林健康评价指标体系的探讨[J].林业资源管理, 2004(1): 31-34. http://www.cnki.com.cn/Article/CJFDTOTAL-LYZY200401007.htm [7] 鲁绍伟, 余新晓, 刘凤芹, 等.北京市八达岭林场森林生态系统健康性评价[J].水土保持学报, 2006, 20(3): 79-82. http://www.cnki.com.cn/Article/CJFDTOTAL-TRQS200603019.htm [8] 赵学明, 刘东兰, 郑小贤.北京八达岭林场森林多功能评价指标体系探讨[J].林业资源管理, 2010(3):45-48. http://www.cnki.com.cn/Article/CJFDTOTAL-LYZY201003010.htm [9] 蔡永茂, 许兰霞, 张咏.八达岭林场的分类经营评价[J].北京林业大学学报, 2003, 25(12): 57-62. http://www.cnki.com.cn/Article/CJFDTOTAL-BJLY2003S1014.htm [10] 朱绍文, 张立, 孙春林.八达岭林场森林资源价值评估及生态效益经济补偿的初步探讨[J].北京林业大学学报, 2003, 25(12): 71-74. http://www.cnki.com.cn/Article/CJFDTOTAL-BJLY2003S1017.htm [11] COSTANZA R, D′ARGE R, DE GROOT R. The value of the world's ecosystem services and natural capital[J].Nature, 1997, 387(15): 253-260. http://mro.massey.ac.nz/handle/10179/5983
[12] COSTANZA R. Ecosystem services: Multiple classification systems are needed[J]. Biol Conserv, 2008, 141(2): 350-352. doi: 10.1016/j.biocon.2007.12.020
[13] 殷鸣放, 郑小贤, 殷炜达.森林多功能评价与表达方法[J].东北林业大学学报, 2012, 40(6):23-26. http://www.cnki.com.cn/Article/CJFDTOTAL-DBLY201206008.htm [14] 张永利, 杨锋伟, 王兵, 等, 中国森林生态系统服务功能研究[M].北京:科学出版社, 2010. [15] 周彬. 太岳山油松林人工林水文特征研究[D]. 北京: 北京林业大学, 2013. [16] 鲍文, 包维楷, 丁德蓉, 等.岷江上游人工油松林凋落量及其持水特征[J].西南农业大学学报(自然科学版), 2004, 26(5):567-571. http://www.cnki.com.cn/Article/CJFDTOTAL-XNND200405014.htm [17] 莫菲, 于澎涛, 王彦辉, 等.六盘山华北落叶松林和红桦林枯落物持水特征及其截持降雨过程[J].生态学报, 2009, 29(6) :2868-2876. http://www.cnki.com.cn/Article/CJFDTOTAL-STXB200906015.htm [18] 杨学军, 姜志林.溧阳地区森林景观的生物多样性评价[J].生态学报, 2001, 21(4):671-675. http://www.cnki.com.cn/Article/CJFDTOTAL-STXB200104025.htm [19] 贾振声, 骆永菊, 徐文权.关于正态分布的等距分组[J].数学的实践与认识, 2010, 40(20):238-244. http://www.cnki.com.cn/Article/CJFDTOTAL-YBSF201005005.htm [20] 王礼先.水土保持学[M].北京:中国林业出版社, 1995:10-15. [21] 彭道黎, 张志华, 靳云燕.北京市生态公益林经营目标及指标体系的研究[J].林业调查规划, 2006, 31(6):16-19. http://www.cnki.com.cn/Article/CJFDTOTAL-LDGH200606003.htm [22] 张邦文, 欧阳杰, 金苏蓉, 等.兴国县飞播马尾松林多功能经营评价[J].林业科技开发, 2014, 28(1):50-54. http://cdmd.cnki.com.cn/Article/CDMD-10410-1013130755.htm [23] 张彦雷. 山西太岳山油松人工林多功能快速评价研究[D]. 北京: 北京林业大学, 2014.




 下载:
下载: