Stability analysis of internal reference gene of Ricinus communis treated by glucose-fipronil
-
摘要:目的
筛选葡萄糖基氟虫腈(GTF)及溶剂二甲基亚砜(DMSO)处理下蓖麻Ricinus communis稳定的内参基因,为研究GTF的韧皮部装载机制提供参考。
方法选取Actin,ARC,ef1a,SamDC,TUA6为内参基因,通过实时荧光定量PCR分析基因表达量并利用geNorm,NormFinder,BestKeeper,Delta CT软件及RefFinder在线分析工具综合比较不同时间和不同浓度的GTF与DMSO处理后,5个候选内参基因在蓖麻幼苗子叶中表达的稳定性。
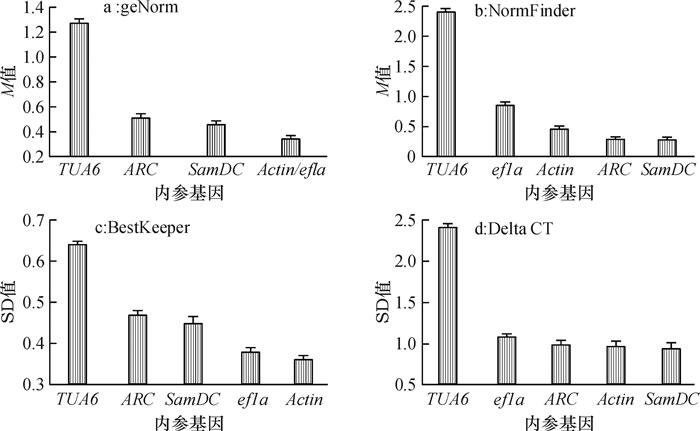
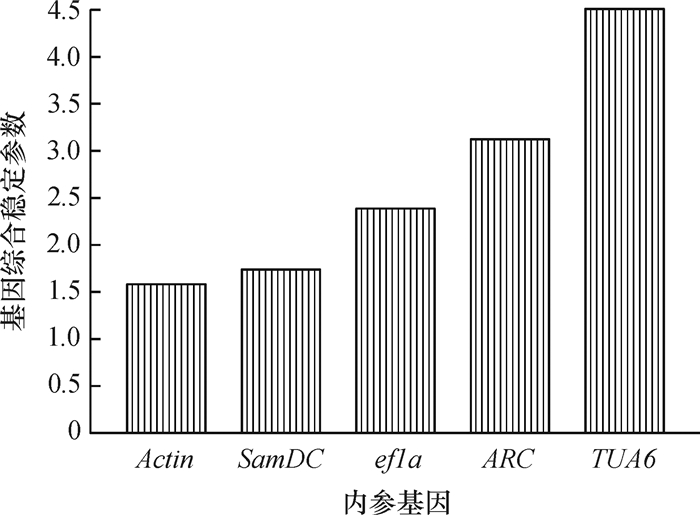
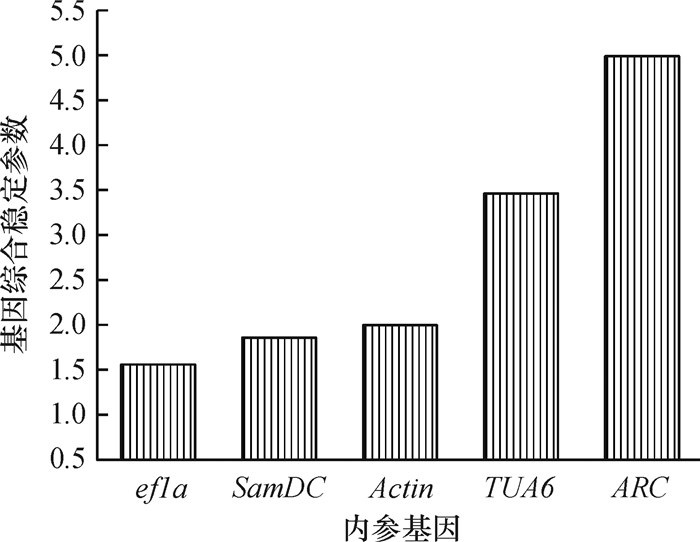
结果各软件分析得出的内参基因稳定性排名依次为geNorm:Actin=ef1a > SamDC > ARC > TUA6;NormFinder:SamDC > ARC > Actin > ef1a > TUA6; BestKeeper:Actin > ef1a > SamDC > ARC > TUA6;Delta CT:SamDC > Actin > ARC > ef1a > TUA6; RefFinder:Actin > SamDC > ef1a > ARC > TUA6,而单独分析DMSO处理时,稳定性排名则为:ef1a > SamDC > Actin > TUA6 > ARC。
结论综合分析GTF和DMSO处理,Actin的表达最稳定;在DMSO处理下,则ef1a最为稳定。
Abstract:ObjectiveTo screen reliable internal reference genes of castor, Ricinus communis, treated by glucose-fipronil (GTF) and the solvent dimethyl sulfoxide (DMSO), and to provide a basis for studying the uptake mechanism of GTF.
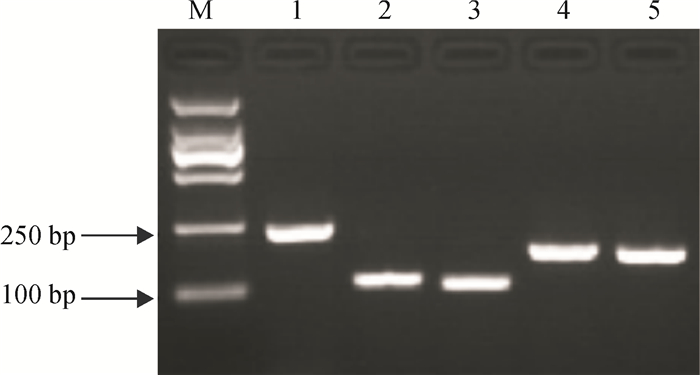
MethodActin, ARC, ef1a, SamDC and TUA6 genes were selected as candidate reference genes. Specific primers for each gene were designed and real-time quantitative PCR was conducted. Five softwares, including geNorm, NormFinder, BestKeeper, Delta CT and RefFinder, were employed to analyze the gene expression stabilities in cotyledon of castor seedlings treated by GTF and DMSO with different concentration and time.
ResultThe stabilities were variant according to different softwares. The rank orders of stability were geNorm: Actin=ef1a >SamDC > ARC > TUA6; NormFinder:SamDC > ARC > Actin > ef1a > TUA6; BestKeeper: Actin > ef1a > SamDC > ARC > TUA6; Delta CT: Actin > ef1a > SamDC > ARC > TUA6; RefFinder: Actin > SamDC > ef1a > ARC > TUA6. With a single analysis of DMSO treatment by RefFinder showed that ef1a > SamDC > Actin > TUA6 > ARC.
ConclusionActin is the stablest reference gene under GTF and DMSO treatments, while ef1a is the stablest one under DMSO treatment.
-
Keywords:
- Ricinus communis /
- GTF /
- DMSO /
- RT-qPCR /
- internal reference gene /
- stability
-
精密播种可实现1穴1粒和固定株距,从而减少用种量、降低劳动强度、节本增效。排种器作为播种机的核心部件直接决定播种精度[1-2]。油菜种子粒径小,其精密排种器设计难度大[3]。气力式排种器适用于高速作业,生产效率高,对种子适应性强、损伤轻,但结构复杂、加工成本高,且风机动力消耗大、性能不稳定[4];窝眼轮式精密排种器属机械式,对不同粒径种子通用性差,但结构简单、加工成本低、性能可靠,在我国精密播种机上应用广泛[5-6]。
型孔是窝眼轮式精密排种器结构组成的重要部分,其形状及参数直接影响排种器的工作性能。Garcia [7]研究发现型孔的形状、尺寸对排种精度有着重要的影响;Wang [8]根据种子尺寸对排种器型孔参数进行了优化设计;吴兆迁等[9]设计了针对不同粒径种子孔深可调的窝眼轮排种器,解决了播量调节不便的问题;宋井玲等[10]设计了1种利用凸轮活销机构实现工作过程中孔深可变的型孔轮式排种器,适用于玉米、大豆等大粒种子。而油菜种子粒径小、流动性强,对窝眼轮型孔结构要求更高,但是目前国内对于窝眼轮式油菜精密排种器型孔结构的研究甚少,使得适用于油菜等小籽粒种子的窝眼轮排种器设计理论不足。
传统的试验周期长、成本高,随着计算机技术的发展,计算机辅助分析方法在排种器研究领域的应用日渐增多。Zhang等[11]采用离散元法研究了大豆在斜槽中的流动过程;石林榕等[6]借助EDEM软件对水平圆盘式精量排种器排种进行了仿真试验。本文利用离散单元颗粒分析软件EDEM,对不同型孔结构的窝眼轮式油菜精密排种器工作机理进行仿真分析和验证试验,探寻不同型孔结构对窝眼轮排种器种子群扰动及工作性能的影响,为窝眼轮式油菜精密排种器的设计工作提供理论依据。
1. 种子群扰动机理分析
1.1 接触模型的建立
排种器工作时,种箱中的油菜种子在窝眼轮转动作用下发生扰动,引起种子间的碰撞产生接触力[12-13]。离散元分析方法中将接触模型分为软颗粒接触和硬颗粒接触,其中软颗粒接触模型可以允许碰撞持续一定的时间,并同时考虑多个颗粒的碰撞,根据颗粒碰撞重叠量和切向位移来计算接触力[14], 种子群扰动与该接触力紧密相关。考虑到油菜种子无表面粘附力,故选择Hertz-Mindlin(no slip)软颗粒接触模型[15-16]。将该模型的接触简化为有耦合器和滑动器的弹簧振子阻尼振动,如图 1所示,其运动微分方程为:

式中,m为模型粒子质量;u为偏离平衡位置位移;c为接触阻尼系数;K为弹簧弹性系数。
1.2 接触力分析
软接触颗粒碰撞模型中接触力可分解为法向力和切向力,其中法向力是模型中弹性力和阻尼力的合力。对于油菜籽的三维球形颗粒,由Hertz接触理论,法向力Fn以及切向力Ft可分别表示为:

式中kn、kt分别为法向及切向弹力系数;cn、ct分别为法向和切向阻尼系数;α为法向重叠量;νij为颗粒i与j的相对速度;νct为接触点滑移速度;δ为切向位移;n为颗粒i与颗粒j接触面的法向单位矢量。
若下式成立:

则颗粒i与颗粒j发生相对滑动,此时有:

式中μs为静摩擦因数,由油菜种子的物理特性确定,为定值;nt为切向单位向量。由公式可知,种子之间的内摩擦力即上述接触模型中的切向力是由法向力确定的,也是产生种子群扰动的主要因素[17-18]。因此以法向接触力Fn为内摩擦力的监测值分析不同型孔结构各轮种子群扰动强度,探寻型孔结构对窝眼轮式油菜精密排种器排种性能的影响。
2. 仿真分析
2.1 窝眼轮式排种器结构及工作原理
窝眼轮式油菜精密排种器由窝眼轮、外壳、清种刷、护种板、排种轴等组成,如图 2所示。排种器充种角度为90°,护种区包角为120°。窝眼轮直径、厚度分别为60、20 mm。为减少漏播,型孔底部窝眼直径D应不小于种子最大尺寸,小于2粒种子的最小尺寸和,孔深H应等于或略大于种子的最大尺寸[9, 19],根据试验所用种子的物理特性,设计D、H分别为2.5、2.3 mm。按型孔倒角不同,结合窝眼轮材料特性及油菜种子的三维尺寸、摩擦角等物理特性,根据不同倒角参数仿真结果,设计了30°倒角(A轮)、不倒角(B轮)以及半径1.25 mm倒圆角(C轮)3种窝眼轮。为确保型孔完整的同时尽可能多地布置型孔以提高充种能力和工作效率,根据窝眼轮直径和型孔尺寸,确定窝眼轮圆周面均布型孔数目为30个。A、B、C 3种窝眼轮结构如图 3所示。
工作时,排种轴带动窝眼轮匀速转动,油菜种子在重力及种间接触力的作用下由种箱进入型孔完成充种过程,经过清种刷后随着窝眼轮进入护种区,转出护种区后,靠重力作用落下,进入种沟,完成排种过程。
2.2 模型建立及仿真
借助Pro-E软件建立排种器模型,定义清种刷为尼龙材料、其余部件为有机玻璃;建立输送带模型,并定义种子与输送带为完全非弹性碰撞。模型导入EDEM软件后网格显示如图 4所示。
种子与种子、种子与排种器之间选用Hertz-Mindlin(no slip)接触模型,种子与输送带之间选择Moving Plan接触模型;导入模型并按表 1、2设置材料特性及材料间接触参数[13, 20-21]。设置颗粒产生方式为静态填充,颗粒半径1 mm并服从正态分布;设置仿真时间步长比例为20%,总时间6 s(第1秒生成颗粒,2~6 s排种),网格尺寸为最小颗粒半径的2倍。
表 1 仿真模型材料参数Table 1. Property parameter of material in the simulation model 表 2 仿真模型材料接触参数Table 2. Contact parameter of material in the simulation model
表 2 仿真模型材料接触参数Table 2. Contact parameter of material in the simulation model
综合考虑油菜种植农艺要求、国内油菜播种机的作业速度水平以及试验排种器的结构参数,在10、20、30、40、50 r·min-1下对A、B、C 3种不同型孔结构的窝眼轮排种器进行仿真分析。图 5显示了各轮30 r·min-16 s时的仿真情况,种箱里种子的堆积情况反映出种子群扰动量为:A轮>C轮>B轮。
2.3 仿真结果分析
2.3.1 不同型孔结构对种子群扰动的影响
30 r·min-1时,A、B、C 3种窝眼轮上方同一位置框选区域中,种子颗粒间接触的平均法向应力以及颗粒的平均速度随时间波动如图 6、7所示。图 6显示各轮平均法向应力随时间变化无规律波动,其中A轮波动最明显,C轮其次,B轮波动最小;A、B、C 3轮平均法向应力均值并无明显区别。由图 7可知,种子颗粒平均速度为:A轮>C轮>B轮。图 6中B轮在5.5~5.8 s法向应力波动变小,而图 7中显示该时段B轮种子颗粒的平均速度也显著降低,观察仿真录像发现B轮此时段充种情况较差(图 8),可见平均法向应力波动能有效反映种子群扰动,且种子群扰动对充种性能影响显著。种子群扰动量越大,种子运动越剧烈,种子瞬时平均速度也越大,更容易在重力和相互碰撞作用下进入型孔完成充种过程。
图 9反映了各轮上方框选区域中种间平均法向应力的均值和方差随转速提高的变化情况。图 9a显示,各轮的法向应力均值均随转速提高先增大后趋于平缓,此过程中B、C轮比A轮先达到拐点;10~30 r·min-1转速下,三轮的法向应力均值出现交叉,转速超过30 r·min-1后,各轮法向应力均值差异逐渐明显。由图 9b可知,A、B、C轮法向应力方差随转速提高而增大,B轮增幅明显小于A、C轮,此过程中,A、B、C轮方差排序为:A轮>C轮>B轮。结合前文所述法向应力、种子群扰动及充种性能的关系可知,相同转速下,各轮的种子群扰动量关系为:A轮>C轮>B轮,且A轮充种性能最好。
2.3.2 不同型孔结构对排种器各工作指标的影响
每次仿真完成后,输出输送带上表面框选区域中油菜种子x坐标值以获取粒距样本,按文献[22]所述方法,对排种器的基本性能指标:粒距合格指数、漏播指数、重播指数、变异系数进行计算,排种性能仿真结果见图 10。
图 10a表明,各轮合格指数均随转速的提高而降低,且A轮>C轮>B轮,且随着转速的提高,各轮合格指数间差值呈增大趋势,型孔结构不同使得各轮的种子群扰动量、充种性能不同。图 10b表明各轮重播指数均随转速的提高而降低,且A轮>C轮>B轮,观察仿真录像发现,型孔结构差异使得A轮型孔的囊种空间大于B轮和C轮,当2粒直径较小的种子同时出现在型孔上方时,A轮出现重播的可能性比B、C轮大。图 10c表明,各轮漏播指数均随转速提高而增加,且B轮>C轮>A轮,且各轮漏播指数差值随转速提高逐渐增大,A轮相比于B、C轮漏播指数增速较为平缓;对照图 9可知,就各轮自身而言,工作转速是影响其漏播的主要因素,平均法向应力的均值和方差对漏播影响不大,而相同转速下,各轮之间对比发现,法向应力方差对漏播影响显著,法向应力方差越大则漏播指数越小,而平均法向应力均值的影响不明显。图 10d表明,各轮的变异系数均随转速提高而增大,A轮变异系数最大,B、C轮变异系数差异不明显,在20、50 r·min-1时两者出现交叉;在EDEM中观察种子运动轨迹发现A轮的投种位置变动较大,故其投种时间间隔误差大,粒距变异系数大,这是由于型孔结构导致种子进入A轮型孔后活动范围大所致。
3. 验证试验与分析
按仿真模型参数定制了A、B、C 3种窝眼轮,安装到同一个窝眼轮排种器上,在南京农业大学工学院自制的铺砂式排种性能测试台上进行试验,其工作原理及参数见文献[23]。以仿真建模所参照的中双11号油菜种子为试验材料,测得其平均粒径1.72 ~2.21 mm、千粒质量4.68 g、密度1.06 g·cm-3、容重0.67 g·cm-3、纯净度98.5%。
试验选取与仿真相同的5种转速,每次试验添加到种箱的种子均为89 g(与仿真时约19 060粒种子质量相同),监测指标及计算方法与仿真分析相同。排种性能试验结果如图 11所示。
对比图 10、11发现,试验中各排种性能指标在数值上与仿真结果有一定偏差,但其变化趋势及其相互之间大小关系与仿真结果基本一致。由图 10a、11a可知,试验中各轮的合格指数随转速提高而下降的速度比仿真中要快,仿真中转速从10 r·min-1增加到50 r·min-1时A、B、C轮的合格指数分别从96.1%、93.1%、94.2%降低到89.8%、75.9%、81.5%,而试验结果中A、B、C轮的合格指数分别从95.8%、90.6%、93.5%降低到86.6%、67.5%、79.2%。B轮合格指数受转速影响最大、C轮次之、A轮最小。由图 10b、11b可以看出,各轮重播指数在试验与仿真中结果差异不明显。由图 10c、11c可知,试验中各轮漏播指数均高于相同转速下仿真中漏播指数,且各轮漏播指数受转速的影响在试验结果中比仿真中表现的更为明显,转速为10 r·min-1时,A、B、C轮试验和仿真漏播指数分别为:0.7%、7.2%、3.0%和0.5%、4.3%、2.4%,当转速增加到50 r·min-1时,A、B、C轮试验和仿真漏播指数分别升高到:12.4%、32.3%、20.1%和9.3%、23.9%、18.1%,可见B轮漏播指数受转速变化的影响最大,A轮最小,这与前文所述不同型孔结构对种子群扰动量及囊种空间大小的影响一致。观察图 10d、11d发现,变异系数随转速提高而上升,但试验中各轮变异系数均比相同转速下仿真中变异系数大,这与种子落到输送带时弹跳、粒距测量精度、输送带速度均匀性、排种器工作转速稳定性等因素有关。
通过仿真及试验发现,A轮在重播指数和变异系数略高于B、C轮的同时,其漏播指数和合格指数明显优于B轮和C轮,对高速作业具有更强的适应性。
4. 结论
1) 借助离散元分析软件EDEM,以接触平均法向应力均值和方差为监测值研究了型孔结构对窝眼轮排种器种子群扰动的影响,发现相同转速下A轮种子群扰动量最大、C轮次之、B轮最小,且种子群扰动量越大充种性能越好。
2) 按仿真建模参数加工了3种窝眼轮,并进行了排种性能验证试验。综合考虑仿真和试验结果,对各轮自身而言,影响其排种性能的主要因素是工作转速,随工作转速提高各轮的合格指数、重播指数均减小,漏播指数、变异系数增大;各轮之间对比发现,相同转速下,种子群扰动量越大漏播指数越小,型孔囊种空间因倒角方式而不同,且囊种空间越大,重播指数、变异系数越大;由于重播指数较小,故合格指数主要受漏播指数影响。试验结果显示,转速在10~50 r·min-1时,种子群扰动最大的A轮合格指数为86.6%~95.8%,明显优于B轮的67.5%~90.6%和C轮的79.2%~93.5%。
3) 仿真与试验的结果在数值上有偏差,但其变化趋势及相互之间大小关系基本一致,用EDEM对排种器进行仿真分析具有一定可行性。
-
表 1 RT-qPCR候选内参基因的引物序列
Table 1 Primer sequences of selected house-keeping genes for RT-qPCR

表 2 5个候选内参基因的标准曲线参数
Table 2 Parameters derived from standard curves for five candidate reference genes

-
[1] 徐汉虹, 张志祥, 程东美, 等.导向农药[J].世界农药, 2004(5): 3-9. doi: 10.3969/j.issn.1009-6485.2004.05.002 [2] DOIDY J, GRACE E, KUHN C, et al. Sugar transporters in plants and in their interactions with fungi[J]. Trends Plant Sci, 2012, 17(7):413-422. doi: 10.1016/j.tplants.2012.03.009
[3] YANG W, WU H, XU H, et al. Synthesis of glucose-fipronil conjugate and its phloem mobility[J]. J Agr Food Chem, 2011, 59(23):12534-12542. doi: 10.1021/jf2031154
[4] WU H, YANG W, ZHANG Z, et al. Uptake and phloem transport of glucose-fipronil conjugate in Ricinus communis involve a carrier-mediated mechanism[J]. J Agr Food Chem, 2012, 60(24): 6088-6094. doi: 10.1021/jf300546t
[5] DENIS M, DELROT S. Carrier-mediated uptake of glyphosate in broad bean (Vicia faba) via a phosphate transporter[J]. Physiol Plantarum, 1993, 87(4):569-575. doi: 10.1111/ppl.1993.87.issue-4
[6] FUJITA M, SHINOZAKI K. Identification of polyamine transporters in plants: Paraquat transport provides crucial clues[J]. Plant Cell Physiol, 2014, 55(5): 855-861. doi: 10.1093/pcp/pcu032
[7] CHOLLET J, DELETAGE C, FAUCHER M, et al. Synthesis and structure-activity relationships of some pesticides with an alpha-amino acid function[J]. Biochim Biophys Acta, 1997, 1336(2): 331-341. doi: 10.1016/S0304-4165(97)00041-X
[8] POSTOLLEC F, FALENTIN H, PAVAN S, et al. Recent advances in quantitative PCR (qPCR) applications in food microbiol[J]. Food Microbiol, 2011, 28(5): 848-861. doi: 10.1016/j.fm.2011.02.008
[9] 袁伟, 万红建, 杨悦俭.植物实时荧光定量PCR内参基因的特点及选择[J].植物学报, 2012(4): 427-436. http://d.old.wanfangdata.com.cn/Periodical/zwxtb201204009 [10] VANDESOMPELE J, DE PRETER K, PATTYN F, et al. Accurate normalization of real-time quantitative RT-PCR data by geometric averaging of multiple internal control genes[J]. Genome Biol, 2002, 3(7): H34. http://d.old.wanfangdata.com.cn/OAPaper/oai_pubmedcentral.nih.gov_126239
[11] TONG Z, GAO Z, WANG F, et al. Selection of reliable reference genes for gene expression studies in peach using real-time PCR[J]. BMC Mol Biol, 2009, 10(1): 71. doi: 10.1186/1471-2199-10-71
[12] HUGGETT J, DHEDA K, BUSTIN S, et al. Real-time RT-PCR normalisation, strategies and considerations[J]. Genes Immun, 2005, 6(4): 279-284. doi: 10.1038/sj.gene.6364190
[13] HONG S, SEO P J, YANG M, et al. Exploring valid reference genes for gene expression studies in Brachypodium distachyon by real-time PCR[J]. BMC Plant Biol, 2008, 8(1):112. doi: 10.1186/1471-2229-8-112
[14] SUZUKI T, HIGGINS P J, CRAWFORD D R. Control selection for RNA quantitation[J]. Biotechniques, 2000, 29(2): 332-337. doi: 10.2144/00292rv02
[15] BARROS R T, KHAJURIA C, WANG H, et al. Validation of reference housekeeping genes for gene expression studies in western corn rootworm (Diabrotica virgifera virgifera)[J/OL]. PLoS One, 2014, 9(10): e109825. http://www.plosoneorg.sci-hub.org/article/fetchobject.action?uri=info:doi/10.1371/journal.pone.0109825&representation=PDF.
[16] 魏永赞, 赖彪, 胡福初, 等.用于荔枝qPCR分析的内参基因克隆及稳定性分析[J].华南农业大学学报, 2012, 33(3): 301-306. doi: 10.3969/j.issn.1001-411X.2012.03.006 [17] GUTIERREZ L, MAURIAT M, GUENIN S, et al. The lack of a systematic validation of reference genes: A serious pitfall undervalued in reverse transcription-polymerase chain reaction (RT-PCR) analysis in plants[J]. Plant Biotechnol J, 2008, 6(6): 609-618. doi: 10.1111/pbi.2008.6.issue-6
[18] ANDERSEN C L, JENSEN J L, ORNTOFT T F. Normalization of real-time quantitative reverse transcription-PCR data: A model-based variance estimation approach to identify genes suited for normalization, applied to bladder and colon cancer data sets[J]. Cancer Res, 2004, 64(15): 5245-5250. doi: 10.1158/0008-5472.CAN-04-0496
[19] PFAFFL M W, TICHOPAD A, PRGOMET C, et al. Determination of stable housekeeping genes, differentially regulated target genes and sample integrity: BestKeeper:Excel-based tool using pair-wise correlations[J]. Biotechnol Lett, 2004, 26(6): 509-515. doi: 10.1023/B:BILE.0000019559.84305.47
[20] SILVER N, BEST S, JIANG J, et al. Selection of housekeeping genes for gene expression studies in human reticulocytes using real-time PCR[J]. BMC Mol Biol, 2006, 7(1):33. doi: 10.1186/1471-2199-7-33
[21] XIE F, SUN G, STILLER J W, et al. Genome-wide functional analysis of the cotton transcriptome by creating an integrated EST database[J/OL]. PLoS One, 2011, 6(11): e26980. http://www.plosone.org.sci-hub.org/article/fetchobject.action?uri=info:doi/10.1371/journal.pone.0026980&representation=PDF.
[22] JAIN M, NIJHAWAN A, TYAGI A K, et al. Validation of housekeeping genes as internal control for studying gene expression in rice by quantitative real-time PCR[J]. Biochem Biophys Res Commun, 2006, 345(2): 646-651. doi: 10.1016/j.bbrc.2006.04.140




 下载:
下载: